歡迎關注凱萊英藥聞公眾號
原文連結:https://mp.weixin.qq.com/s/JcpJ2A9rIZo05mIzbw7igQ
12月6日,丹麥疫苗公司Bavarian Nordic正式宣佈將啟動RSV疫苗MVA-BN RSV的3期臨床試驗。BavarianNordic已聘請了一家CRO公司,預計將於2022年上半年開啟該項關鍵3期臨床試驗,招募2萬名受試者,在多個地區的臨床中心開展,總費用預估為2.5美元,全部來自於股權融資,用於融資的股權約佔Bavarian Nordic總股本的10%。
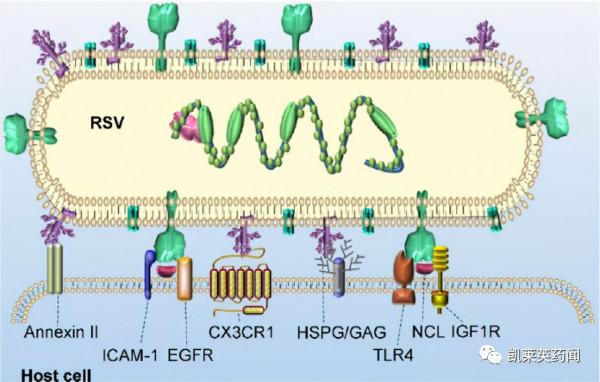
呼吸道合胞病毒(RSV)屬於副黏病毒科的肺病毒屬(Pneumovirus),是一種常見病毒,通常會引起輕微的感冒症狀,但在嚴重情況下會導致嚴重的肺部感染,包括毛細支氣管炎和肺炎,最終可能導致死亡。高危人群通常包括嬰兒、老年人和免疫缺陷人群。
據估計,在美國,每年由RSV引起的65歲及以上成年人感染住院的約為1775251例,其中約140001例死亡。因此,預防RSV引起的感染是全球各國政府和醫療專業人員的當務之急。目前還沒有經監管機構批准上市的RSV疫苗。因此,RSV構成了一個巨大而關鍵的未滿足醫療需求,潛在RS疫苗市場約為每年數十億美元。
Bavarian Nordic的RSV候選疫苗MVA-BN RSV主要目標人群為老年人,包含五種不同的RSV抗原,透過模擬人體對RSV感染的自然應答,刺激人體針對兩種RSV亞型(A和B)產生廣泛免疫應答。包含五種抗原使MVA-BN RSV不同於當前正在研製的其他廠家候選RSV疫苗。
今年9月,Bavarian Nordic報告了一項雙盲、安慰劑對照2期臨床試驗積極結果,該試驗受試人員為18-50歲的健康成年志願者,被隨機分配接受MVA-BN RSV或安慰劑疫苗接種。在接種疫苗28天后,志願者接受鼻內注射RSV A型毒株,61名受試者疫苗保護情況可評估。
結果表明,與安慰劑組(n=31)相比,MVA-BNRSV組受試者(n=30)病毒載量顯著降低,達到主要終點。同時,接種疫苗的受試者表現出與RSV感染相關的臨床症狀顯著減少。MVA-BN RSV疫苗在預防症狀性RSV感染方面的效力高達79%。
此前,Bavarian Nordic報告的另一項2期臨床試驗中,納入了421名55歲及以上的老年受試者,結果顯示MVA-BN RSV具有良好的耐受性,並誘導了廣泛且持久的抗RSV抗體和T細胞應答,以及粘膜免疫應答,這些對於預防RSV可能產生重要的保護。老年受試者的2期臨床中包括受試者在一年後重新接種疫苗,二次接種後免疫應答迅速且顯著增加,尤其是接種前免疫力最弱的受試者接種後顯著強化了免疫應答水平。
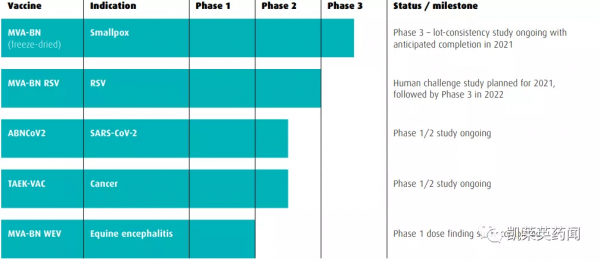
該疫苗基於Bavarian Nordic專有的MVA-BN技術平臺開發而來,該公司基於MVA-BN技術平臺還開發了天花和埃博拉疫苗。