來源:小桔燈網
作者:中國食品藥品檢定研究院
導語丨 2019年,中國食品藥品檢定研究院體外診斷試劑所組織開展了病原宏基因組高通量測序(mNGS)檢測試劑質量評價聯合研究,得到了包括復旦大學附屬華山醫院感染科、同濟大學附屬東方醫院檢驗科、中國醫學科學院北京協和醫院檢驗科及上海交通大學醫學院附屬上海兒童醫學中心4家醫院,中國醫學科學院病原生物研究所、中國疾病預防控制中心傳染病預防控制所及北京化工大學生命科學與技術學院3家科研院所,以及13家體外診斷試劑企業的大力支援和深度參與。本次多中心質量評價聯合研究,透過對mNGS檢測的靈敏度、特異性、準確率及其相關影響因素進行深入探究和分析,對國內相關產品的效能概況、技術特點、現存問題及面臨的挑戰進行全面系統的梳理,初步建立了mNGS質量評價方法,併為mNGS的發展提出技術性建議。
該研究成果於2021年12月發表在柳葉刀雜誌(Lancet)子刊EBioMedicine。中國食品藥品檢定研究院劉東來、周海衛副研究員,雲南農業大學雲南省動物基因編輯及體細胞克隆技術重點實驗室許騰教授,中國醫學科學院北京協和醫院檢驗科楊啟文教授,上海交通大學醫學院附屬上海兒童醫學中心莫茜教授為共同第一作者。中國食品藥品檢定研究院王佑春、張春濤、許四宏研究員,復旦大學附屬華山醫院感染科張文宏教授,同濟大學附屬東方醫院檢驗科吳文娟教授為共同通訊作者。
病原宏基因組高通量測序檢測試劑效能
多中心評估
- 01 -
概 述
背景:病原宏基因組高通量測序技術(mNGS)已廣泛應用於臨床感染性疾病病原學診斷,然而目前大多數研究對該項技術的評估還不夠全面和細緻。
方法:本研究透過設計病原微生物參考品及其相關效能評價指標,對17家單位的mNGS檢測試劑的效能進行質量評價,重點關注mNGS技術的檢測可靠性、關鍵影響因素、精密度以及該技術用於定量檢測的潛力。
結果:研究發現,不同的mNGS 檢測試劑、對於不同種類的病原微生物,其檢測效能表現出顯著差異。常規情況下,20M測序資料量(2000萬條測序序列)價效比高,可以滿足檢測效能需求。基於測序序列數可用於推測微生物的相對丰度。
總結:mNGS檢測效能受到微生物種類、人源宿主核酸含量、測序資料量等因素的顯著影響。對於不同的mNGS試劑,其操作流程和測序平臺、檢測結果的假陽性問題等,均是mNGS檢測準確性和定量面臨的技術挑戰。本研究建議,對於mNGS檢測試劑,至少應在臨床樣本常見的人源細胞背景下(105 cells/mL),實現24小時內,20M測序資料量的情況下,具備≥500 CFU/mL(或copies/mL)病原微生物的靈敏度效能。
- 02 -
實 驗 設 計
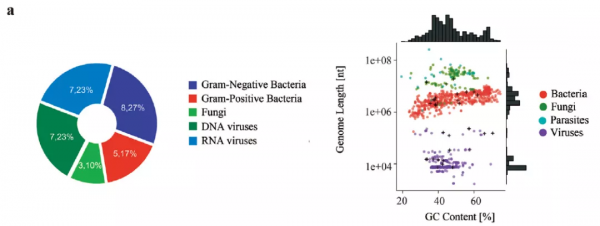
研究選擇革蘭氏陽性菌、革蘭氏陰性菌、真菌、DNA病毒、RNA病毒共19屬、30種病原微生物,嚴格設計並製備9份參考品。所選病原體在病原種類、基因組大小、GC含量等方面覆蓋廣泛,可用於代表實際臨床樣本中病原體的多樣性(圖1a)。
圖1a 30種病原體種類與GC含量分佈
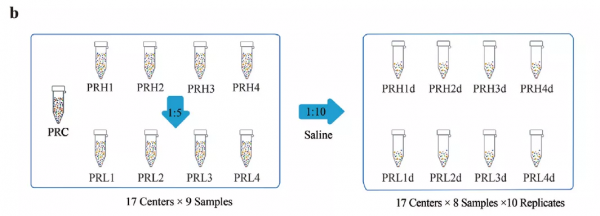
9份參考品中,1份是陰性對照,另外8份參考品分為高含量組(PRH)和低含量組(PRL),並且高低含量組兩兩配對,其宿主細胞核酸的含量相同,雖病原體種類也相同,但其含量比值為5:1。同時每份參考品樣本稀釋10倍,用於評估mNGS定量效果(圖1b)。
圖1b 9份參考品設定圖
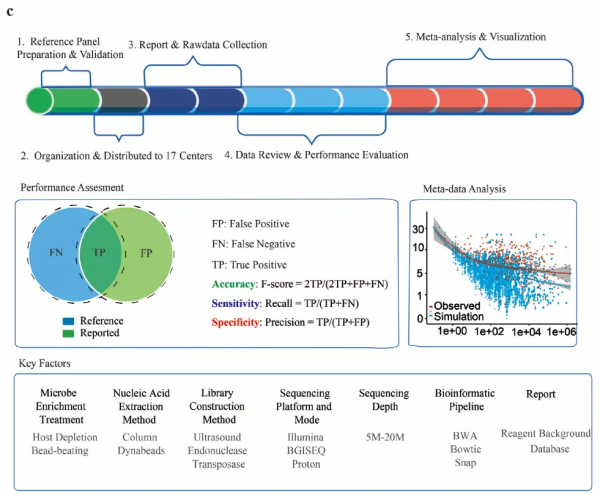
9份參考品分發給17個實驗室進行盲測與生物資訊分析(17個實驗室共有4種前處理方法,2種核酸提取方法,3種文庫構建方法,6種測序平臺,4種生信分析流程)。評估mNGS檢測結果靈敏度(按召回率Recall計算所得)、特異性(按精確率Precision計算所得)和準確率(按F-score計算所得,精確率和召回率的綜合評估指標)(圖1c)。
圖1c (1)多中心研究計劃總覽(2)結果回收後mNGS檢測效能評估指標與計算方式(準確率F-score、靈敏度Recall、特異性Precision)(3)檢測流程關鍵環節可選方法概覽(如核酸提取選擇有柱提法和磁珠法2種)
- 03 -
各實驗室mNGS檢測效能評估結果
各實驗室室間檢測能力差異顯著(圖2a)。 F-scores這一指標得分在0.5-1之間,平均F-score為0.81,其中有兩家總體得分為1(檢測準確,無多報,無少報);召回率(評估靈敏度)平均為0.88,室間差異較小(0.75-1.0);精確率(評估特異性)平均為0.77,室間差異較大(0.45-1.0)。
圖2a 各檢測單位的召回率、精確率、準確率得分情況
實驗室間檢測效能差異主要體現為假陽性的判斷能力。具體分析各實驗室出現的真陽性、假陽性、假陰性物種,發現室間真陽性與假陰性結果較為一致,而假陽性物種數量室間差異大。另外,實驗室間真菌和RNA病毒的檢測能力差異大(圖2d)。無論是低含量或高含量組,所有種類微生物中RNA病毒檢測最具挑戰,平均召回率只有0.71。革蘭氏陽性和革蘭氏陰性細菌召回率最高(0.96和0.94),其次為DNA病毒(0.89)和真菌(0.80)。
圖2d 各病原體型別的召回率
(RNA病毒平均召回率相對其他病原體低)
- 04 -
更深的本土化,
超mNGS靈敏度受微生物與宿主核酸比率影響
微生物與宿主核酸比率是影響mNGS檢測靈敏度的關鍵因素。結果顯示,無論參考品是否進行1:10稀釋,高含量組與低含量組檢出序列數仍然呈現5倍差距,且稀釋前與稀釋後檢出序列數沒有差異。按細菌、病毒、真菌分類後,依然觀察到相似的模式(圖3 a、b)。該結果指出微生物與宿主核酸比率不變的情況下(如1:10稀釋),雖然參考品中病原體濃度降低,但檢測靈敏度並未受到顯著影響,即mNGS的檢測靈敏度需要綜合宿主核酸與微生物含量兩個因素,而不是隻考慮微生物含量。
圖3 病原體相對含量、絕對含量(如稀釋)(a)及類別(b)等因素對mNGS靈敏度的影響
- 05 -
室間或室內微生物丰度比較
室內結果表明mNGS可以實現病原體相對定量。透過微生物投入量,基因組大小等引數計算的期望丰度值與實際丰度符合線性迴歸,即可以透過線性迴歸模型等實現微生物的相對含量推測。
室間結果表明不同實驗室測出來的RPM(Reads per Million, 每1M資料量測到的序列數)差異顯著(圖3e),因此室間比較病原體丰度的價值有限。去宿主核酸和柱提法會產生較高的RPM,研磨破壁步驟會使RPM變低(圖3f)。研究者推測原因可能是去宿主核酸有助於提高各種微生物檢出率,研磨破壁可能降低RNA病毒檢出率。
圖3e 各實驗室間RPM差異顯著
圖3f 研磨破壁、去宿主核酸、柱提法等不同實驗室操作方法與微生物丰度的關係
- 06 -
mNGS精密度受實驗室流程影響
為了評估mNGS檢測結果的精密度,研究者應用收集到的各實驗室報告的結果,評估每一檢測點檢出序列的變異係數(CV,coeffecient of variations)。各檢測點的CV分佈在0.12~1.1之間,平均CV為0.65。
不同檢測流程比較中,去宿主核酸流程CV較低,可能是因為去宿主核酸後提升病原體序列數,促使結果更穩定;核酸內切酶建庫法的CV(0.4)顯著低於轉座酶建庫法的CV(1.0),表明轉座酶建庫法是導致結果差異的重要步驟,可能原因是該方法相較對文庫構建過程中的DNA輸入量比較敏感(圖4b);不同種類微生物檢測中,真菌檢測CV最高,結果最不穩定。
圖4b 不同檢測流程下檢測結果的變異係數
研究者進一步探究測序資料量相關抽樣噪音對檢測精密度的影響。發現模擬抽樣噪音產生的差異總是低於觀察到的總體差異,表明除了測序相關因素外,其它實驗因素對精密度也產生相當大的影響。以上結果表明當設計方案評估宏基因組檢測時,需要充分考慮不同實驗因素帶來的影響;在更好的理解和控制不同實驗因素產生影響前,精準定量病原體頗具挑戰。
- 07 -
mNGS靈敏度受測序資料量影響
相較於核酸提取,文庫構建等步驟,樣本前處理對檢測效能影響較大。其中去宿主核酸可以顯著提高檢測效能,而研磨破壁技術並不一定能夠起到好的效果,總體上是降低了病原體尤其是RNA病毒的檢測效能。其它檢測流程的差異與檢測效能沒有顯著相關性。
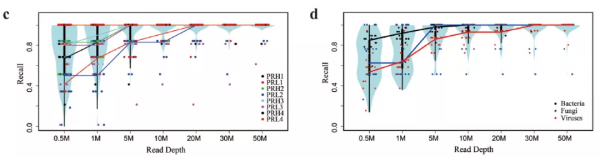
測序資料量是影響宏基因組檢測結果的關鍵因素。一般來說20M資料量可以滿足絕大部分檢測需求。隨著測序資料量增加,mNGS檢測效能逐步提升,而到10M後逐步達到平臺期。從本次所有參與的實驗室結果來看,達到20M測序資料量時,已經可以檢測到絕大部分本次設計中的微生物,隨後繼續增加測序深度,收益顯著下降(圖5c)。
分微生物種類來看,5M資料量時,真菌檢測達到平臺期,10M資料量時,細菌檢測達到平臺期,20M資料量時,病毒檢測達到平臺期(圖5d)。檢測結果也與先前的推論符合,即mNGS檢測靈敏度與微生物基因組大小相關,病毒等小基因組物種需要更多的測序資料量。
圖5 樣本維度(c)及病原體種類維度(d)測序資料量對召回率的影響
- 08 -
mNGS檢測特異性受到背景微生物的挑戰
背景微生物引起的假陽性將會影響mNGS的特異性。探究假陽性的原因,總體分為四類:交叉汙染、背景微生物、錯誤種屬鑑定、病毒錯誤分型。其中,背景微生物(49%)和錯誤種屬鑑定(39%)是最主要的假陽性原因(圖6c、d),不同實驗室間的表現差異也是最大的,而比對演算法差異不是導致錯誤種屬鑑定的關鍵因素。
背景微生物主要受溼實驗流程影響,它既可以來源於通用流程,也可來源於各實驗室的特有流程。不同實驗室需要有各自的方法排除干擾,提高檢測精確度。另外,研究發現高背景微生物不一定代表更差的檢測表現,表明除了要減少背景微生物外,有效的背景微生物資料過濾也十分重要。
另外,研究者發現真陽性物種具有比較高的基因組覆蓋度和較低的片段序列測序深度,基於此可從假陰性裡找回部分真陽性結果。假陽性物種具有顯著較低的基因組覆蓋度,同時背景微生物導致的假陽性物種具有顯著較高的片段序列測序深度。根據上述發現,本研究透過機器學習的方法,設定了一個假陽性過濾器,可以有效的減少假陽性物種(34種減少到11種),同時不會影響真陽性物種。
圖6 各實驗室報告背景微生物數量(c)及假陽性原因(d)
討論
本研究面向17個實驗室,應用各單位的mNGS檢測試劑對9份模擬呼吸道和腦脊液臨床樣本的參考品進行檢測,並對檢測結果進行了統計和分析。本研究是目前為止,最深入、最全面的mNGS檢測試劑質量評價聯合研究。本研究條件下,對於病原體檢測需求,20M測序資料量基本可以滿足。由於mNGS技術的複雜性,對於其它型別的臨床樣本或非典型標本,需要慎重考慮或評估測序資料量。宿主核酸含量會極大影響宏基因組病原微生物檢測靈敏度效能,去宿主核酸有益於提高檢測靈敏度,但應進行充分驗證。目前,有眾多去宿主核酸方法,應用前需要經過驗證,確保這些方法不會非特異性的去除病原體。
同時也應注意本研究的侷限性。參考品不能完全代表臨床樣本,比如真實臨床樣本中還含有許多遊離核酸;本研究無法確定在真實臨床樣本中,破壁流程和不同的建庫方法會不會產生顯著差異;此次研究是由不同檢測平臺與流程,共同檢測同一批參考品,檢測結果有助於發展和最佳化病原檢測流程。