1959 年,諾貝爾獎得主、理論物理學家理查德 - 費曼最早提出了納米技術,他曾設想 —— 未來,奈米級微型機器人將會用於治療人體疾病。這種微奈米機器人可以像醫生一樣,可以在人體內透過 “手術” 切割病灶。
直到 20 世紀 90 年代,隨著半導體工業、微奈米加工工藝的發展,微奈米機器人得以真正發展起來。如今,這些微小的奈米級機器人正在顛覆著生物醫藥領域的發展,現已被廣泛應用於微創手術、細胞操作和分析以及靶向治療等方面,在癌症診斷和藥物輸送成績尤為突出。
今年 9 月,北京航天航空大學(以下簡稱 “北航”)馮林團隊開發出了一種基於活巨噬細胞作為藥物遞送載體的三維磁控細胞機器人(Magnetized cell-based robots,MCRs)系統。這套系統由磁操作平臺(MMP)和磁化微 / 奈米機器人(MMR)兩部分組成。當 MCR 進入體內時,可以透過體外操作 MMP,將 MCR 精準遞送至腫瘤部位,實現靶向給藥。這項研究成果已作為封面文章發表在 Small 期刊上。
在這項研究中,他們保持了巨噬細胞天然吞噬腫瘤的活性,同時也避免了免疫排斥反應。
“微奈米機器人最終是要應用於臨床腫瘤治療上,並非只是炒概念。我們的真正優勢在於把微奈米機器人應用於小鼠體內,且腫瘤抑制率達到了 91%。” 馮林說。
藉此機會,就這項研究的突破性以及微奈米機器人的應用潛力,生輝與馮林教授聊了聊。
馮林現在是北航機械工程及自動化學院的副教授,他博士畢業於名古屋大學微奈米系統專業。今年是馮林加入北航的第 5 個年頭,他於 2016 年透過 “卓越百人” 計劃回到北航建立實驗室開展獨立研究。目前,馮林實驗室的研究方向主要集中在微奈米機器人上,包括基於場控微奈米機器人的藥物靶向遞送系統、主動可控胃腸鏡膠囊機器人以及微奈米級高通量光電鑷微作業系統等。

圖 | 北航機械工程及自動化學院副教授馮林(來源:受訪者提供)
精準靶向實體瘤,抑瘤效果 91%
加入北航之後,馮林的研究重點逐漸從細胞克隆轉移到腫瘤主動靶向給藥,開發磁控微型機器人,包括膠囊機器人、微奈米機器人等。
近期,該實驗室開發出了一種以巨噬細胞為載體的磁控細胞機器人(也稱巨噬細胞機器人)系統,並在小鼠體內驗證了對於幾種實體瘤的治療效果。
該系統包括進入體內的細胞機器人和控制機器人活動的磁操作平臺。細胞機器人(MCR)尺寸大約 20 微米,以具有天然吞噬活性的巨噬細胞作為載體。巨噬細胞透過內吞包裹著廣譜抗癌藥阿黴素(DOX)、PEG 和光敏材料吲哚菁綠(ICG)、磁響應介質 FeNPs 的磁性奈米顆粒(MNPs)將巨噬細胞轉變為磁控細胞機器人,然後巨噬細胞會與 MNP 共培養。
他們設計了一種級聯藥物釋放策略,具有磁性的細胞機器人會在體外磁控平臺的指引下透過血管轉運至腫瘤部位,並透過形變進入腫瘤內部。然後透過近紅外光照射,ICG 產生足夠熱量開啟磷脂雙分子層,脂質體破裂,DOX 從 MNP 中釋放,高濃度的 DOX 促使巨噬細胞破裂,藥物得以在腫瘤部位釋放。
“MCRs 的組成成分 FeNPs、DOX、ICG、PEG、脂質體均為 FDA 批准可用於臨床的材料,MCRs 的劑量、磁場梯度和近紅外光波長也在 FDA 規定的安全範圍內。” 馮林說。
接下來,在腫瘤小鼠模型中驗證磁控細胞機器人的靶向治療效果。試驗結果顯示,利用 808nm 波長的近紅外鐳射照射 8 分鐘後,服用細胞機器人的小鼠腫瘤部位出現明顯燒傷痕跡,且在接受治療第 3 天腫瘤體積變小,第 7 天腫瘤幾乎消除,腫瘤抑制率約為 91%。在 PTT 和近紅外照射刺激 MCR 釋放 DOX 的聯合治療下,腫瘤殺傷約為 97%。
“在這項研究中,我們提出了一個航空母艦攜帶艦載機遠端精準殺傷的策略,巨噬細胞就相當於航空母艦,裡面的奈米藥物相當於艦載機。在外場力指引下,幫助巨噬細胞到達腫瘤部位。到達腫瘤部位之後,透過遠紅外光照射,巨噬細胞裂解釋放藥物,利用磁場特性更加精準打擊腫瘤區域。” 馮林總結道。
除了小分子藥物,馮林告訴生輝,細胞機器人還可以遞送抗體類藥物,理論上可以遞送體積不超過 1 微米的藥物。
他還透露,下一步計劃克服血流阻力,加強對細胞機器人的精準、主動控制。
轉化工作正在有序推進
馮林實驗室圍繞微型機器人開展研究工作,主要以聲、光、電、熱、磁等物理場控方式為主。實驗室專案包括場控微奈米機器人靶向遞送系統、主動可控胃腸鏡膠囊機器人和微奈米級高通量光電鑷微作業系統等等。
在實驗室帶領課題組成員不斷迭代更新微型機器人系統的同時,馮林團隊也有志於將實驗室的專案轉化落地,真正推進研究成果應用於臨床。
馮林現在是蘇州吳中區的創新創業領軍人才,已經落地相關公司著手將實驗室的部分專案進行轉化。
據悉,該實驗室的膠囊機器人專案已經在蘇州落地轉化。據馮林介紹,該膠囊機器人在設計之初與臨床醫生溝通了臨床中的實際需求,以及現有膠囊機器人中存在的一些不足。
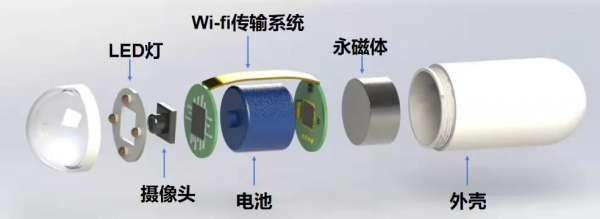
該實驗室研發的磁控膠囊機器人內部搭載永磁體,透過外部磁控系統控制其運動,實現膠囊的穩定懸浮。利用自由度平臺可以實現任意方向的直線運動,亥姆霍茲線圈系統實現轉動,耦合後,運動膠囊可以高精度控制無死角掃描。並基於 wifi 的影片傳輸方式,實時上傳拍攝畫面至雲端,有望降低膠囊機器人在胃腸道中的漏檢率。該專案曾獲得了全國網際網路 + 大賽金獎,北京市挑戰杯特別獎等。
(常見的膠囊機器人從入口起,即以 2 秒 / 張的速度拍照,歷經整個消化道,同時將影象實時傳送至患者口袋裡的記錄儀,從入口到排出體內可能會拍攝數萬張照片。)
另一項研究光電鑷微作業系統也已經在北京落地相關公司進行轉化。這是一套微奈米級別的光電鑷系統,可以在細胞裡面篩選和提純紅細胞、白細胞、血細胞、病毒和病菌以及精子等。目前,國際上的領跑者是納斯達克上市公司 Berkeley Lights, 該公司憑藉 “光電鑷子” 作業系統獲得了紅杉和尼康的加持,並拿到了安進、輝瑞、Ginkgo、Amyris 等大廠的訂單。
微奈米機器人系統是目前正在推進轉化的一項研究。據馮林介紹,上文提到的巨噬細胞機器人正在與北京同仁醫院對接,計劃針對肝癌和瀰漫大 B 細胞淋巴瘤開展臨床試驗。
不過他也強調,從 50 年代概念的提出到 90 年代真正得到發展,微奈米機器人的發展也只有 20 多年的時間,整體來看,微奈米機器人開展動物試驗已經是一大進步。如果要真正應用於臨床是一個系統工程,從動物試驗到人體試驗可能需要從頭設計作業系統,預計 3-5 年後才可能會進入人體試驗。
除了遞送給藥之外,微奈米機器人系統還可以應用於診斷,譬如說設計磁感應熒光探針在體內診斷。“診斷也是微奈米機器人系統極具落地潛力的場景。” 馮林補充道。
“微奈米機器人是高度交叉的學科,閉門造車行不通”
目前,微奈米機器人已廣泛應用於生物探測、智慧載藥、藥物釋放、血栓清除、祛除寄生蟲、殺死腫瘤細胞、啟用細胞能量、實現光熱治療等多個方面。
以靶向給藥為例,一款微奈米機器人從設計到落地給藥應用場景,其中會涉及到如何設計機器人、如何搭建控制系統、光熱材料選擇、如何透過化學修飾突破體內生物屏障,評估藥物在腫瘤部位如何發揮作用、效果等。
這一系列的問題涉及到多種學科,並非單一學科知識可以解答。“微奈米機器人學科是一個高度交叉的學科,其中涉及到工程學、自動化、細胞學、生物學、光電工程等多個方面。我認為,研究微奈米機器人的難點和關鍵點都在於學科交叉,多學科之間的交叉碰撞才能夠真正解決臨床的問題。” 馮林說。
談及微奈米機器人的技術壁壘,馮林也反覆強調了 ——“交叉學科”。據介紹,馮林在北航的課題組的成員學科背景多樣,既有生物學、化學、生物工程、臨床醫學背景,同時也有工程、計算機和機器人背景。馮林本人是機械自動化 + 電子資訊專業背景,主要負責機器人系統的控制系統搭建,生物和化學背景的成員則負責細胞培養、細胞膜表面修飾、機理分析等。
“也正是微奈米機器人的學科交叉特性,我認為未來微奈米機器人研究人員一定要走出自己的小圈子,多與臨床醫生、化學、分子生物學、分子影像等不同專業的研究人員交流,不能閉門造車,埋頭在自己的小圈子裡面死磕。不同的專業,思考問題的角度和方式差別會很大,多學科之間的交流會碰撞出不一樣的火花,這將是微奈米機器人未來的一大發展方向。” 馮林告訴生輝。
馮林坦言,完成上述提到的巨噬細胞機器人研究工作,就得益於多學科人才的通力合作。
此前,馮林團隊主導並獲得了科技部重點研發計劃 —— 靶向藥物輸送場控微納機器人基礎研究。據悉,該團隊的一個重要優勢就在於交叉學科研究團隊,團隊涵蓋了醫生、以及從事藥物化學、藥物注射分析、成像等不同學科背景的科研人員。