撰文 | 胡小話
心肌血運重建 (revascularization) 現已成為治療急性心肌梗塞的首先治療方案,但是,血運重建同樣會引起心肌的缺血再灌注 (ischemia-reperfusion, IR) 損傷進而導致額外的心肌細胞死亡和永久性的結構損傷。遺憾的是,目前還沒有針對IR損傷有效的干預手段。因此,減少血運重建引起的心臟損傷儘管是一個容易被忽視的治療目標,但在臨床上卻有著迫切的需求【1】。
2021年9月17日,來自武漢大學基礎醫學院的李紅良教授與其合作者們在Cell Metabolism上發表了題為Pharmacological inhibition of arachidonate 12-lipoxygenase ameliorates myocardial ischemia-reperfusion injury across multiple species 的研究文章,報道了花生四烯酸代謝通路中的代謝酶——ALOX12是干預IR損傷的一個潛在的藥物靶點,並且他們在高等動物模型中證實ALOX12的小分子抑制劑可以有效緩解心肌再灌注損傷。
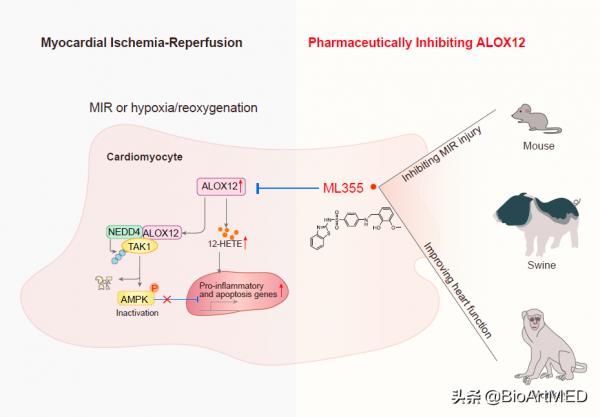
首先,透過對接受血運重建手術前後的心梗患者的血液樣本進行非靶標的代謝組學分析,作者發現花生四烯酸代謝途徑 (AA metabolism) 是被高度富集的,其中該通路中的關鍵代謝酶—ALOX12以及其代謝產物—12HTE的差異最為顯著。進一步,透過構建Alox12-KO小鼠,作者證明ALOX12是導致小鼠心肌再灌注損傷(MRI)的關鍵驅動因子。此外,小鼠實驗表明,Alox12特異的小分子抑制劑—ML355【2】可以有效保護小鼠心臟免受MRI損傷。但是,由於小鼠與人在生理與結構上具有較大的差異,因此以小鼠作為模式生物無疑會給後續的臨床轉化帶來很大的不確定性。基於這一考慮,作者在巴馬豬和恆河猴兩種高等動物上展開了更進一步的實驗驗證,結果顯示,ML355同樣可以起到保護模式動物心肌免受MRI損傷的作用。這些實驗結果共同表明:ALOX12可能是干預心肌MRI損傷的一個潛在的藥物靶點。
那麼,ALOX12介導心肌再灌注損傷的分子機制是什麼?為了回答這一問題,作者在WT、Alox12-KO (敲除) 和Alox12-CTg(過表達)小鼠接受再灌注手術的不同時間後收集小鼠的心臟樣本進行RNA-seq分析,他們發現AMPK訊號與Alox12敲除或過度表達呈現出最高的相關性。儘管AMPK與心臟保護作用密切相關,但其參與Alox12介導的訊號傳導卻尚未報道。有趣的是,作者發現發現ALXO12調控AMPK訊號並不依賴其代謝酶活性,證據有二:第一,ALXO12的代謝產物12HTE並不會影響AMPK訊號;第二,在Alox12-KD的細胞中回補ALXO12代謝酶活缺失的突變體ALOX12A403R可以完全恢復其對AMPK的調控能力。
為了找到ALXO12調控AMPK確切的分子機制,作者利用IP-MS分析了ALXO12的互作蛋白組,最終他們鑑定到調控AMPK磷酸化的上游激酶蛋白—TAK1 (TGF-β-activated kinase 1),此外,在ALOX2-TAK1複合體中他們還鑑定到多個泛素E3連線酶,這提示泛素化修飾可能參與調控ALOX2-TAK1-AMPK訊號。最終,他們篩選到泛素E3連線酶NED44會泛素化TAK1並介導TAK1的泛素化降解,而WT和酶活缺失的ALOX2都可以促進NED44與TAK1的相互作用。因此,這些實驗共同表明ALOX2會以非代謝酶活的方式促進NED44對TAK1的降解,進而降低AMPK的磷酸化。
長期以來,ALOX12作為一種脂氧合酶,一直被認為透過催化多不飽和脂肪酸生成過氧化產物來影響包括肥胖、動脈粥樣硬化、免疫疾病和腫瘤等疾病的發生發展【3】。但是在這項研究中,該研究團隊揭示了ALOX2會以一種非代謝活性的方式介導缺血再灌注引起的心肌損傷。並且他們在小鼠和更高等級的模式生物中證明,用小分子藥物抑制ALXO2的功能可以有效緩解模式動物的心肌再灌注損傷,這為今後的臨床轉化提供了很大的可能性。
本文來自BioArtMED微信公眾號,更多生物領域前沿資訊等你來發現!
轉載須知
【原創文章】BioArtMED原創文章,歡迎個人轉發分享,未經允許禁止轉載,所刊登的所有作品的著作權均為BioArtMED所擁有。BioArtMED保留所有法定權利,違者必究。