撰文 | 蕭平
腎細胞癌 (Renal cell carcinoma, RCC) 起源於腎上皮,約佔腎癌的85%。其病理學分型主要包括透明細胞癌 (ccRCC)、乳頭狀細胞癌 (pRCC) 以及嫌色細胞癌 (chRCC),其中透明細胞癌在臨床中最為常見。約四分之一的腎細胞癌患者表現為區域性浸潤性或轉移性腎細胞癌,後者的中位生存期約為13個月【1】。
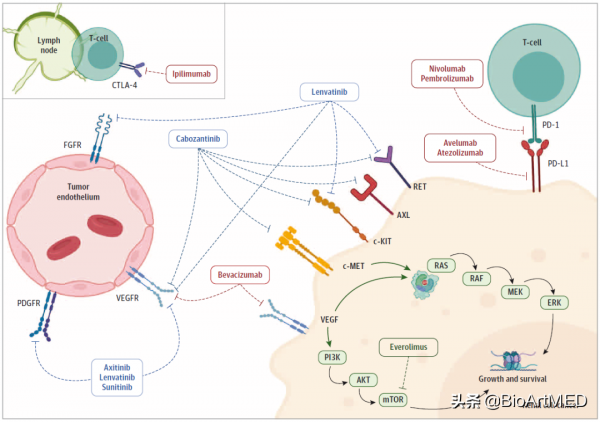
上世紀80年代後,免疫細胞因子干擾素α (IFNα) 和白介素2 (IL-2) 被應用於這一疾病的治療,但療效甚微且副作用明顯。隨著基因組學和分子生物學的快速發展以及癌症免疫應答過程機理的深入闡明,轉移性腎透明細胞癌 (mccRCC) 的預後有所改觀【2-3】。mccRCC患者大多攜帶VHL (von Hippel-Lindau) 基因突變,隨著研究者們對這背後分子生物學事件的探索,靶向血管內皮生長因子受體 (VEGFR) 的小分子受體酪氨酸激酶抑制劑 (TKIs) 在轉移性腎細胞癌治療中的地位被逐步確立【4】。但是,儘管抗血管新生治療在短期內療效顯著,客觀緩解率 (ORR) 和無進展生存期 (PFS) 都有所改善,但耐藥性的產生,導致這一治療無法長期保有效應,也難於提高患者長期生存。故而,提供持久藥物應答、提高患者生存率的新一線治療方法亟待建立。
近年來,免疫療法的臨床應用取得了顯著進展,其中最為重要的是免疫檢查點阻斷劑(ICB),它透過阻斷CTLA-4和PD-1等天然免疫調節分子來提高抗腫瘤免疫效應。根據CheckMate 025 3期臨床試驗結果,美國食品和藥物管理局(FDA)於2015年批准抗PD-1單克隆抗體Nivolumab用於既往接受過抗血管生成治療的晚期RCC患者。然而,目前的證據表明,並非所有患者都能從單一免疫治療中獲益【5】。證據顯示,聯合ICB和VEGFR靶向藥物,能夠進一步改善患者預後,但這一聯合治療的效果需要更為系統的評價和判斷。
近日,卡爾加里大學TomBaker癌症中心的Vishal Navani團隊在JAMA Oncology雜誌上發表題為Treatment selection in first-line metastatic renal cell carcinoma—the contemporary treatment paradigm in the age of combination therapy: a review的綜述文章。這一綜述總結了目前涉及到ICB/ICB聯合用藥或VEGFR + PD-1/PD-L1聯合治療轉移性腎細胞癌的臨床試驗結果,並對未來進行了展望。
該文章從治療效果、用藥選擇、未來展望三個方面,對聯合用藥在腎透明細胞癌治療中的應用進行了系統的梳理。
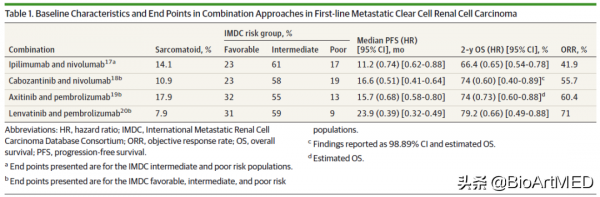
首先,文章總結了ICB/ICB聯合用藥以及ICB/VEGF聯合用藥的臨床試驗結果(表1)。CheckMate-214試驗採用Nivolumab和Ipilimumab聯合用藥後Nivolumab維持治療,結果顯示,同Sunitinib單獨用藥對比, 國際轉移性腎細胞癌聯合資料庫聯盟評分(IMDC評分)中高風險組聯合用藥效果更佳,而IMDC低風險組則更適於Sunitinib (PFS (12.4 vs 28.9 months, HR,1.84)、OS (median not reached in either arm; HR, 0.93))。在ICB/VEGF聯合用藥中,TKI的選用對於試驗結果影響較大。早期Sunitinib或者Pazopanib聯合ICB藥效持久,但毒副作用太過明顯。後期選用Axitinib或者Lenvatinib的臨床試驗結果,包括KEYNOTE-426試驗、CLEAR試驗等,均指向聯合用藥優於單獨用藥。KEYNOTE-426試驗的第一次中期評價中,選用TKI Axitinib聯合PD-1抑制劑Pembrolizumab呈現客觀緩解率 (ORR)、無進展生存期 (PFS) 以及總生存期(OS)的全面改善。
表1 轉移性腎透明細胞癌的臨床一線聯合用藥方案:基線特徵和臨床試驗終點概況
對於目前的臨床試驗結果,文章指出,患者基線水平、統計方法、隨訪時長、生物標誌物獲取途徑以及臨床試驗設計等諸多方面的差異讓交叉試驗困難重重。而不同試驗所採用評價指標的不同以及患者分層的模糊等,更進一步增加了交叉實驗的難點。早期評價指標,比如PFS和ORR,能較早得到藥物評價結果,利於藥物儘早獲批投入市場,隨即幫助癌症進展迅速的患者。而晚期評價指標,如OS、緩解持續時間 (DOR) 以及無治療生存期 (TFS),對於腫瘤控制情況的判斷可能更具有代表性,但收集這些資料成本高、速度慢。
此外,目前還沒有臨床試驗對不同聯合用藥方式進行直接比較,只能從目前試驗結果反映的資訊,選擇更為適合的聯合用藥方案。在這一部分,作者結合臨床試驗結果,分析了患者IMDC分級、共病情況、分子標記物、病理分型以及患者意願等諸多情況下的聯合用藥選擇。
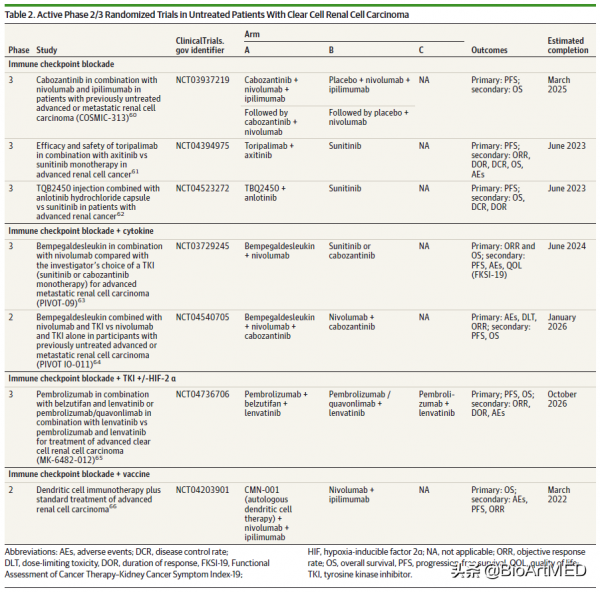
顯而易見,鑑於ICB/ICB以及VEGF/PD-1聯合治療所呈現的優勢,mccRCC一線治療方案的轉變指日可待。但值得注意的是,儘管存在細微差別,但總體而言,ICB/ICB和VEGF/PD-1 ICB治療在方案選擇、療效以及毒副作用上驚人地的相似。故而這其中,最為關鍵的是確定ICB/ICB或VEGF/PD-1 ICB治療方案,並找到最佳的用藥方案,以最大限度地減少毒副作用影響,保證患者的生活質量。顯然,目前尚在進行中的臨床試驗 (表2) 對這一問題並不關注。
此外,文章也對選擇性HIF2α靶向小分子藥物Belzutifan表示了關注。
作以總結,近年來,轉移性腎透明細胞癌在基因組學、分子生物學和免疫學水平的研究進展顯著提高了這一疾病的生存率。然而,關於這一致命性疾病,仍有許多工作要做。在未來,精準的預後評估、個性化的治療方案將進一步提高患者的生存率以及生活質量。
原文連結:
http://doi.org/10.1001/jamaoncol.2021.4337
製版人:十一
參考文獻
[1] Herbert T Cohen, Francis J McGovern. Renal-cell carcinoma. N Engl J Med . 2005;353(23): 2477-90.
[2] Cancer Genome Atlas Research Network. Comprehensive molecular characterization of clear cell renal cell carcinoma. Nature.2013;499(7456): 43-49.
[3] Chen DS, Mellman I. Oncology meets immunology: the cancer-immunity cycle. Immunity. 2013;39(1):1-10.
[4] Escudier B, Eisen T, Stadler WM, et al; TARGET Study Group. Sorafenib in advanced clear-cell renal-cell carcinoma. N Engl J Med.2007;356(2): 125-134.
[5] George S, Rini BI, Hammers HJ. Emerging Role of Combination Immunotherapy in the First-line Treatment of Advanced Renal Cell Carcinoma: A Review. JAMA Oncol. 2019;5(3):411-421.