歡迎關注凱萊英藥聞
近年來,受益於遞送技術突破,核酸藥物得到快速發展,以反義寡核苷酸藥物(ASO)、小干擾RNA(siRNA)等為代表的多款創新藥物進入市場,給脊髓性肌萎縮症、杜氏肌營養不良等適應症帶來了跨時代的臨床進展(詳見:RNA藥物市場概覽與已上市產品LNP技術差異分析 )。本文將重點介紹核酸適配體(Aptamer)和該技術在腫瘤治療領域內的前沿應用管線NOX-A12。
No.1 核酸適配體(Aptamer)
核酸適配體(Aptamer)是一種包含 20-80 個核苷酸的短RNA或單鏈DNA,可以摺疊成獨特的三維構象,特異性識別受體、抗原和生物標誌物等多種靶標並與之相互作用。與靶標結合後,適配體會誘導一系列生化效應,如拮抗、激動、抑制和破壞等。因其可透過化學手段合成,且具有優越的特異性、組織高滲透性、穩定性好、可重複修改等特性,被稱為“化學抗體”,並在臨床治療、診斷、成像等領域內有廣闊的應用前景。
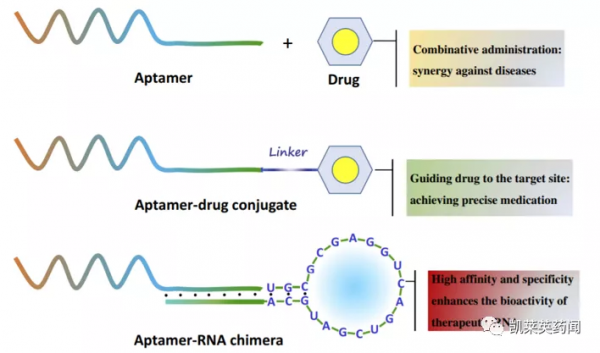
藥物的體內分佈對其藥理作用的有效發揮十分關鍵。為了避免給藥後藥物的彌散性生物分佈造成的較差治療效果和副作用,靶向藥物遞送系統 (TDDS)是目前最有希望的藥物遞送策略之一。基於其易於合成、高度特異性和可修飾潛力,適配體已被證明是出色的TDDS配體,並可以透過各種共軛方法靈活地錨定到各種奈米載體上(見下圖)。
此外,適配體還可透過組合給藥、適配體-藥物偶聯物、適配體-藥物嵌合體等三種形式協同增強對應藥物的治療效果(見下圖)。
目前,核酸適配體的藥物開發仍處於較為“冷門”的階段,全球僅有Pfizer和Bausch Health開發的pegaptanib獲批上市,用於治療新生血管性年齡相關性黃斑病變。除本文要重點介紹的NOX-A12外,僅有3款產品目前處於臨床II期階段。
No.2 NOX-A12
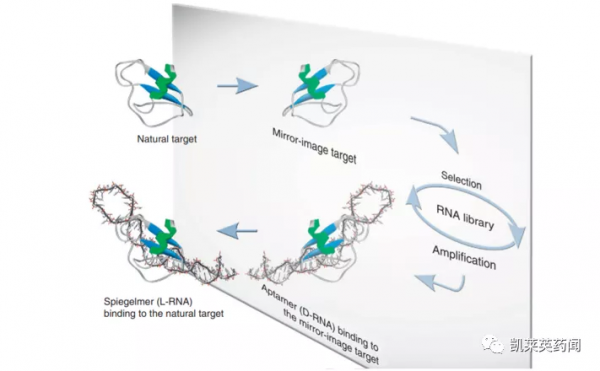
NOX-A12(olaptesed pegol)是由NOXXON Pharma開發的一款靶向基質細胞衍生因子-1(SDF-1,又稱趨化因子CXCL12)的聚乙二醇化的核酸適配體藥物。該藥物是利用NOXXON的專有技術Spiegelmers生產的化合物(L-立體異構體)。
該技術透過使用非天然L-核苷酸構建適配體,相較於傳統的D-核酸適配體,Spiegelmers不僅擁有高親和力和高特異性結合標靶的能力,還因其不能被普遍存在的血漿核酸酶識別而在血漿穩定性和抗核酸溶解(nucleolytic)方面有顯著優勢。
CXCL12
趨化因子是一大類低分子量蛋白質,可促進其靶細胞群的遷移和粘附。根據其功能,趨化因子可分為炎症趨化因子(inflammatory chemokines)和穩態趨化因子(homeostaticchemokines)。CXCL12屬於穩態趨化因子,其編碼基因位於染色體10q11,是唯一具有差異mRNA剪接的CXC趨化因子。
CXCL12透過與其受體CXC趨化因子受體4(CXCR4)和非典型趨化因子受體3(ACKR3)相互作用,在穩態和病理條件下發揮其功能。CXCR4 的啟用主要誘導G蛋白偶聯訊號轉傳導(見下圖)。
目前,NOX-A12被用於開發和放射性療法和免疫療法聯用治療胰腺癌等癌症。其在兩種療法中發揮雙重功能:(1)在放射性療法中,NOX-A12透過阻斷CXCL12可有效抑制放療後由HIF-1介導的血管生成,防治腫瘤組織的“修復”;(2)在免疫療法中,NOX-A12透過阻斷CXCL12改善腫瘤微環境,使抗癌免疫細胞(如殺傷性T細胞)進入腫瘤,從而發揮免疫腫瘤學方法(如免疫檢查點抑制劑)的治療能力。
No.3 臨床表現
聯合放療
2019年9月,一項介入性、序貫分配、單臂、劑量遞增、I/II期研究(NCT04121455)啟動,以評估NOX-A12聯合放療一線治療具有非甲基化MGMT啟動子的膠質母細胞瘤患者的安全性和有效性(n=9)。
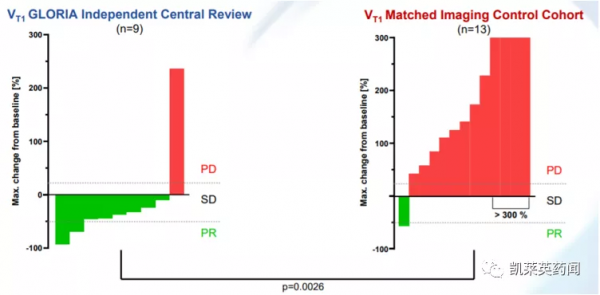
2021年11月,公司在SNO年會上釋出了該項試驗的最新資料。試驗結果顯示,接受 NOX-A12治療的9名患者中有8名 (89%) 實現了腫瘤體積的減小,其中2名患者達到PR,6名患者達到SD。而與之相對的,接受標準護理的匹配佇列的歷史患者結果顯示,僅有1名患者(8%)實現了腫瘤縮小的客觀反應。
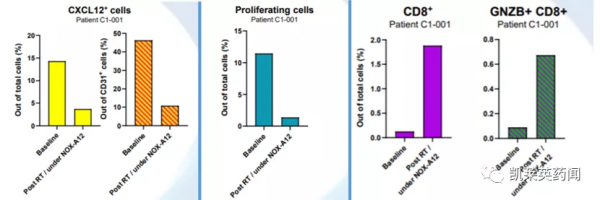
此外,來自接受NOX-A12治療的患者的組織分析資料顯示腫瘤血管內皮上的CXCL12顯著減少(下圖左),腫瘤細胞增殖受到抑制(下圖中),同時啟用的殺傷免疫細胞的腫瘤浸潤增加(下圖右)。
單藥及免疫治療聯用
2017年4月,公司啟動了一項針對轉移性結直腸癌和胰腺癌患者(n=20)的開放標籤、單組分配、兩部分的I/II期試驗(NCT03168139)。試驗第一部分為受試者在2周內接受NOX-A12單藥治療,以評估免疫浸潤變化、安全性和耐受性;第二部分為NOX-A12聯合K藥(pembrolizumab)治療以評估安全性、耐受性和療效。
在安全性方面,聯合用藥方案總體耐受性良好,共有162次不良事件(AE),其中45.7%為I級;37.1%為二級;16.4%三級;無 IV 級;0.7% 為V 級。免疫相關不良反應事件沒有超過K藥已知毒性特徵。
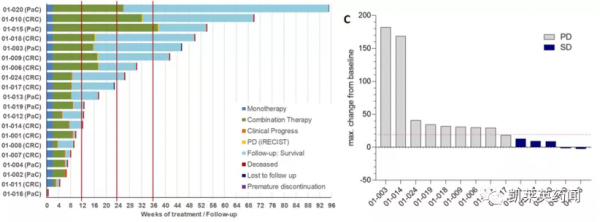
在療效方面,雖然在終末期患者中未觀察到客觀緩解,即部分緩解(PR)和完全緩解(CR)),但20名患者中仍有7名接受試驗治療6個月以上,觀察到聯合用藥治療後的疾病穩定(結直腸癌為27%,胰腺癌為22%)。
在一些未達到穩定疾病的患者中也看到了臨床益處,與他們最近一次治療相比,治療時間明顯增加。
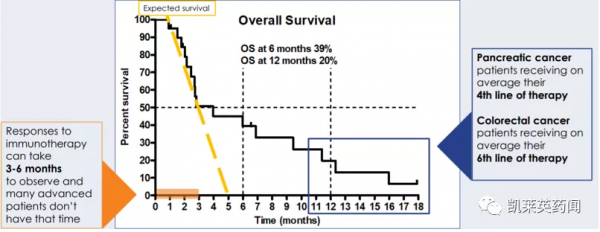
此外,對於本次試驗所納入的此前接受過多線治療的晚期腫瘤患者而言,聯合用藥後的總生存期比預期的要長。在存活超過3個月的10名患者中,80%存活超過24周,60%存活超過36周。據公司介紹,患者產生免疫治療應答可能需要3-6個月,許多晚期患者沒有足夠長的治療時間,從而削弱了免疫療法的臨床效果。而NOX-A12可以延長治療時間,使患者有機會對免疫療法產生應答。
目前,寡核苷酸藥物及相關技術,如遞送系統、修飾技術等,仍處於起步階段的快速發展期,大量實驗室中的技術與發現尚待有效的開發與利用。期待寡核苷酸藥物領域內可以出現製藥界的“新王者”。
參考資料
1. Aptamers as Versatile Ligands for Biomedical and Pharmaceutical Applications. Int J Nanomedicine. 2020 Feb
2. Turning mirror-image oligonucleotides into drugs: the evolution of Spiegelmer() therapeutics. Drug Discov Today. 2015 Jan
3. The unique structural and functional features of CXCL12. Cell Mol Immunol. 2018 Apr
4. Combined inhibition of CXCL12 and PD-1 in MSS colorectal and pancreatic cancer: modulation of the microenvironment and clinical effects. J Immunother Cancer. 2021 Oct
5. CXCL12 inhibition in MGMT unmethylated glioblastoma – Results of an early proof-of-concept assessment in the multicentric phase I/II GLORIA trial (NCT04121455)
6. 公司公告