瑞帕妥單抗(SCT400)是中國自主研發的一種人鼠嵌合IgG1型抗CD20單克隆抗體,恆定區序列選用中國人血細胞提取的最常見天然 IgG1同種異型G1m(1,17),與利妥昔單抗重鏈氨基酸在CH1區第219位的氨基酸(V219A)存在差異,即瑞帕妥單抗為纈氨酸,而利妥昔單抗為丙氨酸。
在2021年第63屆美國血液年會(ASH)召開之際,瑞帕妥單抗也以壁報的形式正式公佈了其Ⅲ期臨床研究資料,評價瑞帕妥單抗聯合CHOP對比利妥昔單抗聯合CHOP治療初治瀰漫性大 B 細胞淋巴瘤(DLBCL)的有效性及安全性。
壁報2480:重組人鼠嵌合抗CD20單克隆抗體(瑞帕妥單抗)聯合CHOP方案治療初治瀰漫性大B細胞淋巴瘤患者的有效性和安全性:一項多中心、隨機、單盲、陽性對照Ⅲ期臨床試驗
研究方法
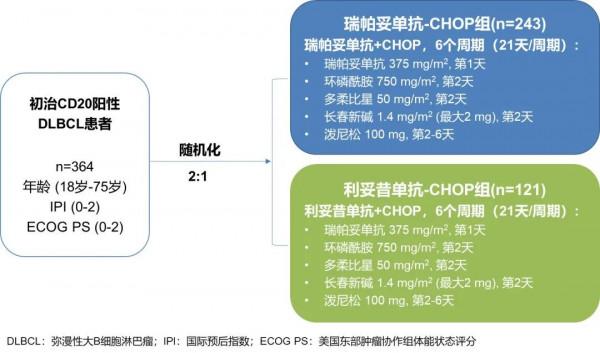
本研究為多中心、隨機、受試者設盲、陽性對照的Ⅲ期臨床試驗,試驗設計見圖1。
主要終點:接受研究藥物6個週期後,獨立影像學評估的客觀緩解率(ORR)。
次要終點:獨立影像學評估的完全緩解率(CRR)、無進展生存期(PFS)、總生存期(OS)、安全性。
本研究採用非劣效設計,主要終點非劣效界值取為-12%。
研究結果
基線
研究從中國37家中心篩選了534例患者,最終納入364例初治DLBCL患者,其中瑞帕妥單抗-CHOP組243例患者,利妥昔單抗-CHOP組121例患者,兩組基線人口學及病理特徵均衡,差異無統計學意義(P>0.05)。
療效
在符合方案分析集(PPS)人群中,瑞帕妥單抗-CHOP組與利妥昔單抗-CHOP組的ORR分別為94.5%和94.1%,兩組間差異無統計學意義(P=0.6569),兩組間ORR率差(瑞帕妥單抗-CHOP組-利妥昔單抗-CHOP組)為0.4%(95%CI: -4.7%~5.6%),非劣效性成立(圖2)。在全分析集(FAS)人群中,主要研究終點ORR的分析結果與PPS人群中相似。
圖2:PPS人群中客觀緩解率(ORR)和完全緩解率(CRR)
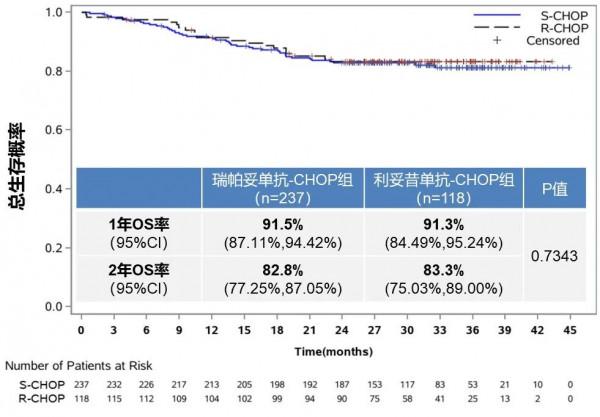
在PPS人群中,瑞帕妥單抗-CHOP組與利妥昔單抗-CHOP組CRR(70.5% vs. 75.4%, P=0.7084)、1年PFS率(81.3% vs. 82.8%, P=0.9320)和2 年OS率(82.8% vs. 83.3%, P=0.7343)差異均無統計學意義(圖2,圖3,圖4)。在FAS人群中,次要研究終點CRR、PFS、OS的分析結果與PPS人群中相似。
圖3:PPS人群中無進展生存曲線圖
安全性
總體不良事件(AE)發生情況見圖5。瑞帕妥單抗-CHOP組與利妥昔單抗-CHOP組總體AE發生率、嚴重程度≥3級的AE發生率、嚴重不良事件(SAE)發生率、導致停藥的AE發生率、導致死亡的AE 發生率,差異均無統計學意義(P>0.05)(圖5)。
圖5:總體不良事件發生情況
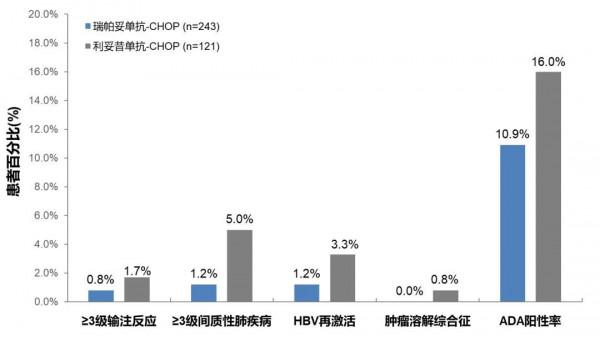
部分臨床關注的不良反應發生率見圖6。其中,≥3級輸注反應(0.8% vs. 1.7%)、≥3級間質性肺疾病(1.2% vs. 5.0%)、乙型肝炎病毒(HBV)啟用(1.2% vs. 3.3%)、腫瘤溶解綜合徵(0.0% vs. 0.8%)的發生率瑞帕妥單抗-CHOP組表現出一定優勢。(圖6)。
免疫原性:治療後與研究藥物相關的抗藥性抗體(ADA)陽性率瑞帕妥單抗-CHOP組與利妥昔單抗-CHOP組分別為10.9%和16.0%(圖6)。
研究結論
對於CD20陽性的初治DLBCL患者,瑞帕妥單抗聯合CHOP方案療效非劣於利妥昔單抗聯合CHOP方案。兩組整體安全性相當,未發現新的與治療相關的不良事件。在部分臨床關注的不良事件和免疫原性方面,瑞帕妥單抗表現出一定優勢,但需臨床進一步驗證。瑞帕妥單抗聯合CHOP方案可以作為DLBCL患者治療的選擇。
參考來源:https://ash.confex.com/ash/2021/webprogram/Paper149861.html