11月12日,國家藥監局官網顯示,西安楊森達雷妥尤單抗(daratumumab)注射液第3項適應症上市申請獲NMPA批准。
達雷妥尤單抗是全球及國內首個獲批的靶向CD38的全人源單克隆抗體,2019年7月,達雷妥尤單抗作為國內首個獲批的靶向作用於CD38的全人源單克隆抗體,獲NMPA附條件批准用於單藥治療復發和難治性多發性骨髓瘤成年患者,患者既往接受過包括蛋白酶體抑制劑和免疫調節劑的治療且最後一次治療時出現疾病進展,商品名為兆珂。
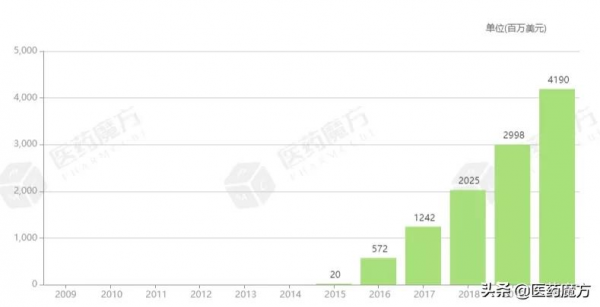
今年4月底,達雷妥尤單抗第2項適應症獲批,與來那度胺和地塞米松聯合用藥或與硼替佐米和地塞米松聯合用藥治療既往至少接受過一線治療的多發性骨髓瘤成年患者。在國外,達雷妥尤單抗適應症已覆蓋多發性骨髓瘤1~4線用藥,已經成為臨床基石療法。作為強生重磅產品,達雷妥尤單抗在2019年的全球銷售額達到29.98億美元,2020年銷售額達到41.90億美元,同比增長39.8%。
此外,10月11日,雷妥尤單抗皮下注射液獲NMPA批准上市,商品名為兆珂速。透過與硼替佐米、環磷醯胺和地塞米松聯合用藥治療新診斷的原發性輕鏈型澱粉樣變患者。該產品是全球首個且目前唯一獲批治療系統性輕鏈型澱粉樣變患者的創新解決方案。
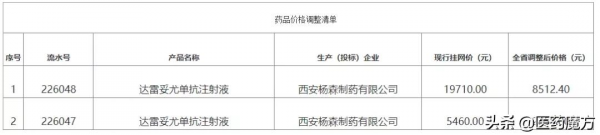
7月27日,遼寧省藥品和醫用耗材集中採購平臺釋出了達雷妥尤單抗注射液的主動降價通知。達雷妥尤單抗注射液100mg/5ml規格從5460元降為2358元,400mg/20ml規格從19710元降為8512.4元,降幅達到56.81%。
去年,達雷妥尤單抗注射液醫保談判失敗。今年醫保談判已結束,達雷妥尤單抗注射液是否談判成功,我們一起等待答案揭曉。