編者按:2021年12月11日~14日,備受矚目的第63屆美國血液學會年會(ASH)在美國亞特蘭大的Georgia世界會議中心隆重召開, 作為全球規模最大、涵蓋內容最為全面的血液學領域學術會議,今年ASH大會報道了諸多的重磅研究。在CAR-T治療方面,ZUMA-7研究的3期結果更新了,比較了抗CD19 CAR-T Axicabtagene Cilouleucel (Axi-Cel)與標準治療方案(SOC)在復發或難治性大B細胞淋巴瘤(R/R-LBCL)患者中的療效差異。針對該話題,《腫瘤瞭望》特邀採訪了復旦大學附屬腫瘤醫院曹軍寧教授,全面解讀了ZUMA-7研究。
● Primary Analysis of ZUMA‑7: A Phase 3 Randomized Trial of Axicabtagene Ciloleucel (Axi-Cel) Versus Standard‑of‑Care Therapy in Patients with Relapsed/Refractory Large B-Cell Lymphoma
● ZUMA-7研究:Axicabtagene Cilouleucel (Axi-Cel) vs標準療法(SOC)在復發/難治性大B細胞淋巴瘤患者中的3期隨機試驗
研究簡介
共入組359例復發或難治性大B細胞淋巴瘤(R/R-LBCL)成人患者, ECOG PS評分為0~1分,中位年齡59歲,1:1隨機分配至axi-cel組或標準治療(SOC)組進行治療,其中axi-cel組在預處理化療後接受2×106/L的CAR-T細胞輸注; 而SOC組則接受2~3個週期、R/R-LBCL治療指南中推薦的以鉑類為基礎的化療方案. 主要的研究終點為無事件生存(EFS),關鍵指標包括客觀緩解率(ORR)及總體生存(OS),安全性為次要指標。
中位隨訪24.9個月,結果顯示:①axi-cel組的客觀緩解率(ORR)顯著高於SOC組,分別為83% vs 50%(OR=5.31,95% CI: 3.1–8.9; P<.0001),完全緩解率(CR)則分別為65% vs 32%, 見圖1。
②axi-cel組的中位EFS明顯要優於SOC組,分別為8.3個月vs 2個月; 2年EFS則分別為41%(axi-cel組) vs 16%(SOC組), 詳見圖2。
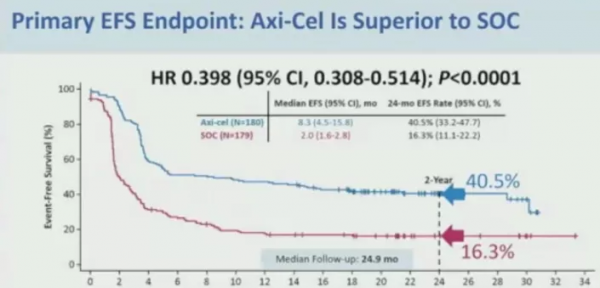
圖2:axi-cel組的中位EFS及2年EFS均優於SOC組
③在總體生存(OS)方面,axi-cel組患者的中位OS尚未達到(NR), SOC組中位OS為35.1個月(HR: 0.730; P=.027), axi-cel組更佳, 詳見圖3。
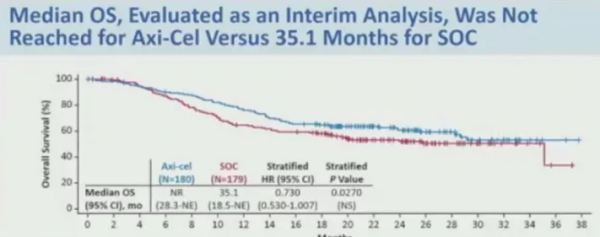
圖3:axi-cel組的中位OS尚未達到,soc組為35.1個月
④安全性方面,≥3級治療相關不良反應(AEs)在兩組患者中相當,分別為91%(axi-cel組) vs 83%(soc組),治療相關死亡病例分別為1例(axi-cel組)和2例(soc組); 此外,axi-cel組≥3級的細胞因子釋放綜合徵(CRS)發生率為6%; ≥3級的神經學毒性事件(NEs)為21%。
綜上,ZUMA-7研究表明,較之於標準治療方案(SOC), 抗CD19 CAR-T藥品axi-cel能使復發或難治性大B細胞淋巴瘤(R/R-LBCL)的緩解率、EFS及OS成倍的提升,要明顯優於標準治療方案(SOC),且安全性尚可靠。
曹軍寧教授點評
在今年的ASH會議上,ZUMA-7研究3期結果的更新引起了較多的關注. 對於一線治療後復發或難治的DLBCL患者而言,目前的標準治療是二線挽救化療+自體造血幹細胞移植(ASCT),然而僅有部分R/R-DLBCL患者在上述二線治療後能夠達到完全緩解或部分緩解(CR/PR),較多R/R-DLBCL患者可能已經化療耐藥、不適合接受移植或無法耐受強烈化療,故此類患者的預後是非常差的。
抗CD19 CAR-T細胞Axi-Cel(阿基侖賽)已經被批准用於二線及二線以上治療後失敗的DLBCL,在國內也已經上市。ZUMA-7研究是一項全球多中心、隨機對照的III期臨床試驗,入組的患者均為充分一線治療後1年內復發或難治、後續計劃接受自體移植的DLBCL患者, 1:1隨機接受Axi-Cel或含鉑挽救化療+ASCT(即標準治療組,SOC),主要研究終點包括EFS。經過2年左右的中位隨訪,這項研究達到了主要研究終點EFS,Axi-Cel組的中位EFS明顯優於標準治療組,分別是8.3個月和2個月(HR= 0.398; P<.0001), Axi-Cel組的總體緩解率和完全緩解率較之於SOC組增加了1倍之多,具有明顯優勢。此外,作為預設的中期分析指標,該研究對OS也進行了比較,中位OS在Axi-Cel組尚未達到,而標準治療組為35.1個月(HR= 0.730; P=.027),但需要指出的是,標準治療組中有56%患者在退出研究後接受了商業化CAR-T細胞治療,對OS的分析會有明顯的影響。最後,在安全性方面, Axi-Cel治療的安全性與既往的研究比較一致, 未發生致死性的CRS或神經學毒性,絕對的治療相關死亡率分別為1%和3%。
總結而言,ZUMA-7研究針對的是一線治療後短期(12個月內)復發或難治的DLBCL患者,此類患者存在耐藥、無法耐受強烈化療或不適合接受自體移植等諸多問題,治療上非常棘手,在ZUMA-7研究的標準治療組中也證實了無法接受移植的最主要原因是疾病進展,對於此類治療棘手、預後差的R/R-DLBCL患者,Axi-Cel治療取得了緩解率(ORR/CR)和無事件生存率(EFS)的顯著改善且安全性可控,是個值得期待的新療法。最後,需要我們思考的一個問題是:
對於一線治療失敗的DLBCL,CAR-T細胞治療是否能夠成為替代現有治療手段的新標準?我們非常期待延長隨訪時間後的進一步資料更新。
復旦大學附屬腫瘤醫院
腫瘤內科淋巴瘤專科副主任
淋巴瘤多學科副首席專家
上海市抗癌協會淋巴瘤專業委員會 主任委員
中國抗癌協會淋巴瘤專業委員會 常務委員
中國臨床腫瘤學會抗淋巴瘤聯盟 常務委員
中國臨床腫瘤學會 理事
中國抗癌協會腫瘤臨床化療專業委員會 委員
中華醫學會腫瘤學分會淋巴血液學組 委員
中國藥學會抗腫瘤藥物專業委員會 委員
中國醫療保健國際交流促進會腫瘤內科分會 副主任委員
中國老年保健協會淋巴瘤專業委員會 副主任委員
國家食品藥品監督總局仿製藥質量和療效一致性評價專家委員會 委員

















