本文來自微信公眾號:X-MOLNews
三氟甲基碳氟鍵(C-F)是有機合成化學中廣為人知的高鍵能化學鍵,其斷裂官能化可以直接合成多種常規方法難以製備的、且具有重要合成價值的部分氟代有機分子。這種快速構建高值含氟結構單元的策略也促使了眾多化學家投身於三氟甲基的碳氟鍵官能化反應研究中。其中,將三氟甲基C-F鍵選擇性還原為C-H鍵(即脫氟氫化,HDF)尤為引人注目,該方法在藥物和天然產物分子編輯中具有非常吸引人的應用前景。此類策略的開發允許對目標分子進行精準的原子替換,這對於篩選候選藥物分子的生物活性以及藥代動力學具有重要意義。然而,目前已知的方法均受限於三氟甲基芳烴和烯烴分子,同時,C-F鍵的鍵解離能(BDE)隨著脫氟的發生而逐漸降低,過還原產物的形成也一直是該領域中難以解決的問題。在此背景下,開發新型三氟甲基化合物的選擇性脫氟氫化反應,並突破芳烴和烯烴分子的限制是推動該領域發展的重要途徑。
圖1. 基於卡賓策略的漸進式脫氟氫化反應
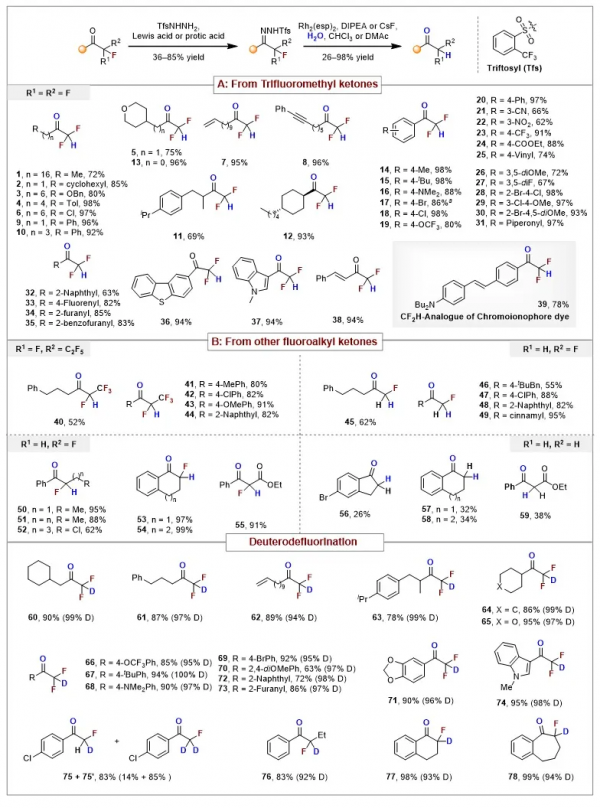
近日,東北師範大學畢錫和課題組開發了一種基於卡賓策略的漸進式脫氟氫化反應,成功實現了多樣化氟烷基酮的選擇性脫氟氫化。該策略的開發提供了一種更為便捷且直接的方法來獲取多種部分氟代的酮類化合物。
圖2. 氟烷基酮的脫氟氫化/氘化
該反應以鄰三氟甲基苯磺醯腙作為氟烷基重氮前體,在銠催化劑和水的存在下即可實現一鍋法的脫氟氫化反應。該反應的底物適用範圍廣泛,烷基和芳基取代的磺醯腙均能以非常優秀的產率得到目標產物。其中,烷基磺醯腙並未發生傳統的Bamford-Stevens反應,即β-H消除反應(如圖2所示),展示了該催化體系的高選擇性。眾多常見官能團如:烷氧基、鹵素、氨基、三氟甲基、三氟甲氧基、酯基、硝基等均能非常好的容忍。此外,多種多取代、稠芳環以及雜芳環底物也都順利進行該反應。含有生物活性分子片段的底物同樣能夠得到較好的收率,這也進一步表明了該方法良好的相容性。
圖3. 生物活性分子的逐級脫氟氫化/氘化
另外,對於其他多氟烷基、二氟烷基、甚至單氟烷基酮類化合物也都可以順利進行這種選擇性的脫氟氫化反應,成功合成了眾多部分氟代的酮類衍生,為此類化合物的製備提供了更為便捷且直接的方法。將水替換為氘代水後,脫氟氘代反應同樣反應良好,且氘代率極高。隨後,作者將該策略應用於生物活性分子的逐級脫氟氫化反應中,進一步驗證了該方法在藥物分子精準修飾中的應用潛力(圖3)。
圖4. 理論計算
最後,作者透過理論計算對反應機理進行了研究(圖4)。DFT計算表明銠卡賓中間體可以經歷水的親核進攻以及β-H遷移兩種路徑,但其經歷β-H遷移形成Z式和E式的三氟甲基烯烴產物需要相對較高的活化自由能,因此該競爭反應是能量不利的。另一方面,水對銠卡賓中間體進行親核進攻,得到活性中間體氧鎓葉立德。該中間體經由五元環過渡態進行了氟化氫脫除,並進行雙水分子協助的烯醇互變得到最終產物。
該研究成果發表在Angewandte Chemie International Edition 上,並被編輯遴選為“Hot Paper”。東北師範大學博士研究生張曉龍和博士研究生張欣宇為共同第一作者,理論計算部分由博士生宋清敏完成,通訊作者為畢錫和教授。該研究工作得到了國家自然科學基金的大力支援。
A Carbene Strategy for Progressive (Deutero)Hydrodefluorination of Fluoroalkyl Ketones
Xiaolong Zhang, Xinyu Zhang, Qingmin Song, Paramasivam Sivaguru, Zikun Wang, Giuseppe Zanoni, Xihe Bi*
Angew. Chem. Int. Ed., 2021, DOI: 10.1002/anie.202116190
導師介紹
畢錫和
https://www.x-mol.com/university/faculty/9495