2021年7月《柳葉刀》上發表了一篇有關Ib/II期CARTITUDE-1試驗的隨訪分析結果。CARTITUDE-1是一項在美國和日本開展的註冊臨床研究(編號為NCT03548207),旨在評估cilta-cel治療復發/難治性多發性骨髓瘤(RRMM)患者的安全性和有效性。接下來我們一起來看一下這項研究的隨訪分析結果。
MM患者接受免疫調節劑、蛋白酶體抑制劑和抗CD38抗體治療後,最終復發或耐藥,導致不良預後。目前,MM患者對新療法的需求尚未得到滿足。Ciltacabtagene autotoleucel(也被稱為cilta-cel)是一種CAR-T細胞療法,其設計的CAR-T細胞上表達兩個靶向BCMA的單域抗體,一個帶有4-1BB共刺激域的CD3-ζ訊號域,以最佳化T細胞的啟用和增殖。
研究方法
研究設計和受試者
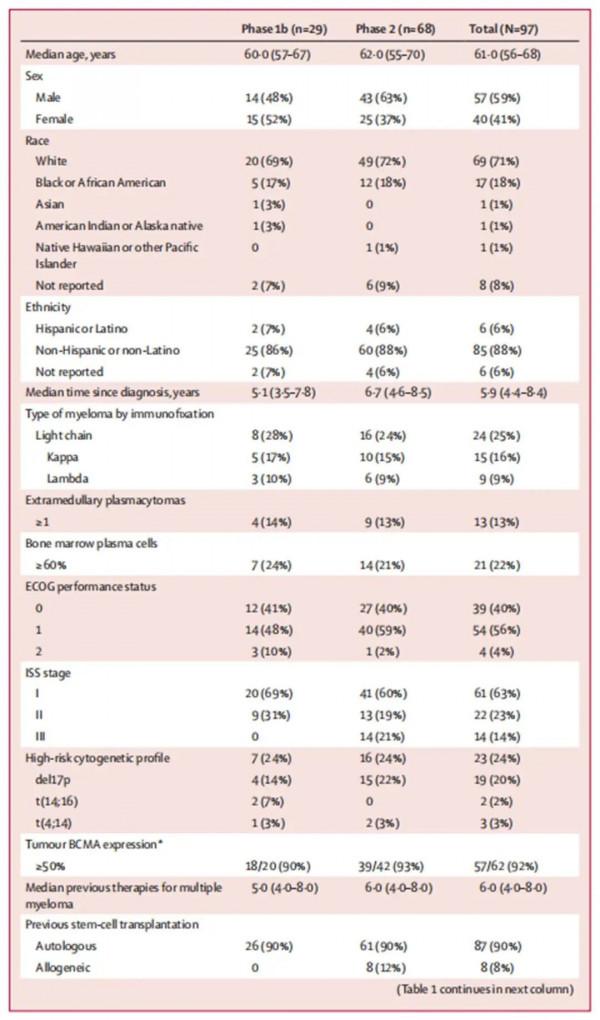
在這項單臂、開放標籤、Ib/II期研究中,納入了來自美國16箇中心、年齡≥18歲、符合IMWG診斷標準以及具有測量病灶的RRMM患者。受試者需同時滿足:①ECOG評分≤1;②既往接受過至少3線骨髓瘤治療或者對蛋白酶體抑制劑和免疫調節劑雙重耐藥;③接受過抗CD38抗體治療。排除既往接受過CAR-T細胞靶向治療或BCMA靶向治療的患者。另一個佇列研究正在日本進行。Ib期試驗研究目的是評估cilta-cel治療的安全性和II期試驗研究的推薦劑量; II期試驗的主要目的是評估cilta-cel的療效。患者的基線資料列於表1。
根據要求對患者進行血液單採,完成血液單採後允許接受接橋治療。Cilta-cel是透過將表達抗BCMA-CAR的慢病毒載體(包括兩個BCMA結合域,一個CD3-ζ訊號域,一個4-1BB共刺激域)轉匯入T細胞製備而成,隨後進行T細胞擴增。
Cilta-cel製備成功後,患者先接受3日靜脈輸注300 mg/m²環磷醯胺和30 mg/m²氟達拉濱進行淋巴清掃,在開始進行淋巴清掃5-7天后,接受cilta-cel輸注(目標劑量:0.75×106活的CAR陽性T細胞/kg[範圍:0.5-1.0×106/kg])。Ib期試驗的主要研究終點是不良事件的發生率和嚴重程度。II期試驗的主要研究終點是總體緩解率(ORR)。Ib期試驗和II期試驗的次要終點包括嚴格意義的完全緩解率(sCR)、完全緩解率(CR)和非常好的部分緩解率(VGPR); 緩解時間; 微小殘留病灶(MRD)陰性率; 無進展生存期(PFS); 總生存期(OS); 以及藥代動力學和藥效學標誌物。
研究結果
在2018年7月16日至2019年10月7日期間,該研究共納入113名患者,所有患者均進行了單採(圖1)。16名(14%)患者由於疾病進展、死亡或退出研究而未接受cilta-cel治療。
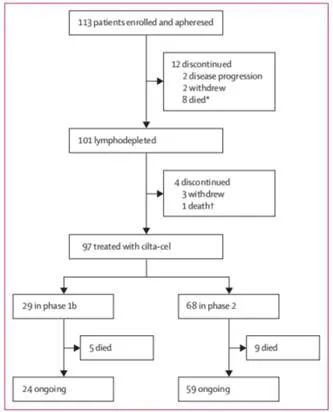
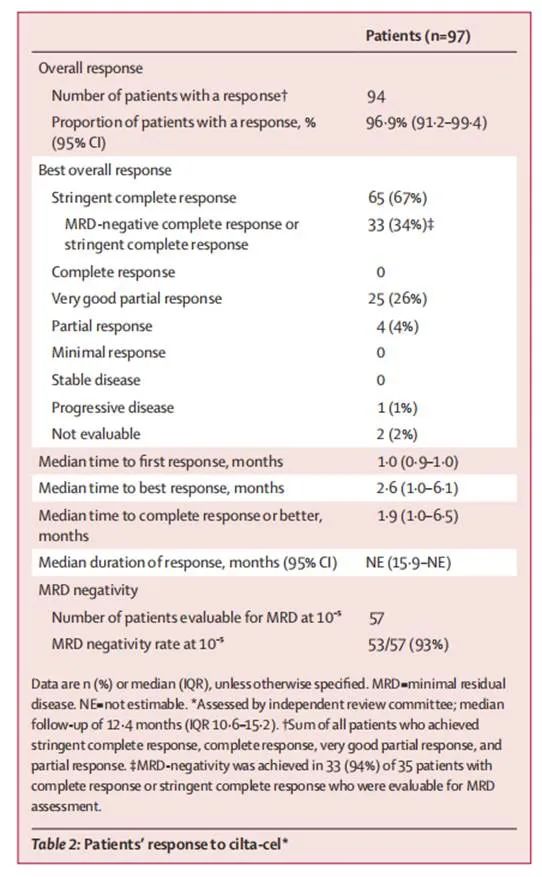
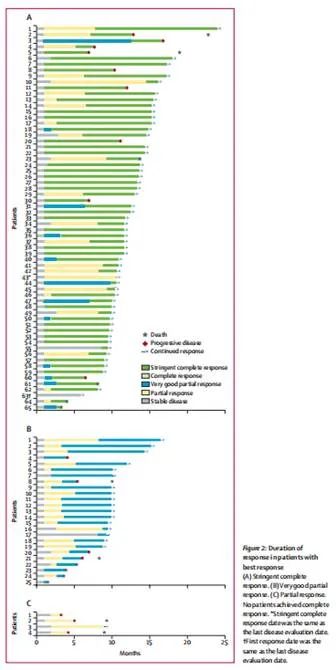
中位隨訪12.4個月(IQR 10.6-15.2),ORR為97% (95% CI 91.2-99.4),65例(67%)患者達到嚴格意義的完全緩解(表2)。首次緩解中位時間為1.0個月(IQR 0 9-1.0),94例得到緩解患者中有74例(79%)是在輸注cilta-cel後1.0個月內出現第一次緩解。最佳緩解中位時間為2.6個月(1.0-6.1)。完全或更好緩解中位時間為1.9個月(1.0-6.5); 65例達到完全或更好緩解患者中,有40例(62%)患者在輸注cilta-cel 3個月內達到完全或更好緩解。隨著時間的推移,97例緩解患者中有70例(72%)患者的緩解仍在持續,並不斷加深(圖2)。中位緩解持續時間(DOR)未達到(95% CI 15.9-不可估計)。
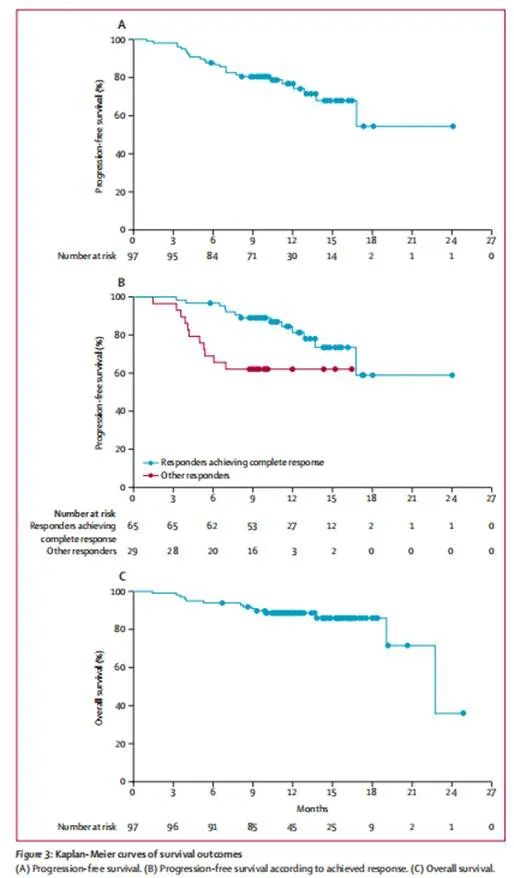
中位PFS未達到(95% CI 16.8-不可估計)(圖3); 12個月PFS率為77% (95% CI 66.0-84.3)。達到完全或更好緩解患者的12個月PFS率為85%(72.0-91.8),達到非常好的部分緩解或部分緩解患者的12個月PFS率為62%(42.1-76.9),兩組的中位PFS均未達到(95% CI分別為16.8-不可估計和5.4-不可估計; 圖3)。12個月OS率為89%(80.2-93.5;圖3)。
57例可評估MRD的患者中,53例(93%)達到MRD陰性。65例達到嚴格意義的完全緩解患者中,35例(54%)可進行MRD評估,其中33例(94%)達到MRD陰性。達到MRD陰性的中位時間為1.0(IQR 0.9–1.0)個月。
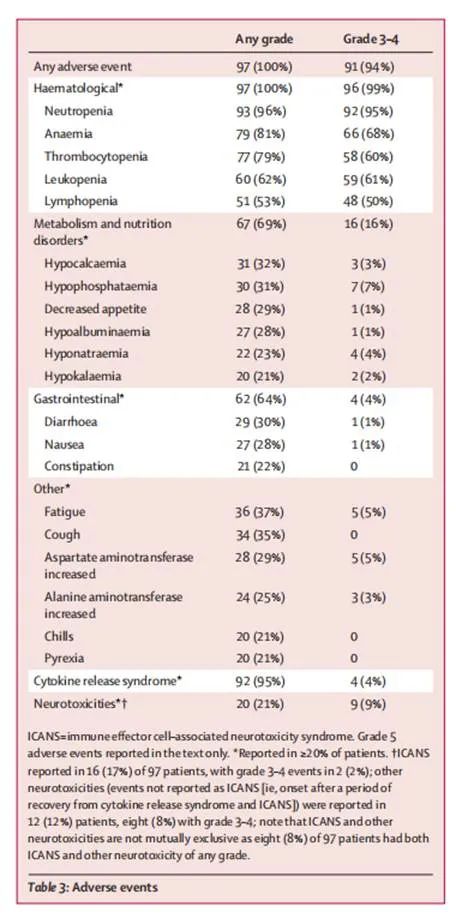
所有97例患者均有不良事件發生,包括3-4級事件(表3)。血液學不良事件最為常見;3-4級血液學不良事件為中性粒細胞減少(92例[95%])、貧血(66例[68%])、白細胞減少(59例[61%])、血小板減少(58例[60%])和淋巴細胞減少(48例[50%])。
這篇對Ib/II期CARTITUDE-1研究的隨訪分析結果為單次低劑量注射cilta-cel建立了一個積極的風險-收益分析資料,cilta-cel可對既往治療過的多發性骨髓瘤患者產生快速、深度和持久的緩解。有關cilta-cel對其他早期多發性骨髓瘤患者的研究正在進行中。
參考文獻
1.Berdeja JG, et al. Ciltacabtagene autoleucel, a B-cell maturation antigen-directed chimeric antigen receptor T-cell therapy in patients with relapsed or refractory multiple myeloma (CARTITUDE-1): a phase 1b/2 open-label study. Lancet. 2021 Jul 24;398(10297):314-324.