12月24日,北恆生物宣佈,其自主研發的CTA101 UCAR-T(通用型CAR-T)細胞注射液產品新藥臨床試驗申請獲CDE受理(受理號:CXSL2101509)。這是國內首個基於CRISPR基因編輯技術的免疫細胞治療產品,也是國內首個“現貨型”異體來源的CAR-T創新藥,屬治療用生物製品1類新藥。
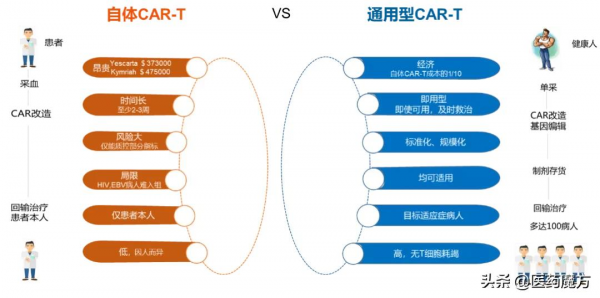
UCAR-T是使用健康人的T細胞製備完成,相比自體CAR-T,UCAR-T具有抗腫瘤活性高、成本低和可及性高等優勢。通用型免疫細胞治療無需配型,“現貨"儲存,即時使用,顯著降低病人治療週期,一位健康捐獻者可製備成百上千人份“現貨”,可顯著降低細胞治療成本。
CTA101是一款雙靶點UCAR-T細胞注射液,針對CD19和/或CD22陽性成人復發/難治急性淋巴白血病。該產品採用北恆生物第一代UCAR-T平臺,結合CRISPR基因編輯技術,敲除TRAC基因以避免移植物抗宿主病(GvHD),同時敲除CD52基因並聯合使用抗CD52單抗避免患者對CAR-T細胞的排異反應(HvG),延長UCAR-T細胞的體記憶體續時間。2021年4月,CTA101探索性臨床研究(IIT)結果在Clinical Cancer Research 原著論文形式發表,初步資料顯示,CTA101安全性及有效性良好。