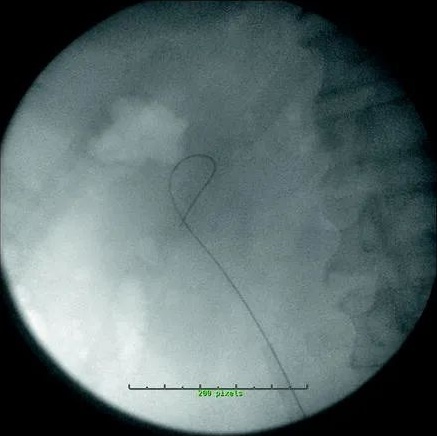
輸尿管軟鏡終於有了用武之地!這主要是因為有了通路鞘 (UAS)!
Abstract
輸尿管軟鏡檢查已成為泌尿科醫生診斷和治療包括腎結石和尿路上皮細胞癌在內的上尿路病理學的越來越重要的工具。輸尿管通路鞘 (UAS) 的發展透過為外科醫生提供低壓、視覺清晰的手術環境,有助於採用輸尿管軟鏡檢查。本章重點介紹了 UAS 在輸尿管軟鏡檢查期間提供的好處,並討論了一些對它們的使用的擔憂。討論了不同護套的特性,以及正確使用和放置的技術。討論了使用 UAS 擴大輸尿管軟鏡檢查的適應症以及使用後的退出策略。
Introduction
在過去十年中,輸尿管軟鏡在治療上尿路腎結石和腫瘤方面的作用不斷擴大。這是由於輸尿管軟鏡設計的改進、儀器的小型化以及作為體內碎石術黃金標準的鈥:YAG 鐳射器的發展。輸尿管通路鞘 (UAS) 的發展有助於進一步推進輸尿管軟鏡檢查。Takayasu 和 Aso 於 1974 年首次描述了 UAS 的使用 。從那時起,它已被證明是一種經濟高效的工具,可以安全有效地重新進入輸尿管和集合系統,同時改善視野、降低腎內壓力並提供更好的患者預後 。
使用 UAS 有幾個優點
與不使用 UAS 時相比,在輸尿管軟鏡檢查中使用 UAS 有幾個優點(表 24.1)。當 UAS 處於適當位置時,由於沖洗液透過輸尿管鏡通道連續流入並透過 UAS 流出,從而改善了腎臟中的沖洗流量。在鐳射碎石術或腫瘤消融過程中,手術過程中有足夠的流量很重要,因為這將有助於保持視野清晰,使外科醫生能夠看到目標。例如,鐳射碎石術會產生許多小碎石,即所謂的“鈥鐳射風暴”,如果沒有通路鞘,這種結石碎塊雲,會嚴重影響能見度。透過允許連續的低壓沖洗,結石碎片和灰塵狀碎片可以從腎臟中沖洗出來,並透過通路鞘排出。同樣,在鐳射碎石術或腫瘤消融過程中,可能會發生一些出血。透過通路鞘改進的沖洗,沖洗集合系統中的血液,從而保持清晰的視野。同樣,有結石病史或尿路上皮細胞腫瘤病史的患者也可能出現血尿。如果由於尿液中的血液影響視覺化,而未使用 UAS,則在這些患者中進行輸尿管軟鏡檢查可能具有挑戰性。在這些患者中,放置後透過通路鞘的初始返回通常非常暗。然而,透過輸尿管鏡沖洗,現場的血液通常會迅速清除,便於視覺化。
表 24.1 輸尿管通路鞘的優點
UAS 的正確放置允許在輸尿管輸尿管軟鏡檢查期間保持較低的腎內壓。在輸尿管軟鏡檢查期間,將腎內壓保持在 40mmH2O 以下可防止手術期間腎盂靜脈和/或腎盂淋巴迴流。Rehman 等人使用 10/12、12/14 和 14/16 F UAS 研究了屍體腎臟的腎內壓,並將其與沒有 UAS 的對照進行了比較。輸尿管鏡就位後,在 50、100 和 200 cmH2O 的壓力下進行沖洗。如果沒有 UAS,腎內壓升至 52-59 cmH2O,高到足以導致腎盂靜脈和腎盂淋巴迴流。使用 UAS 觀察到較低的壓力。10/12 F 通路產生 22–29 cmH2O 的壓力,而較大的 12/14 和 14/16 F 護套具有較低的壓力,測量值分別為 17.5–19.5 和 14.5–19.5 mmH2O [7]。這表明,至少在腎內壓力管理方面,12/14 F UAS 在鞘的大小和有效性之間取得了最佳平衡。
在上尿路上皮細胞癌的治療過程中,適當選擇和部署的UAS,可能有助於透過維持較低的腎內壓來防止腫瘤細胞外滲。護套還可以減少輸尿管下段,對腫瘤細胞的暴露,因為它有效地覆蓋了尿路上皮,並促進沖洗液直接透過護套而不是圍繞它流出。
在 UAS 就位後,外科醫生可以在手術過程中隨意插入和取出輸尿管鏡。在研究腫瘤時,可以使用較大的儀器(如後載活檢鉗)進行多次活檢。然而,最大的優勢可能是在治療腎結石方面。在對輸尿管上段或腎結石進行鐳射碎石術後,外科醫生能夠透過 UAS 籃式提取碎片,以試圖使患者無結石。移除的碎片的大小受到通路鞘直徑的限制。通路鞘可保護輸尿管,防止意外移除過大的碎片,這些碎片可能會卡在輸尿管中,或者更糟的是,如果不使用鞘,會撕脫輸尿管。如果試圖去除對於鞘來說太大的碎片,則在嘗試進一步去除之前,透過鐳射碎石術進一步減小它們的尺寸。
去除碎片對患者有幾個潛在的好處。當患者透過碎片時,他們可能會出現腎絞痛。更糟糕的是,如果碎片被阻塞,可能需要進一步的干預,包括可能的支架放置或進一步的碎石術。如果碎片未能透過並留在腎臟中,則它們可能成為未來結石形成的病灶 。在一項非隨機研究中,L'Esperance 等人證明與不使用通路鞘的手術相比,使用 UAS 的無結石率高出 12%(分別為 79% 和 67% SFR)[10]。
庫蘭巴斯等人進行了一項研究,將 59例計劃接受輸尿管鏡檢查的患者隨機分為兩組——一組有 UAS,另一組沒有。大多數 (85%) 的手術是針對結石病進行的。他們確定,在手術過程中使用通路鞘時,平均手術時間顯著減少了 10.5 分鐘。此外,儘管通路鞘的成本較高,但在使用鞘的情況下,每位患者的總成本降低了 350 美元。與 L'Esperance 的資料相反,這項研究顯示兩組之間的無石率沒有差異。短期隨訪並未發現研究的通路鞘臂中輸尿管狹窄的發生率增加。
缺血
放置 UAS 的一個問題是是否會發生輸尿管缺血。在一項動物研究中,Lallas 等人使用鐳射多普勒流量計研究了放置通路鞘後豬輸尿管缺血的可能性。放置 10/12、12/14 和 14/16 F 的通路鞘,並從近端輸尿管每隔 5 分鐘進行測量。在前 5 分鐘間隔內,所有輸尿管的血流量均減少,但血流量減少最大的是較大的 12/14 和 14/16 F 鞘,15 分鐘後血流量減少超過 50%。然而,血流量隨後在 70 分鐘時增加到基線水平的 70%。手術後 72 小時對輸尿管進行的組織學檢查顯示沒有缺血或壞死的證據 。這表明,儘管血流量最初減少,但影響是短暫的,減少不足以誘發缺血性壞死。
輸尿管血流量的暫時減少提出了一個問題,即接受輸尿管鏡檢查的患者是否會增加狹窄形成的風險。迄今為止,還沒有隨機資料表明這是一種風險。在一項非隨機研究中,Delvecchio 等人。回顧了 150 名使用 UAS 接受輸尿管鏡檢查的患者的記錄。其中 62 名患者的隨訪時間超過 3 個月。在該亞組中,只有一名患者出現狹窄,表明總體狹窄率與之前公佈的無鞘輸尿管鏡檢查後的狹窄率相似。
支架或無支架
在過去的十年中,關於是否在輸尿管鏡檢查後放置支架的爭論一直在持續。幾項研究表明,在簡單的輸尿管鏡檢查中,不需要常規支架置入術,並且未置入支架的患者疼痛、麻醉劑使用和發病率降低。然而,這項工作是在 UAS 廣泛使用之前完成的,這些研究不討論 UAS 的使用。UAS 的放置可能會在插入過程中對輸尿管造成一些輕微的損傷以及短暫的缺血。拉帕波特等人在一項非隨機系列患者中報告說,接受輸尿管鏡檢查和 UAS 的患者中有 37% 在術後期間返回進行計劃外急診,而接受輸尿管鏡檢查的患者中則有 14% 不帶通路鞘。他們建議在所有涉及 UAS 的輸尿管鏡檢查病例後放置支架。目前尚不清楚是什麼導致在手術期間放置 UAS 的組中 ER 就診率增加,但輸尿管痙攣或水腫引起的短暫絞痛是一種可能的解釋。
減少鏡頭的損害
現代輸尿管軟鏡有限的耐用性和高維修成本是一個應用障礙,對於一些希望採用該技術的中心來說是難以克服的 。在使用歷史對照的非隨機研究中,Pietrow 等人報告說,當使用 UAS 時,與不使用通路鞘時(27.5 次使用)相比,他們能夠在需要修理內窺鏡之前將手術次數增加一倍。有幾個因素可能導致這種情況。當不使用 UAS 時,輸尿管軟鏡通常透過導絲向上傳遞(鐵路技術)。這可能會導致導線損壞內窺鏡通道,尤其是具有剛性後端的導線。輸尿管鏡通道的小穿孔會導致洩漏,從而進一步損壞內窺鏡。通道中的小瓣也可能會導致器械難以透過。此外,當輸尿管鏡前進過程中遇到阻力時,內窺鏡會因受力而彎曲。鑑於這些瞄準鏡的精緻設計,這也可能導致進一步的損壞。當透過 UAS 推進時,可以防止鏡頭彎曲。
不同通路鞘的特性
有多種市售的 UAS,它們的物理特性各不相同。通路鞘的特性可能會影響它們的臨床效果。蒙加等人在一項研究中評估了 8 種 UAS,以確定它們對屈曲和扭結的抵抗力以及潤滑性(摩擦係數)。他們確定 Applied Forte XE(Applied Medical,Rancho Santa Margarita,CA)和 Cook Flexor 鞘(Cook Medical,Bloomington,IN)的抗扭結性和潤滑性都最強(圖 24.1)。Cook Flexor 還具有最大的抗屈曲能力 。透過防止扭結,進入通路鞘的內腔在手術過程中不太可能塌陷。具有較低的摩擦係數,可以使通路鞘更容易滑上輸尿管,但也可能使其在手術過程中更容易向後滑動。當遇到一些阻力時,例如在輸尿管口或骨盆邊緣,抗屈曲可以使護套更容易透過。
使用這些資料,進行了一項前瞻性隨機試驗,在一項臨床研究中比較了這兩種鞘。54 名患者隨機接受使用 12/15 F Applied Access Forte XE 或 12/14 F Cook Flexor 進行輸尿管軟鏡檢查。這兩種鞘均採用嵌入式線圈系統進行加固,並具有親水塗層。Applied Access Forte XE 的整體裝置故障率為 44%,而 Cook Flexor 沒有故障。屈曲 (25%)、扭結 (25%) 和難以透過器械 (13%) 是 Applied 護套失敗的原因。值得注意的是,在應用鞘管失敗的程式中,隨後嘗試放置庫克屈肌鞘管。在所有情況下, Cook屈曲均已成功放置。Cook Flexor 在放置的難易度、器械透過和結石取出的難易度方面,外科醫生主觀上的評分也更高。作者推測,Applied 護套的較大外徑(15 F 與 14 F)以及護套尖端的長度和配置可能是影響研究結果的一個因素。
一項後續研究在屈曲和扭結方面評估了“下一代”鞘“系統。評估的鞘包括 Cook Flexor(12/14 F,35 cm)、ACMI UroPass(12/14 F,38 cm)(Gyrus ACMI,Southborough,MA)、Bard Aquaguide(11/13 F,35 cm)(Bard Medical , Covington, GA) 和 Boston Scientific Navigator (11/13 和 13/15 F, 36 cm) (Boston Scientific, Natick, MA)。Cook Flexor 再次是最耐屈曲的,需要 5.1 N 才能屈曲,其次是 ACMI 3.2 N、Bsci-13/15 2.9 N、Bard 2.8 N 和 Bsci-11/13 2.0 N . Bard 和 BSci 11/13 的較小直徑似乎使它們更容易彎曲。Bard 鞘最容易扭結,只需 9 N/mm 即可扭結。BSci 13/15 扭結為 30 N/mm,BSci 11/13 為 41 N/mm,Cook 為 42 N/mm,最不可能扭結的是 ACMI 為 83 N/mm。所有測試的鞘都有親水塗層,並顯示出相似的摩擦係數。
臨床經驗表明,使用現代線圈增強接入鞘 UAS 在手術過程中很少看到鞘的扭結,但隨著鞘的推進可能會遇到屈曲。將 UAS 穿過 Amplatz 超硬導絲可能會降低屈曲的發生率,但必須注意不要施加太大的力,以避免對輸尿管造成創傷。研究表明,有經驗的泌尿科醫生在放置通路鞘時使用高達 6.6 N 。雖然在導絲上推進通路護套時刺穿輸尿管所需的確切力取決於所使用的 UAS 型別以及個體患者因素,但 CT-1 針需要 4.7 N 的力才能刺穿人體輸尿管。
UAS 和輸尿管軟鏡結合,在其它方面的應用
雙鏡聯合的應用,在經皮腎鏡手術期間,使用輸尿管軟鏡結合 UAS 可能是有利的。透過在經皮腎鏡取石術 (PCNL) 開始時,以逆行方式放置 UAS,通路鞘允許小結石碎片透過鞘流出,而不是卡在輸尿管中。這也有助於在手術過程中維持腎臟集合系統內的低壓。在經皮穿刺之前,可以在手術過程中將輸尿管軟鏡向上推進到腎臟中,以顯示最佳的腎盞。可以透過內窺鏡注入造影劑或空氣以方便穿刺,但內窺鏡的尖端也可以作為透視目標。將範圍就位後,當針頭進入收集系統時,可以直接看到針頭的穿刺情況。導絲也可以用穿過內窺鏡的取石籃捕獲並透過 UAS 取出。帶有鐳射碎石和取石籃提取的輸尿管鏡軟也可用於清除 PCNL 過程中,無法以順行方式到達的殘留結石負荷。這可能會減少結石大或複雜的患者對多個腎造瘻道的需求 。
徑向球囊擴張式輸尿管通路鞘
已經報道了一種包含徑向擴張球囊的新型 UAS。整合到 UAS 中的徑向擴張球囊的擬議優點是它消除了與軸向擴張相關的剪下力。據報道,這是在 PCNL 期間使用球囊擴張與徑向擴張相比的優勢,並且可能轉化為與 UAS 放置類似的發現。哈珀等人報告了他們放置球囊擴張式輸尿管通路 (BEUS) 的經驗,並將其與在 10 頭豬中放置傳統鞘管 (Cook Flexor, 12/14 F) 進行了比較。BEUS 在非膨脹形式下為 9.5 F,在放置後它膨脹到具有 12 F 的內徑和 14 F 的外徑。研究表明,BEUS 需要的最大值更少(0.36 磅與 1.48 磅),與傳統 UAS 相比,放置的平均力更小(0.11 磅與 0.49 磅)。透過 BEUS 的流速也比傳統 UAS 略有提高(90.0 cc/min 與 80.6 cc/min)。 BEUS 對輸尿管整體損傷較小 。這種型別的通路鞘設計有望成為對當前設計的進步。但是,可能需要對通路鞘放置技術進行一些更改。在放置之前,確保輸尿管中沒有未被識別的狹窄是很重要的。如果遇到鞘不能擴張的緊密狹窄,則需要透過狹窄拉動擴張的鞘。目前還不清楚這會對輸尿管施加多大的力,但令人擔憂的是可能會產生足夠的力,來導致輸尿管撕裂的風險。該力會根據狹窄的位置和其他患者因素而變化。透過在放置鞘管之前執行逆行輸尿管造影,人們將能夠識別以前無法識別的狹窄並在放置 BEUS 之前對其進行適當治療。
UAS 促進大型腎內結石的治療
傳統上,大於 2.0 cm 的腎結石採用 PCNL 治療,已被證明既安全又有效 。然而,在某些特定的患者群體中,PCNL 可能是困難的或不可能的,例如病態肥胖、解剖結構變形導致難以經皮進入腎臟、長期抗凝或拒絕 PCNL 的患者。此外,PCNL 具有相關的併發症,通常至少需要住院過夜。UAS 的發展和擴大使用,以及輸尿管軟鏡和鈥激光纖維的進步,使外科醫生在透過輸尿管鏡治療更大的結石負擔方面變得越來越積極。海姆斯等人對接受輸尿管軟鏡鈥鐳射碎石術治療 2-3 cm 結石的患者進行了回顧性多中心審查,67% 的病例使用了 UAS,84% 的患者進行了單階段手術。這組選定患者的總體併發症發生率較低,但無結石率較低,僅有 47% 的患者無石,66% 的患者碎片≤2.0 cm。萊利等人報道了他們在所有患者中使用 UAS ,使用輸尿管軟鏡和鈥鐳射碎石術治療 22 名大於 2.5 釐米結石患者的經驗 (13/15 F)。患者平均接受了 1.82 次手術,只有 5 名患者需要一次手術。併發症低,總體無石率(定義為碎片
使用 UAS 的輸尿管軟鏡及鈥鐳射碎石術,似乎是具有大結石負荷的特定患者的可行替代治療方法。未來需要將 PCNL 與 URS 與鐳射碎石術和 UAS 進行比較的隨機試驗,以更好地定義這兩種程式的相對利弊。
技術:腎結石
現今, UAS已常用治療腎結石。術前未置入支架的患者,選用12/14 F UAS,術前置入支架的患者,尤其結石負荷較大的患者,選用14/16 F UAS。對於女性,選擇 35 釐米的長度,除非她們的身高低於 152 釐米,在這種情況下,使用 28 釐米的UAS。對於男性,選擇 45 釐米長的 UAS(表 24.2)。用直導管排空膀胱,如果懷疑合併輸尿管結石,則使用 8-10 同軸擴張器擴張遠端輸尿管,並使用低於 7.0 F 的半剛性輸尿管鏡檢查輸尿管。如果懷疑沒有輸尿管結石,則透過 5 F 開口導管進行逆行腎盂造影。逆行腎盂造影可將結石證明為充盈缺損,識別其他病理,重要的是,它將顯示出上輸尿管和 UPJ 的解剖結構,這將指導 UAS 的放置 。使用 Superstiff 鋼導絲可降低 UAS 推進過程中導絲扭結和彎曲的風險。在透過 UAS 以啟用親水性之前,應用水徹底潤溼 UAS塗層。如果可能,將 UAS 推進到 UPJ 的水平,但如果輸尿管在 UPJ 處有明顯的角度,則必須注意不要過度推進 UAS ,因為 UAS 的剛性尖端會傷害輸尿管或腎臟。 UAS 的推進應始終在透視引導下向下(圖 24.2)。一旦到位,內部閉塞器和 Superstiff 金屬絲就應被移除。然後用 2.0 絲線縫合將護套固定到患者的大腿內側。這可以防止 UAS 在手術過程中滑出,從而減少在沒有內部閉孔器就位的情況下,重新定位通路鞘造成的潛在輸尿管損傷。使用加壓沖洗系統,然後用輸尿管軟鏡仔細檢查腎臟。透視可以幫助這個過程,並且所有的腎盞都應該被視覺化。目標視覺化後,鈥激光纖穿過時應注意保證鏡面筆直,以免損壞脆弱的內通道。300 μm 纖芯尺寸的光纖用於最大化透過內窺鏡的流量,而不是限制偏轉,並減少偏轉機構的磨損。6 Hz 頻率下 0.6 J 的鐳射能量設定是典型的啟動設定。如果結石看起來非常緻密,則根據需要選擇更高的能量和脈衝率。結石破碎後,用 1.5 F 無尖鎳鈦諾取石籃去除碎片。必須小心不要試圖取出太大的碎石塊,否則可能會損傷輸尿管。取出碎片後,緩慢撤回 UAS,同時用輸尿管鏡檢查輸尿管。這樣做是為了確保輸尿管中沒有遺漏結石,並且沒有看到輸尿管的其他病理。移除鞘管後,進行另一次逆行腎盂造影,放置 6 F 輸尿管支架,並排空膀胱。
表 24.2 輸尿管通路鞘的優點
降低腎內壓
改進的視覺化
能夠使輸尿管鏡進行多次檢查
取出結石碎片時保護輸尿管
減少活檢或消融期間下尿路中腫瘤細胞的暴露,減少活檢或消融期間下尿路中腫瘤細胞的暴露
減少內窺鏡的磨損
我們的做法是將支架留在原位大約 7 天。患有不透射線結石的患者在移除支架前進行 KUB, 以確保沒有任何明顯的殘留碎片。支架取出後,患者在 8 周後返回進行腎臟超聲檢查。
結論
UAS 的發展促進了輸尿管軟鏡在治療腎結石和腫瘤等上尿路病變方面的應用。如果使用得當,UAS 可以促進安全、低壓的程式,具有出色的視覺化效果,減少了軟鏡的磨損,並且能夠根據需要輕鬆地多次透過軟鏡。UAS 的未來改進可能會看到採用徑向擴張的鞘。
【來源:中國網醫療頻道】