長期以來,科學家們對人體的神經控制機能,特別是大腦意識的產生感到十分困惑,包含大腦在內的神經系統,無論是物質和能量的轉換過程,還是大腦自主意識的形成,抑或大腦意識反饋肢體行為等等,似乎都是“遙不可及”的。
如果人類能夠全面掌握神經系統特別是大腦的作用機能,創造出可以影響甚至控制大腦意識產生和反饋的“干擾”模式,那麼不但會為治療神經系統疾病提供支撐,而且從遠期看還會為“腦機介面”的真正實現,打下堅實的基礎。
美國科技“狂人”馬斯克,近年來也在“瘋狂”地做著有關“腦機介面”的實驗,先後以植入大腦晶片的方式,對小豬和猴子的大腦進行“改造”。其中對小豬的實驗,證明了植入晶片的確可以判斷小豬的精神變化情況,為後續實驗奠定了基礎。而對猴子的實驗,則更進一步,在晶片中加入了可以發射訊號的無線電裝置,透過人工干預訊號的刺激,來教猴子打電子遊戲,試圖控制猴子大腦的意識。
這兩個實驗均取得了一定成功,但是代價也很大。由於要想將晶片植入大腦,必須開啟顱骨,掀開大腦皮層,因此一定會對實驗物件造成神經組織的損傷。那些實驗小豬和猴子,有相當一部分在實驗後發生死亡,即使沒有死亡的,身體自由活動能力也受到很大限制。所以,類似的“腦機”介面實驗,受到了很多科學家的質疑和反對。
美國斯坦福大學的一個研究團隊,近日另闢蹊徑,採取了不需要植入大腦晶片的方式,而是利用近紅外光線,來進行遠端操控小白鼠大腦細胞,實驗竟然成功了。
這項研究的出發點,是根據之前已經具備一定科學基礎的技術,即光遺傳學來實施的。光遺傳學是什麼呢?簡單來說,就是透過基因技術,首先改變大腦細胞的部分基因性狀,使其在細胞膜結構上能夠表達出光敏蛋白,然後再利用特定波長的光線,來照射這些大腦細胞,從而控制光敏蛋白的“開關”,最終達到控制大腦神經元活動的目的。
由於大腦是非透明的,用光源照射時不可能使光線透過,所以傳統的光遺傳學技術,必須在實施物件的大腦上安裝特定的光學裝置,因此並沒有從根本上改變將異物“植入大腦”的弊端。
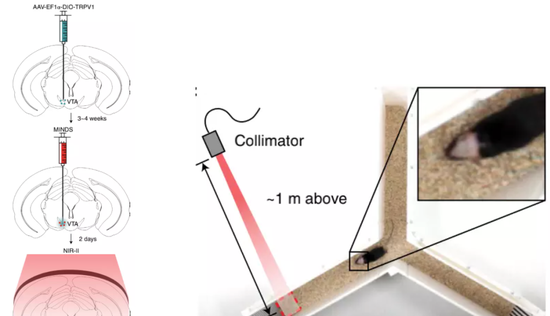
研究團隊為此,做了兩個方面的改進,一個是在光源的選擇上,採用了1000-1700nm的近紅外波段,這種光線即使在動物的大腦內,也能擁有較高的穿透性。另一個改變是透過基因技術,提取動物體內原有的TRPV1蛋白質,然後在這個蛋白質上面做文章。
TRPV1這種蛋白質是一種能夠感受灼熱和疼痛感的受體。研究團隊使用腺病毒,在這種病毒的表面包裹一層TRPV1蛋白,然後去感染大腦內的目標神經元,從而將腺病毒的遺傳物質與蛋白一起引入了神經細胞內部。作這些預處理之後,研究團隊將它率先植入蛇的體內,蛇就能改變原有夜間基本不捕食的習性,在夜間也變得活躍起來。與此同時,把這種蛋白植入小白鼠眼睛的視錐細胞中,小白鼠也擁有了在夜間看清溫熱物體的能力。這就說明,這種蛋白受體對近紅外光線非常敏感。
不過,當將這種受體蛋白植入小白鼠的大腦神經元之後,卻發現對近紅外光線並不起作用,這主要是由於近紅外光線的能量太小所致。於是研究團隊進行了最後的處理,那就是在上述改造後的腺病毒內,又想方設法增加了一種專門用於吸收和放大紅外光線的“感測器”,起到放大近紅外光線訊號的目的。
於是正式實驗開始,研究團隊透過控制紅外光源訊號,來引導處在“迷宮”中的小白鼠,結果發現被“改造”後的小白鼠,在夜間的活動能力增強,並且似乎對紅外光線非常喜歡,能夠快速找到光源,並且長時間地“沐浴”在紅外光線的照射範圍內。而對照組沒有進行“改造”後的小白鼠,則沒有這種行為方式的改變。在一定程度上,這個實驗說明利用近紅外光線的方式,可以達到控制“改造”後大腦神經元的活動,從而能夠影響和操控實驗物件的行為模式。
透過這個實驗,讓一些人看到了今後攻克癲癇、漸凍症等神經系統疾病的曙光。不過,仍然有很多人對此感到非常擔憂,最主要的是這個實驗,並非完全意義上的“非侵入式”,排除近紅外線的照射、TRPV1蛋白的“迴歸”因素外,實驗的關鍵是需要透過腺病毒的方式來侵入神經元或者大腦細胞。
雖然不需要破壞實驗物件的頭骨或者大腦皮層,但是利用病毒的方式來影響和改變神經細胞的生理功能,不確定性和潛在風險仍然很大,從某種意義上來說,這種風險要比異物植入還要具有不確定性。還是那句話,科學技術的進步,固然離不開大膽的嘗試,但是必須要以不損害人類的利益、不對人類造成威脅、不違背倫理道德為基本底線,在沒有充分的論證和精準的評估之前,還是最好不要貿然投入臨床試驗。