編者按:3c型糖尿病,又稱胰源性糖尿病、胰腺外分泌糖尿病,是胰腺外分泌疾病所導致的一種特殊型別糖尿病,慢性胰腺炎(Chronic pancreatitis,CP)和胰腺癌(Pancreatic cancer,PaC)是其主要病因。
3c型糖尿病的主要特徵為胰腺內分泌及外分泌腺均受損,病理生理機制複雜,臨床異質性大,且涉及消化科、普外科、內分泌科等多個學科,很難被正確識別並分型,常常被漏診或誤診為2型糖尿病(T2DM),其臨床診治存在很大挑戰。東南大學附屬中大醫院內分泌科李玲教授團隊與美國加州大學UCLA深入合作,2022年在Diabetes & Metabolism等期刊發表了兩項最新研究[1, 2],透過混合膳食測試評估慢性胰腺炎後糖尿病(PPDM)以及胰腺癌相關糖尿病(PaCDM)患者進食前後胰腺功能及胃腸道激素水平的變化,揭示了3c型糖尿病與T2DM鑑別的臨床特徵。李玲教授的博士生祁靚、鮑建彤分別為兩篇文章的第一作者,我們一起來看這些研究。
要點概覽
與T2DM相比,PPDM患者餐後C肽(CP)、胰島素(INS)、胃飢餓素(Ghrelin)和肽YY(PYY)反應性降低;其胰島β細胞功能降低,而胰島素敏感性增高。
PPDM的發病機制與胰島細胞功能障礙、INS分泌減少,胰高血糖素(GCG)升高及腸促胰素(GIP/GLP-1)效應受損有關。
PaCDM患者以胰島β細胞功能低下、胰島素及C肽釋放低平為特徵。
PaCDM患者胰島素敏感性高於T2DM患者,與健康志願者無明顯差異。
引言
近年來,3c型糖尿病的發病率逐漸增長,患病人數上升至所有型別糖尿病的第二位,受到國際廣泛關注[3]。3c型糖尿病包括PPDM、PaCDM、囊性纖維化相關糖尿病(CFRD)[4],以及與其他一些罕見病因相關的糖尿病(纖維結石性胰腺病、血色素沉著症、遺傳障礙)[5]。作為一種特殊型別糖尿病,3c型糖尿病的臨床診斷和發病機制仍不清楚。
CP是3c型糖尿病的主要原因之一,80%的CP患者可發展為3c型糖尿病[6]。李玲教授團隊近期發表在Pancreas上關於3c型糖尿病的Meta分析表明,隨著內分泌功能損傷的進展,33%的CP患者會在5年內發展為PPDM[7]。胰島細胞的廣泛破壞,尤其是β細胞功能障礙是PPDM的主要原因[8]。同時,胰島中所有型別的細胞(α、β、δ、PP和ε細胞)及其分泌激素(胰高血糖素、胰島素、生長抑素、胰多肽和胃飢餓素)的功能障礙也參與其發生[9]。此外,腸道內分泌細胞及其分泌的腸道激素如GLP-1、GIP和PYY可透過調節胃排空和胰島素分泌以響應食物攝入,在3c型糖尿病中發揮重要的作用[10]。因此,檢測多種胰腺和腸道激素可能有助於闡明PPDM的病理機制,並利於建立更可靠的診斷策略來區分PPDM和T2DM。
胰腺癌(PaC)是一種惡性程度高、發展快、預後極差的惡性腫瘤,5年生存率僅10%,新發糖尿病可能為其早期臨床表現。這種與PaC發生發展密切相關的糖尿病,又稱為PaCDM。目前,PaCDM特徵尚未明確,與T2DM分型不清,致使大部分患者在早期被誤診為T2DM,從而延誤了最佳治療時機。本研究透過混合餐刺激下的胰腺及胃腸激素反應,比較PaCDM患者與T2DM患者的腸胰功能,為後續臨床診斷標準的建立提供依據。
混合膳食被認為是測量各種胰腺和腸道激素餐後反應的理想刺激物。本研究旨在比較CP/PaC、PPDM/PaCDM、T2DM和健康志願者對混合膳食測試後的胰腺和腸道激素反應的差異,同時關注胰島素分泌和胰島素敏感性的變化。
材料和方法
受試者(隔夜禁食至少8 h後)給予12盎司標準混合膳食(360卡路里、61.5 g碳水化合物、15 g蛋白質和6 g脂肪),5 min內勻速飲用。分別於空腹和進餐後15、30、60、120 min收集血清,其中CP、INS、GCG、Ghrelin、GLP-1、GIP和PYY的濃度透過MILLIPLEXMAP人代謝激素磁珠板(HMHEMAG-34K)基於Luminex xMAP技術(Luminex Corporation,Austin,USA)檢測。
結果
01
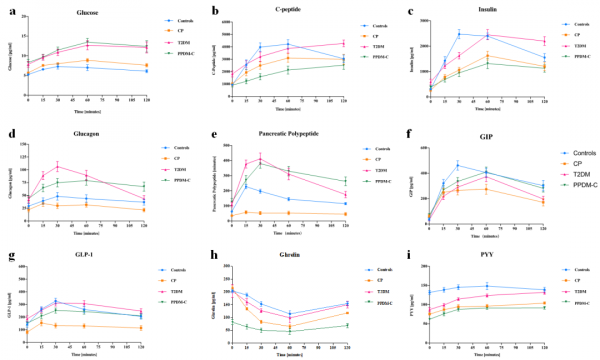
在PPDM患者中,與健康對照組相比,其表現出較低的Ghrelin和PYY水平;與CP患者相比,其GCG、PP、GLP-1和GIP升高;與T2DM相比,其C肽、Ghrelin和PYY降低(圖1)。
圖1. 混合膳食測試過程中血清葡萄糖(a)、C肽(b)、胰島素(c)、胰高血糖素(d)、胰多肽(e)、GIP(f)、GLP-1(g)、Ghrelin(h)和PYY(i)在CP(橙色)、T2DM(紅色)、PPDM(綠色)和健康對照(藍色)組中的水平。資料表示為平均值±標準誤
02
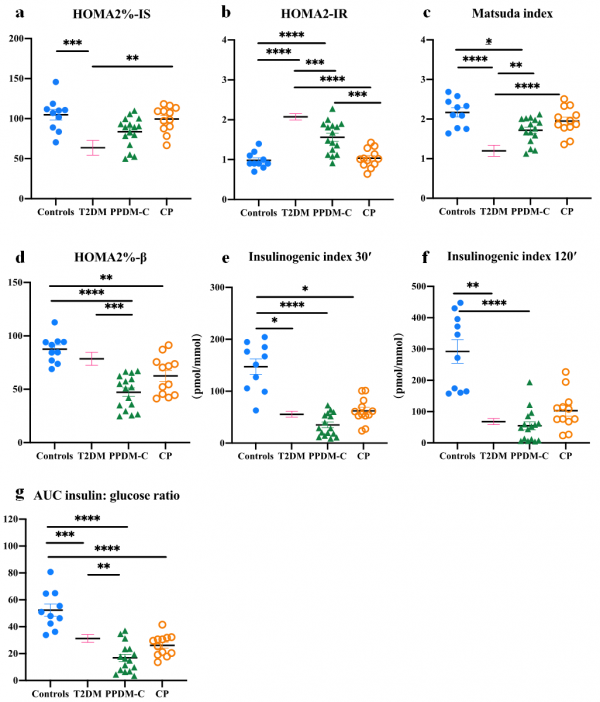
與T2DM相比,PPDM組胰島β細胞功能降低,胰島素敏感性增高(圖2)。
圖2. 空腹[HOMA2%-IS(a)、HOMA2-IR(b)]和餐後[松田指數(c)]胰島素敏感性以及空腹[HOMA2%-β(d)]和餐後[胰島素分泌指數30ʹ(e)、胰島素分泌指數120ʹ(f)、AUC胰島素:葡萄糖比(g)]胰島β細胞功能在T2DM、PPDM-C、CP和健康對照組的差異
03
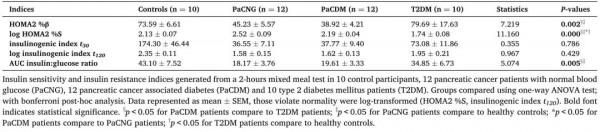
與T2DM相比,PaCDM組以胰島β細胞功能低下、胰島素及C肽釋放低平為特徵;其胰島素敏感性增高,與健康志願者無明顯差異(表1)。
表1. 各組的胰島素指標濃度
總結
這兩項研究旨在調查PPDM及PaCDM患者胰腺和腸道激素對混合膳食測試的反應。結果提示,與T2DM相比,PPDM的特徵是INS、Ghrelin和PYY反應降低,GCG、PP、GIP和GLP-1水平相似。在CP基礎上,PPDM的發病機制與胰島細胞功能障礙、INS分泌減少、GCG升高及GIP/GLP-1作用受損有關。PPDM與PaCDM患者均表現出胰島β細胞功能低下,而胰島素敏感性高於T2DM患者。該發現經更大規模人群驗證後,對闡明3c型糖尿病的發病機制、展示其與T2DM鑑別的臨床特徵、推動規範化診療具有重要臨床意義。
參考文獻
1. Qi L, et al. Pancreatic and gut hormone responses to mixed meal test in post-chronic pancreatitis diabetes mellitus. Diabetes Metab. 2021; 48(3): 101316.
2. Bao J, et al. Pancreatic cancer-associated diabetes mellitus is characterized by reduced β-cell secretory capacity, rather than insulin resistance. Diabetes Res Clin Pract. 2022 185: 109223.
3. Petrov MS. DIAGNOSIS OF ENDOCRINE DISEASE: Post-pancreatitis diabetes mellitus: prime time for secondary disease. Eur J Endocrinol. 2021; 184(4): R137-R149.
4. Petrov MS. Diabetes of the exocrine pancreas: American Diabetes Association-compliant lexicon. Pancreatology. 2017; 17(4): 523-526.
5. 2. Classification and Diagnosis of Diabetes: Standards of Medical Care in Diabetes-2021. Diabetes care. 2021; 44(Suppl 1): S15-s33.5.
6. Petrov MS, Yadav D. Global epidemiology and holistic prevention of pancreatitis. Nat Rev Gastroenterol Hepatol. 2019; 16(3): 175-184.
7. Zhu X, et al. New-Onset Diabetes Mellitus After Chronic Pancreatitis Diagnosis: A Systematic Review and Meta-analysis. Pancreas. 2019; 48(7): 868-875.
8. Sasikala M, et al. β-Cell dysfunction in chronic pancreatitis. Dig Dis Sci. 2012; 57(7): 1764-1772.
9. Da Silva Xavier G. The Cells of the Islets of Langerhans. J Clin Med. 2018; 7(3): 54.
10. Latorre R, et al. Enteroendocrine cells: a review of their role in brain-gut communication. Neurogastroenterol Motil. 2016; 28(5): 620-630.
專家簡介
李玲
德國醫學博士,美國加州大學博士後,主任醫師,教授,博士生導師。現任東南大學胰腺研究所所長、糖脂代謝研究中心主任,東南大學附屬中大醫院院長助理、內分泌科主任。江蘇省“青年科技獎”獲得者,江蘇省中青年領軍人才,江蘇省“六大人才高峰”,江蘇省“六個一工程”高層次人才,江蘇省“科教強衛”醫學重點人才。擔任中華醫學會心身醫學分會青委副主委、中華醫學會糖尿病學分會青委、江蘇省醫學會糖尿病學分會副主委,南京市醫學會內分泌分會副主委。現為國家自然科學基金委醫學科學部評委、教育部博士學位論文評審專家、SCI前沿期刊客座主編。
長期致力於胰腺內、外分泌時空網路對話研究,國家重點研發計劃幹細胞專項子課題負責人,主持國家自然科學基金5項,主要負責國家級科研專案8項,以通訊作者在Nature Communications等期刊發表SCI論文50餘篇,其中IF≥10分7篇。榮獲國家教育部高等學校科學研究優秀成果獎、江蘇醫學科技獎、江蘇省新技術引進獎。多次應邀赴德國和瑞士胰腺研究所進行學術交流訪問,並被美國胰腺學會主席、加州大學胰腺研究中心主任Stephen Pandol教授邀請為國際合作夥伴,將進一步拓展胰腺疾病與糖尿病的器官組織間對話前沿研究。