最近,Replicor公司宣佈,成功確認核酸聚合物(NAP)靶向乙肝病毒亞病毒顆粒(SVP),並以“HBsAg isoform dynamics during NAP-based therapy of HBeAg-negative chronic HBV and HBV/HDV infection”為題發表在Hepatology Communications上(內容比較長,需要點耐心)。
乙肝REP301/-LTF/401研究,S-HBsAg下降更快,完整資料及結論公佈
這是由Replicor公司贊助的 REP 301、301-LTF 和 REP 401 研究,並由雅培診斷公司(Abbott Diagnostics)贊助的實驗性HBsAg亞型檢測。在三項研究中,在基於NAP的組合療法,觀察到的 qHBsAg下降包括所有 HBsAg 亞型的下降,並且與NAP的引入相關。
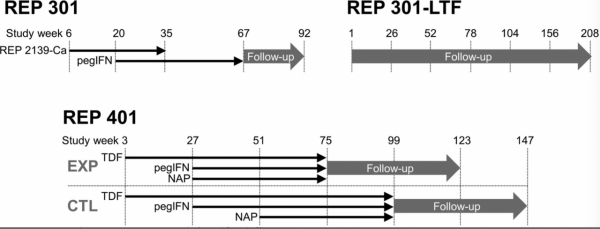
REP 301 和 REP 301-LTF 研究(上)和 REP 401 研究(下)的設計
在42名 qHBsAg 大幅下降(較基線>2log10 IU/ml)的參與者中,觀察到有39人 S-HBsAg 的更快清除(與基線相比>2log10 IU/ml),研究人員認為,這與之前發表的NAPs對球形SVP組裝和分泌的選擇性作用相一致。
選擇性 S-HBsAg 下降在10名受試者中9名qHBsAg中度(<2log10 IU/ml)下降,與 TDF + pegIFN 通常觀察到的適度 qHBsAg 反應一致,進一步表明,NAPs在這些患者中不僅抗病毒作用減弱,而且需要抑制SVP的組裝和釋放才能使HBsAg強烈而快速的下降。
一小部分參與者 HBsAg 對NAP反應減弱的基礎尚未完全瞭解,但似乎並不是因為肝細胞吸收減少,因為無論HBsAg反應如何,HBV/HDV合併感染的參與者的HBV-NAP反應是相似的在早期的研究中,增加NAP劑量的頻率可以挽救HBsAg的輕微反應,表明NAP向ERGIC (SVP形態發生的部位)的轉運在這些參與者中可能會減弱,更多的NAP頻繁攝取到肝細胞中可能會改善。
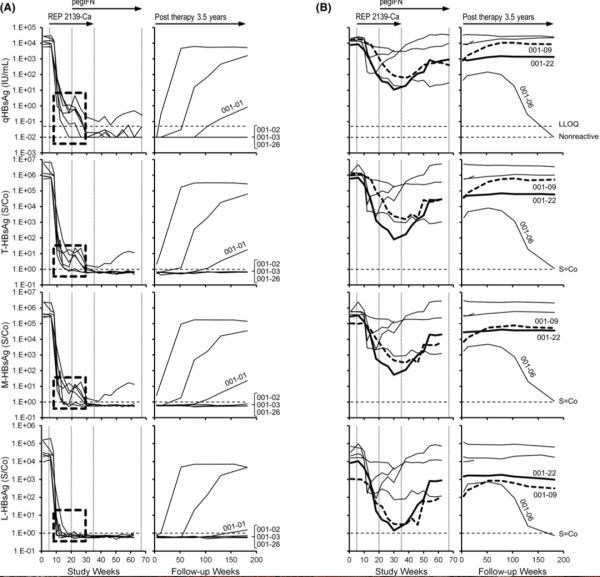
REP301/301-LTF的治療和隨訪期間,總乙肝表面抗原 、中等HBsAg和大HBsAg同種型個體參與者動態
隨訪結束時,在所有實現功能性治癒HBV的參與者中,均未檢測到HBsAg亞型。然而,在隨訪期間,8名參與者的qHBsAg微量反彈(<10 IU/ml)似乎主要由S-HBsAg和M-HBsAg組成。此外,在隨訪結束時,這些參與者的cccDNA活性標記物要麼很低,要麼不存在。雖然S-HBsAg和M-HBsAg的產生普遍儲存在整合HBVDNA中,但在相當少數HBV-DNA整合中,L-HBsAg的產生被preS1區破壞。因此,這些參與者中S-HBsAg和M-HBsAg的選擇性反彈可能來自不能產生L-HBsAg的整合HBVDNA。
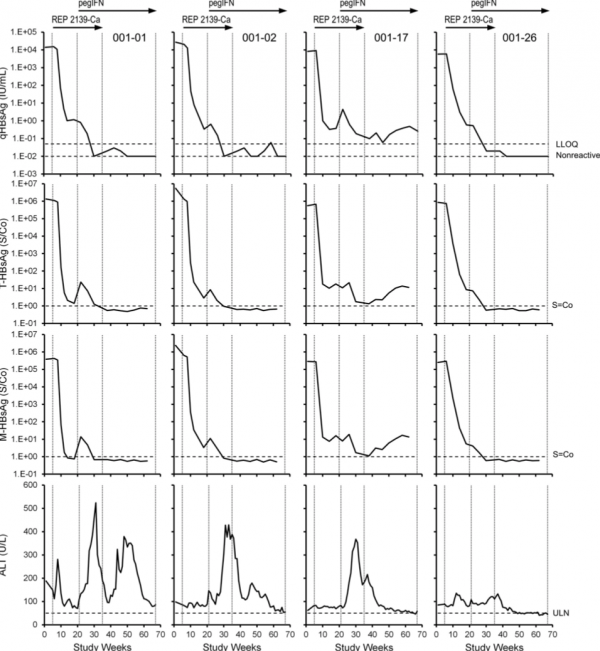
REP 2139-Ca單藥治療結束時存在殘留qHBsAg的 4 名REP 301參與者中,T-HBsAg和M-HBsAg同種型和ALT個體參與者動態
在基於NAP為基礎的治療或隨訪期間的結果中,未發現 HBsAg亞型基線水平與 HBsAg 下降之間存在相關性。然而,在 REP 301/301-LTF 和 REP 401 研究中,除了引入NAPs後早期觀察到的選擇性 S-HBsAg 下降之外,qHBsAg <10 IU/ml 時的HBsAg整體清除似乎對L-HBsAg比其他HBsAg異構體更有效。雖然這種對 L-HBsAg 清除的選擇性作用與在HBV感染的乙肝e抗原陽性接受核苷類藥物治療(NUC)中出現的 M-HBsAg和L-HBsAg的選擇性下降有關,但在 REP 301和REP 401研究中,並未包括乙肝e抗原陰性參與者中的M-HBsAg。在REP 301研究中,在沒有NUCs和pegIFN治療之前發生。
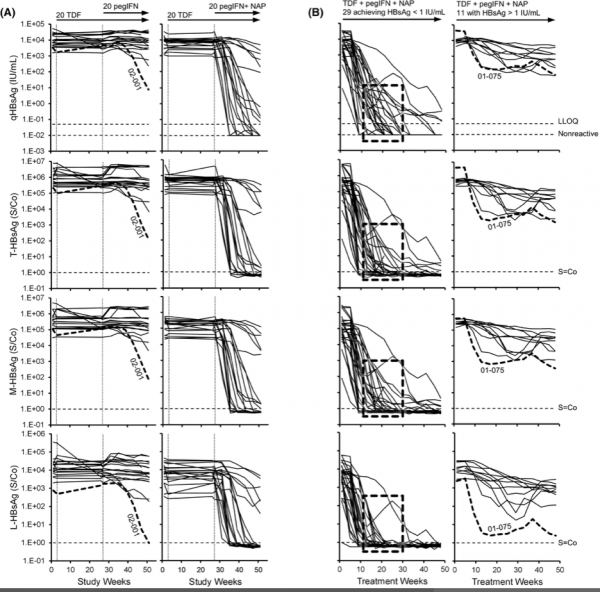
REP401研究中治療期間T-HBsAg、M-HBsAg 和 L-HBsAg 同工型的個體參與者動態
最近研究表明,使用NUCs和pegIFN可以使cccDNA失活/降解,這兩種方法都是本研究中評估的基於NAP療法的組成部分。這些作用可能有助於透過滅活/清除cccDNA來更有效地清除 L-HBsAg。在HBV/HDV共感染參與者中,L-HBsAg的清除更為有效,這可能反映了合併感染中cccDNA的水平較低,隨後隨著T-HBsAg和M-HBsAg的清除(伴隨著轉氨酶發作),提示整合HBVDNA的清除。
這些懸而未決的問題強調了進一步研究的必要性,最好包括HBsAg定量異構體分析。在經歷強烈qHBsAg下降的參與者中,觀察到的選擇性S-HBsAg亞型反應證實了NAP在接受NAP治療的人中抑制球形SVPs組裝和分泌的選擇性作用。在未來的NAP研究中,進行額外的亞型分析將有助於更詳細地檢查NAP在人類中的抗病毒作用。

隨訪期間REP 401研究中 T-HBsAg、M-HBsAg和 L-HBsAg亞型的個體參與者動態
小番健康結語:因為沒有詳述試驗方法,直接將研究人員的核心觀點表述出來,接下來我們簡單歸納一下本研究人員是怎麼思考並設計這些研究的,以及得到的結論。目前,已有幾種在研乙肝新藥屬於核酸聚合物(NAP),NAP可以阻斷乙肝病毒的亞病毒顆粒的組裝,有效防止乙肝表面抗原在迴圈中的補充。
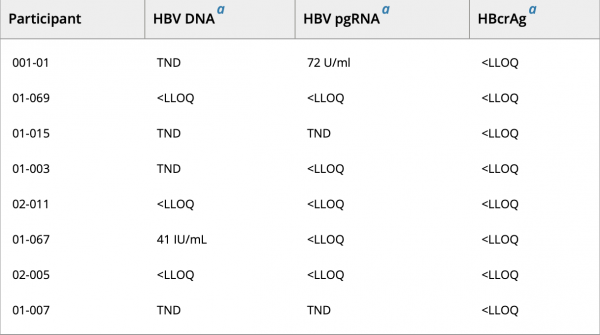
qHBsAg 反彈 <10 IU/ml 參與者隨訪結束時共價閉合環狀DNA活性的標誌物
以NAP為基礎的組合療法,應用在HBV感染或HBV/HDV共同感染時,研究人員觀察到了組合療法伴隨著HBsAg清除和血清轉換,在共同感染中HBVRNA清除,以及持續的HBV功能性治癒(HBsAg < 0.05 IU/ml,HBV-DNA靶標未檢測到,丙氨酸氨基轉移酶正常化)和持續的HDVRNA清除!在REP 301/REP 301-LTF (HBV/HDV) 和 REP 401 (HBV) 研究中,分析了HBsAg亞型在HBsAg定量下降(qHBsAg)期間和後續無治療隨訪期間的變化。
使用Abbott Research Use Only方法,分析冷凍血清樣本中的HBsAg亞型(大 [L]、中 [M] 和總 [T])。透過 T-HBsAg 與 M-HBsAg 的比率隨時間的變化推斷出小 HBsAg 相對於其他同種型隨時間的相對變化。所有參與者HBsAg亞型隨qHBsAg下降而下降。在任何功能性治癒的參與者中,均未檢測到HBsAg亞型。42 名參與者中有 39 名 HBsAg 從基線下降 > 2 log10 IU/ml 與選擇性清除 S-HBsAg 相關。

可見在基於NAP的組合療法期間 HBsAg (S-HBsAg) 的選擇性下降
HBsAg從基線下降 < 2 log10 IU/ml 的 10 名參與者中有 9 名沒有選擇性 S-HBsAg 下降。在隨訪期間,qHBsAg輕度反彈<10 IU/ml,主要表現為S-HBsAg和M-HBsAg,不伴有顯著的共價閉合環狀DNA活性。

治療期間選擇性 S-HBsAg 清除與 qHBsAg 反應之間的相關性
由Replicor公司與雅培診斷等科研人員聯合開展的這些研究結論是:我們觀察到 S-HBsAg 下降更快,這說明乙肝病毒的亞病毒顆粒已經從迴圈中被選擇性清除,這和之前對核酸聚合物作用機制描述是一致的。在沒有HBVDNA的情況下,觀察到微量的乙肝表面抗原反彈,這可能反映出這些乙肝表面抗原來自整合的HBVDNA,而不是病毒感染的反彈導致的。
相信當您能夠耐心地看到這裡,已對本研究結果有一定理解,這些研究結論也和最近Replicor公司的Andrew Vaillant博士(NAP技術發現者)描述的,成功確認NAPs對乙肝病毒的亞病毒顆粒(SVP)靶向作用結論一致。本研究使用到的NAP是在研乙肝新藥REP2139。