文|陳根
近年來,外泌體被廣泛用於探索治療人類疾病,在藥物遞送領域表現出巨大潛力。如果將細胞比喻為生產生物分子的工廠,那麼外泌體就是攜帶這些分子的運載器,它們能夠直接進入受體細胞內部,釋放所攜帶的物質,進而影響受體細胞。
2020 年 6 月,禮來(Eli Lilly)、武田製藥(Takeda)、拜耳(Bayer)等國際大型製藥公司涉及外泌體公司的交易逾 10 億美元。近年來,專注開發基於外泌體載體的腫瘤藥物靶向治療和基因治療的新公司不斷產生。這也從側面證明,業界看好外泌體發展。
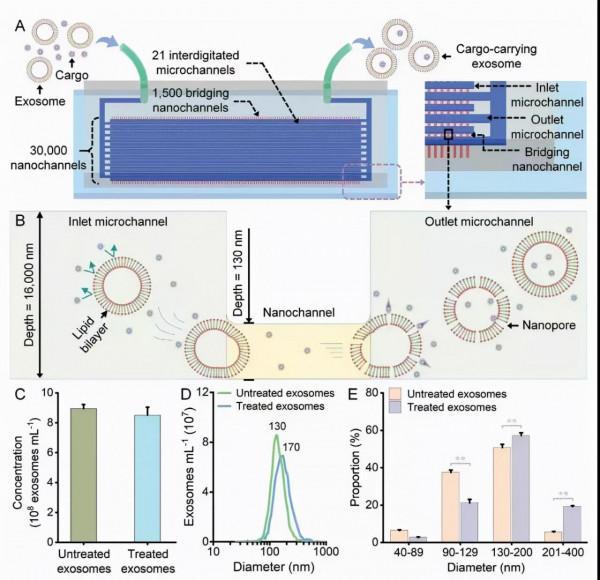
傳統方法中,如果想將外源物質裝載到外泌體中,裝載效率往往過低,且極易破壞外泌體完整性和功能性,這讓外泌體在生物醫藥應用上面臨重大挑戰。為了解決這一問題,中國科學院深圳先進技術研究院的科學家們研發了一種奈米流控晶片技術,實現了外泌體藥物載體的高通量製備。
該方案藉助了微奈米流體技術,實現了 3 萬個並行工作的模組。透過對外泌體的囊膜直接施加機械擠壓力和流體側向剪下力的“雙重作用”,在外泌體的膜表面產生短暫存在、不破壞生物膜結構的奈米孔。
該外泌體的直徑大約為30~200奈米,作為一種天然的細胞間物質載體,可以分泌到細胞外空間或體液,並透過生物分子的轉移和傳遞,來實現細胞間的通訊。此外,該方法可將多種外源物質裝載到外泌體中,並獲得大量裝有藥物的無損傷外泌體樣品。
實驗結果表明,這個新型奈米流控晶片,確保了含藥外泌體的活性,同時架起了對抗癌細胞、腫瘤細胞等的‘直擊通道’,在不產生免疫反應的情況下釋放內含藥物,提供了外泌體藥物臨床應用的重要前提。
值得一提的是,該方法無需引入任何會破壞外泌體或被裝載物質的因素,能夠高效地保持藥物或其他生物分子的功能性,可以在不破壞物質本來特性的基礎上,實現高效裝載。
未來,科學家們預期在2 年內實現標準化生產並發展成為平臺型工具,為生物學和臨床醫學研究、疾病的早期診斷和精準治療開闢新機會。