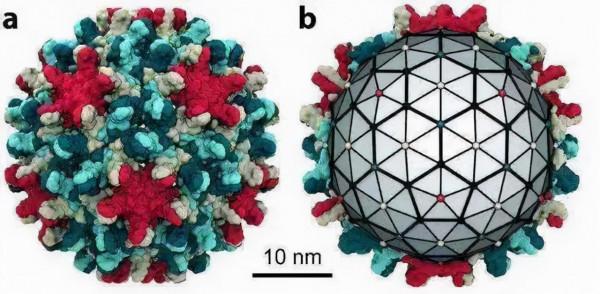
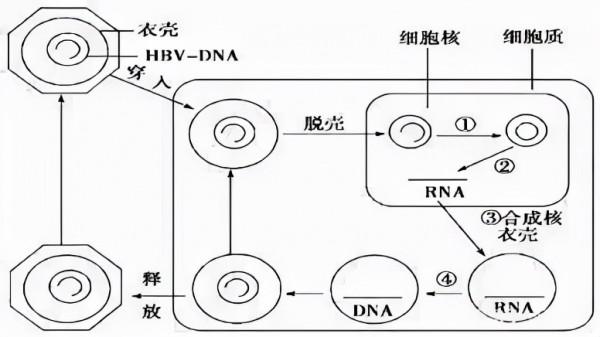
乙肝病毒的核心蛋白,是開發慢乙肝新藥有相當吸引力的靶點。由於核心蛋白參與到乙肝病毒的基本步驟,開發此類化合物可以透過干擾其自身的組裝來抑制病毒複製。最近幾年中,我們也看到全球科研人員正在朝著這個方向來推動衣殼組裝調節劑(CAM)進入臨床試驗。
乙肝在研新藥有吸引力靶點,衣殼組裝調節劑CAM,又分為兩大類
一、CAM的作用機理和代表藥物
現有的CAM分子,可以分成兩大類,I類是雜芳基二氫嘧啶(HAP),如GLS4、RO7049389等,這一類CAM的作用機理是誘導非衣殼聚合物或核心蛋白大聚體形成;II類是苯丙烯醯胺 (PPA) ,以AB-423比較有代表性,這一類的作用機理是產生沒有pgRNA的空衣殼。這兩類CAM在二聚體-二聚體的介面和相同的疏水口袋結合,並能夠引導核心蛋白錯誤地組裝,最後阻止感染性的子代病毒粒子形成。
CAM,是目前開發新的乙肝抗病毒在研新藥方向之一,相關化合物都在開發當中,開發目標也是指向功能性治癒HBV。功能性治癒需要滿足乙肝表面抗原(HBsAg)和或e抗原(HBeAg)血清學轉換,並實現HBVDNA/RNA檢測不到(陰轉),讓慢乙肝患者不需要終身給藥。HBV生命週期中的多個步驟,都有利於開發新靶點,HBV核心蛋白就是其中之一。
除HBV核心蛋白外,還有Toll樣受體(TLR)7/8激動劑,這種方法主要目的是刺激先天免疫反應;還有 HBV 特異性 siRNA 降解病毒 mRNA、使用成簇的規則間隔短迴文重複序列 (CRISPR)/Cas9 系統清除共價閉合環狀 DNA (cccDNA)、中斷HBV X蛋白(HBx)損傷特異性之間的相互作用DNA 結合蛋白 1 (DDB1)等。
二、CAM未來開發方向
乙肝衣殼組裝調節劑是一個總稱,主要包括雜芳基二氫嘧啶(HAP)、苯丙烯醯胺 (PPA) 、氨磺醯苯甲醯胺 (SBAs) 。組合療法在慢乙肝新藥開發過程中,已經扮演重要角色,因為聯合不同作用機理的在研乙肝新藥或聯合核苷(酸)類似物(NAs)有助於抑制HBV生命週期中的多個步驟。
三、CAM中,代表藥物GLS4以往已公佈進展
GLS4(甲磺酸莫非賽定)由我國東陽光藥自主研發,是一種全球有代表性的HBV衣殼組裝調節劑。它屬於二氫嘧啶 I 類 CAM,能夠干擾乙肝病毒的核心蛋白組裝。根據小番健康以往釋出的GLS4 在歐洲肝臟大會上的進展,在我國進行的1b期隨機、單中心、開放標籤研究中,旨在評價GLS4+利托那韋聯合用藥的耐受性、抗病毒活性和藥代動力學(PK)特徵。
結果表明,在GLS4新增利托那韋(CYP3A4 抑制劑)後,可提高人體GLS4的血清濃度;A佇列和B佇列的HBVDNA平均減少1.42 和 2.13 log IU/mL,乙肝表面抗原平均減少 0.06 和 0.14 log IU/mL,pgRNA 平均減少 0.75 和 1.78 log 複製/mL,乙肝核心抗原分別平均減少 0.23 和 0.5 log U/mL(試驗資料已發表在相關學術期刊)。
小番健康結語:在全球乙肝在研新藥物靶點中,衣殼組裝調節劑無疑已經得到許多科研人員肯定其未來開發潛力。比較經典的CAM如雜芳基二氫嘧啶,相對應的化合物多數都已經進入臨床1期或2期研究中。
衣殼組裝調節劑還有一個特點是,該類化合物正在和已獲批核苷類藥物或其他免疫刺激候選藥物聯用。除了我國正在開發的甲磺酸莫非賽定之外,全球還有許多同類靶點在研新藥,比如RO7049389(羅氏公司、2期、I類CAM)、VBR(以往名ABI-H7031、Assembly Bio公司、II類CAM、2期)等等,後面小番健康會介紹它們之間的區別的研發進展。