普納替尼(Ponatinib)是第三代酪氨酸激酶抑制劑(TKI),適用於耐藥或不耐受慢性期(CP)、加速期(AP)或急變期(BP)的慢性髓系白血病(CML)患者、費城染色體陽性急性淋巴細胞白血病(Ph+ ALL)或T315I突變的患者。今天,小編整理了3篇2021 ASH年會中有關普納替尼治療CML患者的研究進展,供讀者參考。
摘要號:307
OPTIC試驗中基線BCR-ABL1水平和突變狀態對慢性髓系白血病慢性期(CML-CP)患者使用普納替尼後療效影響的事後分析
OPTIC(Optimizing Ponatinib Treatment in CP-CML, NCT02467270; ongoing)是一項Ⅱ期試驗,評估了普納替尼在對≥2種TKI耐藥或有T315I突變的CP-CML患者中的安全性和有效性。
研究方法
對≥2種TKI耐藥或具有BCR-ABL1T315I突變的CML-CP患者被隨機分配至普納替尼起始劑量為45mg/天(A組,45 mg→15 mg)、30mg/天(B組,30 mg→15 mg)和15mg/天(C組)三組中接受治療。在佇列A和B中達到≤1%BCR-ABL1IS後,劑量減至15mg。患者可能會因治療無反應而重新加量至起始劑量。
主要終點是BCR-ABL1IS≤1%持續12個月;次要終點包括細胞遺傳學和分子學反應以及安全性結果。在該分析中,透過對受試者的基線T315I突變狀態和基線疾病負擔進行分析得出結果。BCR-ABL1突變在中心實驗室(MolecularMD, Portland, OR, USA)透過Sanger測序進行評估。
研究結果
283例患者被隨機分組(A/B/C:n=94/94/94)。基線時,84.1%的患者有較高的疾病負擔(BCR-ABL1IS≥10%),23.8%有T3151突變,17.0%有除T3151外的突變,57.8%無突變。
OPTIC事後分析顯示,三種給藥劑量都可以減輕耐藥患者的疾病負擔。其中無論基線BCR-ABL1IS水平如何,45 mg→15 mg劑量組在36個月時BCR-ABL1IS顯示出最高的≤1%BCR-ABL1IS反應率。無論基因突變的狀態或型別,該組患者≤1%BCR-ABL1IS反應率最高,為54%-60%。
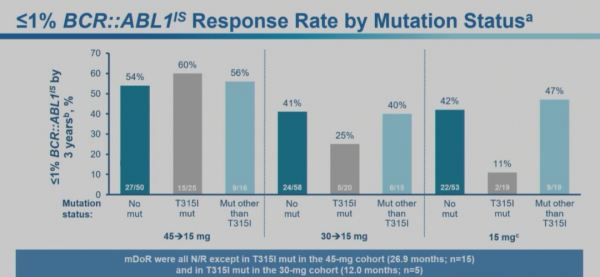
無論突變狀態如何,接受普納替尼治療的患者均表現出良好的生存結果。伴有T315I突變的患者在給藥劑量45mg→15mg時,患者的無進展生存期(PFS)顯著優於其他組。除T315I突變外,其他基因突變的患者也實現了長期PFS和總生存期(OS)。

三個劑量組在治療期間不良反應(TEAE)和治療時動脈閉塞事件(TE-AOE)方面沒有顯著差異。最常見的非血液學TEAE是高血壓(28%)、頭痛(18%)和脂肪酶增加(17%)。最常見的血液學TEAE是血小板減少(40%)、中性粒細胞減少(26%)和貧血(19%)。總體而言,6.0%的患者治療時經歷了TE-AOE,4.6%的患者經歷了≥3級的TE-AOE。
研究結論
既往分析證實,這些耐藥患者在接受普納替尼治療時獲得了較高的緩解率。與此一致的是,OPTIC事後分析顯示,無論基線時T3151突變狀態如何,患者從3種給藥方案均可獲益。無論基線疾病負擔如何,根據BCR-ABL1IS水平評估,A組顯示了最高的緩解率。
摘要號:3603
普納替尼在義大利CML患者中的多中心、前瞻性和回顧性觀察佇列研究:OITI試驗的初步分析
來自義大利的一項使用普納替尼治療CML患者的觀察性研究(OITI)旨在評估自普納替尼批准以來在義大利治療的CML患者的治療模式和結果,包括藥物安全性和有效性。
研究方法
OITI是一項非介入佇列研究,納入了來自義大利26箇中心,臨床常規治療中開始使用普納替尼的≥18歲確診為慢性期、加速期或急變期的患者。研究人群包括:一組為前瞻性佇列,包括在試驗啟動後12個月入組期內,開始接受的普納替尼治療的患者;一組為回顧性佇列,包括接受普納替尼治療但在試驗啟動前死亡或隨訪失敗的患者;一組為回顧性/前瞻性佇列,包括試驗啟動前已開始接受普納替尼治療,並在試驗結束時仍在治療或隨訪的患者。在研究開始時和常規護理訪問時,從患者的病歷中收集人口統計學、有效性和安全性資料。從第一個患者入組開始,研究持續時間為48個月,觀察期在最後一個患者入組後24個月結束。
主要終點是CML-CP患者開始普納替尼治療6個月後完全細胞遺傳學反應(CCyR)率。在缺乏細胞遺傳學評價的情況下,使用分子學評價,分子學反應(MR)為2.0或更好的患者被認為有CCyR。主要次要終點為主要分子學應答(MMR;MR3.0)、深度分子學反應(DMR;MR4.0和MR4.5)以及安全性。本文對主要終點(中位隨訪時間23.7個月[1.3-70.8])的所有可評估患者進行了初步分析。
研究結果
研究共納入119例患者(110例CML-CP,6例CML-AP、3例CML-BP)。59例(49.6%)患者在二線治療使用普納替尼,41例(34.4%)患者在三線治療,19例(16.0%)患者在四線治療或是更晚使用。改用普納替尼治療的原因多為不良事件(AE)或耐藥。
普納替尼的起始劑量為45mg(37.0%)、30mg(41.2%)或15mg(21.8%)。中位治療持續時間為22.8個月(範圍1.4–73.6個月)。研究期間共有178次劑量調整,多數因為AE和醫生決策。
除1例患者的基線資料不可用,在6個月時,80/107例(74.8%)可評估的CML-CP患者處於CCyR,29/56例(51.8%)達到CCyR,50/50(100%)維持CCyR;在6個月時,56例(52.3%)和13例(12.1%)CML-CP患者分別實現了MMR(MR3)和DMR(MR4-MR5)。CML-CP患者PFS率和OS率結果如下圖。

71例(59.7%)患者出現治療相關不良事件(TRAE),最常見的是皮疹、高血壓(1-2級)和血小板減少(3級)。2例(1.7%)患者發生了治療相關的動脈閉塞。77例患者停止使用普納替尼,主要原因為AE(33.3%)、醫生決策(24.2%)和其他原因(42.4%),如死亡、疾病進展和造血幹細胞移植。
研究結論
這項觀察性研究表明,在義大利的標準臨床實踐中,普納替尼在CML患者中具有良好的有效性和安全性。6個月後,74.8%的可評估的CP-CML患者達到CCyR,52.3%和17.8%分別達到MMR(MR3)和DMR(MR4-MR5)。2年生存率為>88%,未出現既往未報道的安全訊號。早期用藥(84%患者作為二線、三線的治療)和謹慎的劑量選擇似乎是這項真實世界研究中觀察到的安全性和有效性結果的關鍵。
摘要號:312
普納替尼聯合FLAG-IDA治療慢性髓系白血病急變期:英國試驗加速計劃(TAP)無縫I/II期劑量探索試驗的最終結果
CML-BP患者的預後極差,異基因幹細胞移植(alloSCT)是唯一的治癒方式。更重要的是,移植後是否能長期生存取決於能否透過挽救性治療恢復到慢性階段。因此,需要新的治療方案來改善反應及移植結果。在TKI時代,CML-BP已經較為罕見。因此,很少有指導臨床實踐所需的前瞻性試驗。此研究報道了前瞻性試驗的最終結果,該試驗使用創新的EffTox設計來研究TKI普納替尼與高劑量化療聯合應用的療效和耐受性,以改善CML-BP患者的緩解狀態和移植結局。
研究方法
英國TAP在2015年3月至2018年4月期間招募了17例患者參與這一探索劑量的無縫式I/II期試驗,該試驗每日使用普納替尼聯合氟達拉濱、阿糖胞苷、粒細胞集落刺激因子和伊達比星(PON-FLAG-IDA)挽救治療。研究者採用了一種先進的貝葉斯方法EffTox,同時考慮所有患者的療效和劑量限制毒性(DLT),提供了臨床效用的單一衡量標準,為後續的劑量建議提供了參考。主要目的是根據EffTox模型確定普納替尼聯合化療的有效和耐受劑量。主要結果是達到第二慢性期和達到DLT。次要結果是探索療效、安全性、生存率和移植結果。
研究結果
17例患者中9例完成了一個週期的PON-FLAG-IDA治療,8例完成了兩個週期的治療。使用EffTox分析後,確定普納替尼的最佳劑量為30mg/天。11例患者恢復到慢性期,4例患者經歷了DLT,符合預先指定的臨床療效和毒性標準。經PON-FLAG-IDA挽救性治療後,8例患者獲得CCyR,5例患者獲得MMR。
12例患者進行了alloSCT,其中5例在1個週期的PON-FLAG-IDA治療後進行移植,7例是在2個週期後進行移植。其中3例患者死亡,3例患者復發。所有患者的中位OS為12個月(95%CI:6-NR),接受alloSCT的患者的中位OS尚未達到。

常見的3-4級血液學AE為嗜中性粒細胞減少(71%)、血小板減少(65%)、貧血(41%)和白細胞減少(41%)。常見DLT為心肌病、腦靜脈竇血栓形成、澱粉酶升高、谷丙轉氨酶(ALT)升高。3例患者出現了治療相關死亡。
研究結論
相關試驗表明,普納替尼與大劑量化療聯合使用具有一定的安全性,以使CML-BP患者從急變期恢復到慢性期,是這一高危人群的新治療策略。隨後患者接受alloSCT治療可實現長期無病生存。EffTox方法能夠有效地利用這一高風險患者群體的資料,是研究其他罕見癌症新療法的模型。
參考文獻:
[1]2021ASH.Abstract#307.
[2]2021ASH.Abstract#3603.
[3]2021ASH.Abstract#312.