在您的科研生涯的某個時候,都有可能會用到熒光顯微鏡。這種無處不在的技術改變了顯微鏡學家對研究物件進行成像、標記和追蹤的方式,不論是整個生物體,還是單個蛋白質等等。
透過本文,我們將探討什麼是“熒光”,包括其定義背後的歷史和基礎物理原理,綠色熒光蛋白(GFP)的發現和應用,並展望量子點等熒光探針不斷擴大的應用領域。
我們如何定義“熒光”?
在任何搜尋引擎中輸入“熒光的定義”,你會得到以下語句,或者非常相似的內容;
“由較短波長的入射輻射,如X射線或紫外線,某些物質會發出可見或不可見的輻射。”
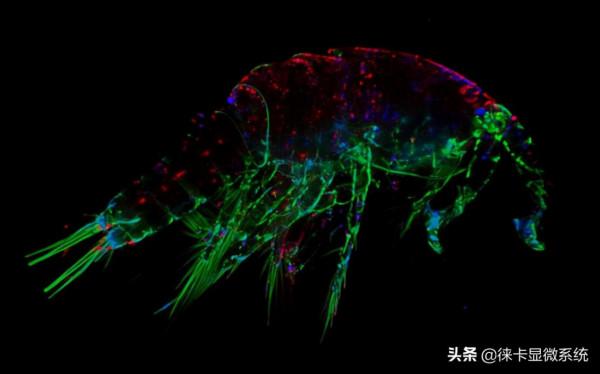
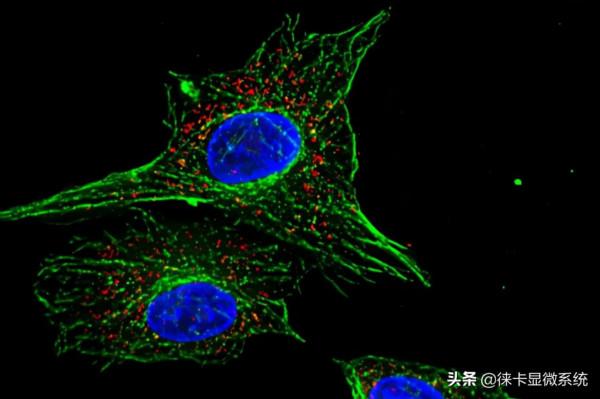
這個定義與熒光顯微鏡(圖1)有何關聯呢?“波長較短的入射輻射”只是用來“激發”樣品發射熒光的光源。這種光線包括可見光、紫外線(UV)和紅外線(IR),顯微鏡的光源可以是汞或氙弧光燈,也可以是鐳射。熒光基團(即上述定義中的“某些物質”)是具有特殊性質的化合物,它們在較短波長光線的激發下,可以再次發射較高波長的光線/光子。
圖1:熒光顯微鏡下顯示的熒游標記細胞。
波長的基本單位是米,“波長”定義為光波的兩個連續波峰或波谷之間的距離。波長的符號是希臘字母λ(l)。顯微鏡使用的波長通常以奈米(nm)為單位,可見光譜段在400至700奈米之間,紫外光譜段在400奈米以下,紅外光譜段從700奈米開始(圖2)。
圖2:可見光光譜
熒光基團按其激發和發射波長分類,通常以圖形的形式顯示最大波峰。熒光基團在所謂的“基態”中自然穩定。它們吸收到(來自“較短波長”入射光的)光子時,光子的能量將熒光基團的電子提升到更高能量的“激發”狀態。被激發的電子不會保持在這種狀態,而會失去振動能量,並在返回基態時發射出一個較長波長的光子。對於顯微鏡使用熒光基團,從激發到返回基態的一個完整週期需要0.5到20納秒。
熒光基團的激發和發射波長通常縮寫為希臘字母lambda,加上下標“ex”(激發)或“em”(發射;即lex或lem)。
每個熒光基團都有一個不同的最大激發和發射譜段,這一特性用來區分同一樣品中的不同標靶。例如,使用熒光染色劑DAPI(4',6-二脒基-2-苯基吲哚)高亮顯示細胞中的核蛋白,同時使用熒游標記的鬼筆環肽來高亮顯示肌動蛋白細胞骨架。
熒光的雅布隆斯基圖
波蘭物理學家亞歷山大·雅布隆斯基(Aleksander Jablonski,1898-1980)首先用三能級能量圖描述了基態/激發/發射之間的迴圈,因此稱為“雅布隆斯基圖”。 1930年,他憑藉題為《關於激發光波長變化對熒光光譜的影響》的論文獲得華沙大學博士學位。1933年,他在《自然》雜誌上發表了自己的論文(《染料中反斯托克斯熒光的效率》”),其中含有雅布隆斯基圖。這種簡單而有效的示意圖清晰表現出熒光基團從基態到激發態的激發行為,然後在發射較長波長光子後回到基態(圖3)。
圖3:熒光雅布隆斯基圖。熒光基團會吸收光子。光子的能量將熒光基團的電子提升到更高能量的“激發”狀態。隨後,激發的電子失去振動能量,並在返回基態時發射一個較長波長的光子。
雖然圖3是簡化版的雅布隆斯基圖,但應該可以注意到,熒光基團可以存在多個不同的激發和發射狀態。此外,熒光基團可以透過不同的弛豫狀態返回基態,這些弛豫狀態被稱為“三重態”,具體取決於分子的電子自旋。
斯托克斯位移
喬治·加布裡埃爾·斯托克斯爵士(1819-1903)是愛爾蘭數學家和物理學家,他一生中在光學和光線領域頗有建樹。1849年他受命擔任劍橋彭布羅克學院的盧卡斯數學教授,並一直擔任該職務,直到1903年去世。他寫了一篇文筆優美的描述性論文,發表於1852年,名為《論光的折射性的變化》[1]。他在論文中使用的語言不同於我們在現代科學文獻中使用的語言。以下是斯托克斯爵士所用精彩語言的兩段簡短摘錄;
“去年深秋,雖然因為節氣遲來,觀察機會不多,我從不同渠道得知,之前提到過的那種具有高內色散性的黃色玻璃採用氧化鈾染色。”
以及:
“看到試管在浸入不可見光線的瞬間點亮,這當然是一個奇怪的景象:那實際上是可見的黑暗。總的來說,這種現象有點不可思議。”
“斯托克斯位移”這詞就是為了紀念這位科學家。當激發的電子回到基態併發出光子時,其波長始終大於激發熒光基團的入射光線的波長。這是由於光的特性,即波長與輻射能量成反比。斯托克斯位移描述了熒光基團的峰值激發波長和峰值發射波長之間的差值(以奈米為單位)(圖4)。
圖4:斯托克斯位移發射光的波長始終大於用來激發熒光基團的光線波長。
增加斯托克斯位移,熒光基團的激發光和發射光之間區別就越明顯。熒光基團的電子排布和分子結構令其在斯托克斯位移方面有著獨特的性質。
綠色熒光蛋白的發現與應用
斯托克斯爵士首先使用“熒光”這個術語來描述他觀察到的現象,但其發現可以追溯到1565年。來自西班牙的醫生兼植物學家尼古拉斯·莫納德斯(Nicolas Monardes)描述了一種墨西哥樹(Lignum nephriticum),其木頭被注入了奇怪的藍色。儘管有這些早期的觀察,但直到約400年後,人們才在活體組織中找到一種綠色熒光物質。1955年,Davenport和Nicol發表論文[2],描述了一種在稱為水螅水母(Hydromedusae)的水母亞綱生物的嗜酸性粒細胞中找到的發光組織。當時,兩位論文作者並沒有意識到這些嗜酸性粒細胞含有綠色熒光蛋白(GFP)。
直到1962年,下村脩(Osamu Shimomura,出生於1928)發表了一篇論文[3],認定這種發光成分是一種蛋白質。透過與他在普林斯頓大學的老師(弗蘭克·約翰遜教授)合作,他們從生物發光水母Aequorea Victoria(維多利亞多管發光水母)身上收集到樣本。他們用一種獨特的方法從水母中分離出熒光蛋白,即透過棉布袋擠壓分離的生物發光組織,產生一種被下村稱為“擠壓物”的溶液。
1994年,哥倫比亞大學的馬丁·查爾菲(Martin Chalfie,出生於1947年)教授發表論文,證明了基因編碼GFP可以在原核細胞和真核細胞(即大腸桿菌和秀麗隱杆線蟲的神經元)中實現功能表達[4]。該論文寫道“由於這種熒光不需要外源底物和輔助因子,GFP表達可以用於監測生物體內的基因表達和蛋白質定位。”正是這篇文章的發表為GFP在生物學研究中的廣泛應用鋪平了道路。
圖5:線蟲,GFP在神經系統中的表達。
一年後,一直在研究野生型GFP突變體的加州大學聖迭戈分校教授錢永健(1952-2016)在《自然》的科學通訊上發表了自己的論文[5]。錢教授和他的同事發現,他們選擇的一個單點突變(S65T)具有最長的激發和發射波長(490/510nm),這令它更具有光穩定性,並帶來眾所周知的GFP激發/發射峰。
2008年,下村脩、錢永健和查爾菲因在GFP的發現和應用方面發揮的重要作用共同獲得諾貝爾化學獎。下村脩在他的諾貝爾演講中表示,“當我在1979年發現GFP的髮色團時,我認為自己已經完成了所有研究工作,因而決定終止我在GFP方面的工作,以便集中精力研究生物發光”。他接著承認,“GFP是一種美麗的蛋白質,但在發現之後的30年中,它依然百無一用。”
自從錢永健發現GFP的應用之後,他的實驗室已經設計出多種GFP變體,涵蓋了大部分的可見光譜,並徹底改變了光學顯微鏡和成像領域。得益於這種基因工程,GFP的色彩範圍從光譜的藍色譜段(EBFP;380/460奈米)到光譜的黃色譜段(YFP;514/527奈米)。
報告基因和探針
除了成像領域,熒光團可以作為研究細胞和生物體中基因表達的“報告基因”。熒光素酶以及基因編碼GFP,就是檢查細胞是否表達特定基因的常用報告基因。生物體或細胞被基因改造的病毒DNA或質粒轉染,當目標基因獲得表達時,這些質粒會發出熒光。細胞內部的相關細胞器或位點可以在受轉染的細胞中進行觀察和檢查。
利用熒光基團標記(或“標註”)的抗體通常稱為“熒光探針”。在GFP和其他熒光基團得到廣泛應用之前,兩種最常用的熒光基團標記抗體是FITC(異硫氰酸熒光素)和TRITC(異硫氰酸四甲基羅丹明)。儘管FITC和TRITC仍在使用,但該領域已取得重大進展,至少可以說,熒光基團和探針的選擇非常廣泛。
當然,如今實驗室中使用最為廣泛的熒光基團之一是“Alexa Fluor”染色劑。目前Alexa Fluor染色劑的可用色彩範圍已超越可見光譜,其中激發波長範圍可達346至784奈米。
量子點
1981年,俄羅斯科學家阿列克謝·埃基莫夫(Alexey Ekimov)在聖彼得堡瓦維洛夫國立光學研究所工作時,首次在玻璃基質中發現了量子點。然而,在新澤西州AT&T貝爾實驗室從事半導體工作的路易斯·布魯斯(Louis Brus)首先發現了量子點膠體溶液。他現在是哥倫比亞大學化學系教授。在1983年和1984年發表的兩篇論文中,布魯斯將量子點描述為“小型半導體微晶”。
量子點有著奇特的行為方式,儘管它們包含100到10萬個原子,但它們表現出的性質就像它們由單個原子組成一樣。當然,它們確實符合熒光基團的性質,即它們可以吸收光能並激發,然後在返回基態時釋放光子。不過,量子點發射光線的波長取決於量子點的大小,即量子點越小,發射波長就越短。這種特性是因為較小的量子點具有較大的“最小帶隙”。這正是激發電子到更高能態所需的能量。由於較小的量子點需要更多的激發能量,它們隨後會發射較短波長的光(波長與激發能量成反比)。
大約20年後,即2002年,加州量子點公司的生命科學研究人員實現了量子點的商用開發。
量子點是一種非常明亮且穩定的熒光工具。研究表明,量子點的的亮度比傳統熒光基團高几個數量級,儘管與有機染料相比,量子點的明亮程度存在一些差異[6]。就光穩定性而言,量子點的穩定性是傳統熒光基團的100倍,在一項活體成像研究中,量子點的熒光持續時間長達4個月[7]。
在傳統熒光探針中,一個或多個熒光基團可以附著在單個相關抗體上。然而,由於量子點的表面積非常大,許多分子和抗體可以附著在單個量子點上,這會帶來許多優點,包括熒光訊號放大。量子點的使用也為多重分析提供了優勢,可以在檢測中同時對各種波長進行成像。在這種分析中,唯一的變數是研究者選擇的量子點大小(因此發射波長)。可以使用白光同時激發大範圍的量子點,這樣就可以避免使用多道鐳射和多次調整來形成最終影像。