M*僅供醫學專業人士閱讀參考
如何持續管理患者心血管疾病風險、助力心血管疾病拐點早日到來是學術界不懈追求的目標。在近日舉辦的中華醫學會第二十三次全國心血管年會暨第十二屆海峽心血管病高峰論壇上,武漢大學人民醫院徐林教授對此進行了深入闡述。
單純干預LDL-C,
仍有60%-70%心血管殘餘風險
心腦血管疾病是“健康中國2030”的最大挑戰之一,徐林教授首先指出,4S、LIPID等他汀相關研究提示我們,他汀治療的普及雖然帶來了25%-35%心血管獲益,但平均高達70%的心血管疾病殘餘風險持續存在[1,2]。
進一步心血管風險控制的需求催動臨床關注非他汀類降脂藥物及新降脂靶標。
IMPROVE-IT研究[3]提示,即使急性冠脈綜合徵(ACS)患者經他汀及依折麥布治療後,低密度脂蛋白膽固醇(LDL-C)<70mg/dL、合併糖尿病或下肢動脈疾病(PAD)的患者7年主要不良心血管事件(MACE)發生率仍高達60%,提示僅干預LDL-C存在侷限性,即基線LDL-C越低,對其進行強化治療的獲益越小。需要注意的是,除LDL-C外,我們還需要關注其他的血脂目標。
心血管殘餘風險主要來自於致動脈硬化的顆粒,包括非高密度脂蛋白的主要成分和甘油三酯等。當甘油三酯大於1.2mmol/L(100mg/dL),富含甘油三酯的脂蛋白及其殘餘物就開始在血液中累積,加速動脈粥樣硬化程序,“潘多拉之盒”被開啟。
以甘油三酯為焦點,
ASCVD風險能降低嗎?
近年來已有多項研究對以甘油三酯為靶目標的心血管獲益進行了分析。
FIELD研究[4]提示非諾貝特沒有顯著降低冠狀動脈事件主要結局風險,ACCORD Lipid[5]研究發現與單用辛伐他汀相比,非諾貝特和辛伐他汀的聯合用藥並未降低致死性心血管事件、非致死性心肌梗死或非致死性卒中的發生率。
這些研究先後顯示的陰性結果,使得2016年美國食品與藥物管理局(FDA)宣佈撤銷他汀類藥物與煙酸緩釋劑、非諾貝特酸聯合用藥相關的此前批准[6]。此外,《2021歐洲心臟病學會(ESC)心血管疾病臨床實踐預防指南》[7]指出,貝特類藥物主要用於降低甘油三酯,偶爾用於增加高密度脂蛋白膽固醇(HDL-C),支援其減少心血管事件的證據有限,同時,鑑於支援他汀類藥物的有力證據,不推薦在心血管疾病的預防中常規使用貝特類藥物。
另一類ω-3脂肪酸製劑的相關結果則喜憂參半,僅有兩項使用大劑量、高純度二十碳五烯酸(EPA)的研究獲得陽性結果,其使用劑量分別為1800mg/d及4g/d,分別納入18645例和8179例受試者[8,9]。
但其他相關研究多顯示出ω-3脂肪酸製劑不能帶來心血管風險事件獲益的陰性結果。例如VITAL[10]研究納入25871例受試者,發現補充ω-3脂肪酸1g/d並未降低主要心血管不良事件(MACE)或癌症的發生率;OMEMI[11]研究納入了1027例受試者,其結果也顯示不能透過應用930mg EPA+660mg 二十二碳六烯酸(DHA)進一步降低心肌梗死患者心源性猝死和其他臨床事件的發生風險。
基於以上非一致性結果,2019年3月28日,歐洲藥品管理局(EMA)謹慎回顧研究之後,發表宣告撤回了含有ω-3脂肪酸製劑的降低心血管風險的適應證。
他汀+貝特聯合治療改善動脈粥樣硬化心血管疾病(ASCVD)的結局尚存爭議,是因為甘油三酯並非有效的ASCVD防治靶點嗎?
答案是不!
2021年9月,《2021歐洲動脈硬化學會(EAS)共識宣告:富含甘油三酯的脂蛋白及其殘餘物——代謝觀察、在ASCVD中的作用及新興治療策略》[12]指出,甘油三酯、富含甘油三酯的脂蛋白及其殘餘物水平升高與ASCVD存在因果關聯,同時也會增加LDL-C降低後的殘餘心血管風險。
KP REACH研究[13]結果提示,甘油三酯水平≥150mg/dL的一級預防患者的校正死亡風險較低(風險比0.91,95%CI 0.89-0.94),MACE風險較高(風險比1.14,95%CI 1.05-1.24)。甘油三酯水平≥150mg/dL的二級預防患者的校正死亡風險較低(風險比0.95,95%CI 0.92-0.97),MACE風險(風險比1.04,95%CI 1.05-1.24)較高。
由此可見,透過降低甘油三酯進一步降低患者心血管殘餘風險的思路並沒有錯。
循證證據提示,
IPE進一步降低殘餘心血管疾病風險
那麼透過調整血脂譜來降低心血管風險,我們有何新治療手段呢?
REDUCE-IT研究[8]提示,對於已經接受他汀治療、LDL-C水平在41~100mg/dl之間的高危/極高危患者,如果甘油三酯水平高(150~499mg/dl),則應用IPE治療可進一步顯著降低主要終點心血管死亡、非致死性心肌梗死、非致死性卒中、冠脈血運重建和不穩定心絞痛複合終點(5P-MACE)風險達25%(P<0.001),顯著降低關鍵次要終點心血管死亡、非致死性心肌梗死和非致死性卒中複合終點(3P-MACE)達26%(圖1)。
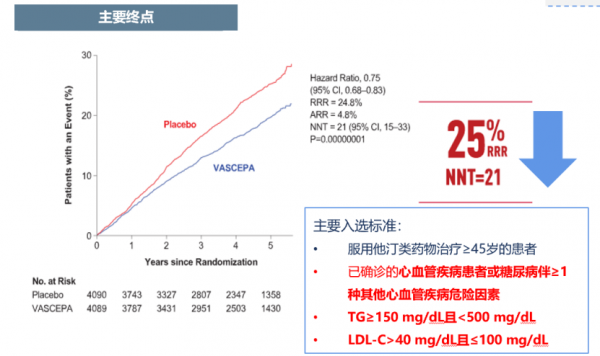
圖1 IPE治療進一步降低患者5P-MACE風險(注:TG,甘油三酯)
另一項JELIS研究[9]提示,應用大劑量高純度EPA(1800mg/d)可在一級及二級預防人群中顯著減少主要冠狀動脈事件達19%。
有理論[14]認為,根據目前不同的隨機對照試驗結果,在降低中度高甘油三酯血癥高危個體的ASCVD風險方面,高劑量IPE優於其他的製劑。需要指出的是,IPE不僅僅可以透過降低甘油三酯降低心血管風險,還可以透過減少炎症標誌物、膽固醇結晶形成、內皮功能障礙和各種含載脂蛋白B(ApoB)脂蛋白顆粒的氧化修飾,以及升高高密度脂蛋白等多種機制阻止動脈粥樣硬化進展中的各個步驟,發揮減少心血管事件作用。
總結
綜上所述,單純干預LDL-C,患者仍有60%-70%心血管殘餘風險,相關證據提示甘油三酯應成為ASCVD干預的新靶點,對於已啟動他汀治療的糖尿病患者更為如此。藥物選擇方面,高劑量IPE是在ASCVD一、二級預防中對心血管殘餘風險管理更值得期待的有效優選方案。
參考文獻:
[1]Randomised trial of cholesterol lowering in 4444 patients with coronary heart disease: the Scandinavian Simvastatin Survival Study (4S). Lancet. 1994; 344(8934): 1383-9.
[2]Long-Term Intervention with Pravastatin in Ischaemic Disease (LIPID) Study Group. Prevention of cardiovascular events and death with pravastatin in patients with coronary heart disease and a broad range of initial cholesterol levels. N Engl J Med. 1998; 339(19): 1349-57.
[3]Cannon CP, Blazing MA, Giugliano RP, et al. Ezetimibe Added to Statin Therapy after Acute Coronary Syndromes. N Engl J Med. 2015; 372(25): 2387-97.
[4]Keech A, Simes RJ, Barter P, et al. Effects of long-term fenofibrate therapy on cardiovascular events in 9795 people with type 2 diabetes mellitus (the FIELD study): randomised controlled trial. Lancet. 2005 Nov 26;366(9500):1849-61.
[5]ACCORD Study Group, Ginsberg HN, Elam MB, et al. Effects of combination lipid therapy in type 2 diabetes mellitus. N Engl J Med. 2010 Apr 29;362(17):1563-74.
[6]https://www.federalregister.gov/documents/2016/04/18/2016-08887/abbvie-inc-et-al-withdrawal-of-approval-of-indications-related-to-the-coadministration-with-statins.
[7]Visseren FLJ, Mach F, Smulders YM, et al. 2021 ESC Guidelines on cardiovascular disease prevention in clinical practice. Eur Heart J. 2021; 42(34): 3227-3337.
[8]Bhatt DL, Steg PG, Miller M, et al. Cardiovascular Risk Reduction with Icosapent Ethyl for Hypertriglyceridemia. N Engl J Med, 2019, 380(1):11-22.
[9]Oikawa S, Yokoyama M, Origasa H, et al. Suppressive effect of EPA on the incidence of coronary events in hypercholesterolemia with impaired glucose metabolism: Sub-analysis of the Japan EPA Lipid Intervention Study (JELIS). Atherosclerosis. 2009; 206(2): 535-9.
[10]Manson JE, Cook NR, Lee IM, et al. Marine n-3 Fatty Acids and Prevention of Cardiovascular Disease and Cancer. N Engl J Med. 2019 Jan 3;380(1):23-32. doi: 10.1056/NEJMoa1811403. Epub 2018 Nov 10. PMID: 30415637; PMCID: PMC6392053.
[11]Rauch B, Schiele R, Schneider S, et al. OMEGA, a randomized, placebo-controlled trial to test the effect of highly purified omega-3 fatty acids on top of modern guideline-adjusted therapy after myocardial infarction. Circulation. 2010; 122(21): 2152-9.
[12]Ginsberg HN, Packard CJ, Chapman MJ, et al. Triglyceride-rich lipoproteins and their remnants: metabolic insights, role in atherosclerotic cardiovascular disease, and emerging therapeutic strategies-a consensus statement from the European Atherosclerosis Society. Eur Heart J. 2021 Sep 2:ehab551.
[13]Ambrosy AP, Yang J, Sung SH, et al. Triglyceride Levels and Residual Risk of Atherosclerotic Cardiovascular Disease Events and Death in Adults Receiving Statin Therapy for Primary or Secondary Prevention: Insights From the KP REACH Study. J Am Heart Assoc. 2021; 10(20): e020377.
[14]Hernandez P, Passi N, Modarressi T, et al. Clinical Management of Hypertriglyceridemia in the Prevention of Cardiovascular Disease and Pancreatitis. Curr Atheroscler Rep. 2021; 23(11): 72.
僅供醫療衛生專業人士為了解資訊使用。該等資訊不能以任何方式取代專業的醫療指導,也不應被視為診療建議。如該等資訊被用於瞭解資訊以外的目的,本平臺及作者不承擔相關責任。
此文僅用於向醫療衛生專業人士提供科學資訊,不代表平臺立場
- End -

投稿/轉載/商務合作,請聯絡:[email protected]

















