摘要:
文題釋義:
細胞外囊泡:由細胞分泌或者從細胞膜上脫落的雙層膜結構囊泡狀小體,直徑從數十到數百奈米不等,主要由微囊泡和外泌體組成,攜帶與其細胞來源相關的多種蛋白質、脂類、核酸等,參與細胞間通訊、細胞遷移、血管新生和免疫調節等過程。
半數抑制濃度:即IC50,也稱半抑制濃度或半抑制率,指某物質能將細胞生長、病毒複製等抑制50%所需的濃度。
背景:中樞神經系統疾病往往與神經元凋亡密切相關。星形膠質細胞與神經元聯絡緊密,來源於星形膠質細胞特別是活化星形膠質細胞的細胞外囊泡能否抑制穀氨酸所致損傷神經元的凋亡,發揮神經保護作用,尚未見報道。
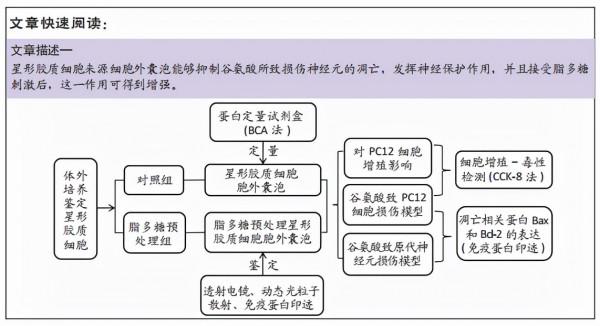
目的:探究星形膠質細胞胞外囊泡(astrocyte extracellular vesicles,AS-EVs)和脂多糖預處理的星形膠質細胞胞外囊泡(LPS-preconditioned astrocyte extracellular vesicles,LPAS-EVs)對穀氨酸誘導神經元損傷的作用及可能機制。
方法:體外培養星形膠質細胞,並利用脂多糖預處理建立誘導活化模型,收集上清,超離法提取細胞外囊泡並進行蛋白定量和鑑定。利用PC12細胞進行初步實驗,先探究AS-EVs及LPAS-EVs對PC12細胞增殖的影響,再建立穀氨酸誘導的PC12細胞和原代神經元損傷模型,實驗分4組:PBS組(與EVs組同體積的PBS處理24 h)、穀氨酸組(10 mmol/L穀氨酸處理24 h)、AS-EVs組(200 mg/L AS-EVs預處理24 h+10 mmol/L穀氨酸處理24 h)、LPAS-EVs組(200 mg/L LPAS-EVs預處理24 h+10 mmol/L穀氨酸處理24 h)。CCK-8法檢測PC12細胞存活率,Western blot檢測細胞凋亡相關蛋白Bax和Bcl-2表達。
結果與結論:①成功提取星形膠質細胞並建立脂多糖誘導的星形膠質細胞活化模型;②成功提取AS-EVs及LPAS-EVs,經鑑定符合細胞外囊泡形態學標準,相關標誌物表達陽性;③AS-EVs及LPAS-EVs對PC12細胞增殖無明顯影響;④與穀氨酸組相比,AS-EVs和LPAS-EVs能夠提高PC12細胞存活率,且LPAS-EVs作用強於AS-EVs(P均< 0.05,n=3);⑤AS-EVs和LPAS-EVs能夠抑制促凋亡蛋白Bax的表達,促進抗凋亡蛋白Bcl-2的表達(P均< 0.01,n=3),從而抑制PC12細胞和原代神經元凋亡,發揮神經保護作用,且LPAS-EVs的作用強於AS-EVs(P均< 0.05);⑥結果表明,星形膠質細胞所釋放的細胞外囊泡能夠抑制穀氨酸所致損傷神經元的凋亡,具有神經保護作用,並且在受到脂多糖刺激後,這種作用得到增強。
縮略語:星形膠質細胞胞外囊泡:astrocyte extracellular vesicles,AS-EVs;脂多糖預處理的星形膠質細胞胞外囊泡:LPS-preconditioned astrocyte extracellular vesicles,LPAS-EVs
https://orcid.org/0000-0002-3821-2995(孫海濤)
中國組織工程研究雜誌出版內容重點:幹細胞;骨髓幹細胞;造血幹細胞;脂肪幹細胞;腫瘤幹細胞;胚胎幹細胞;臍帶臍血幹細胞;幹細胞誘導;幹細胞分化;組織工程
關鍵詞: 星形膠質細胞, 細胞外囊泡, 脂多糖, PC12細胞, 神經元, 凋亡
引用本文: 孫海濤, 黃永輝, 龔愛華, 曹興兵, 李 震. 脂多糖預處理活化星形膠質細胞來源細胞外囊泡可保護神經元[J]. 中國組織工程研究, 2022, 26(13): 1985-1992.
閱讀更多請登入《中國組織工程研究》雜誌官網