2022年1月6日,南京艾美斐生物醫藥科技有限公司(以下簡稱“艾美斐醫藥”)CCR8拮抗劑IPG7236在美國完成首例受試者給藥,未見任何藥物相關的不良反應。IPG7236臨床I期(IPG7236-001 )是一項開放、多中心、劑量遞增及劑量拓展的臨床研究,旨在評價其單藥在晚期實體腫瘤患者的安全性、耐藥性、藥代動力學及初步療效。該專案臨床研究的首席科學家(PI)是來自於美國德克薩斯奧斯汀的Next Oncology的Dr. Andrae Vandross教授。
關於IPG7236
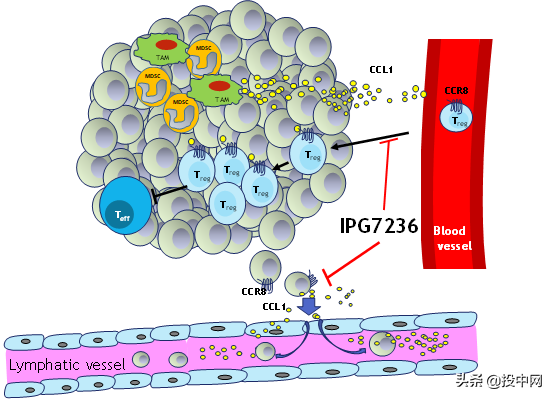
IPG7236由艾美斐醫藥自主研發,是全球第一款進入臨床研究階段的靶向趨化因子受體CCR8的小分子拮抗劑,於2021年8月正式獲得美國FDA臨床試驗批文,並於2021年12月初獲得中國國家藥監局臨床試驗批文。CCR8是腫瘤相關調節性T細胞(Treg)上高表達的一種趨化因子受體,其在非腫瘤相關的Treg上表達極低或不表達。CCR8也表達在多種腫瘤細胞上。IPG7236高效阻斷腫瘤相關Treg向腫瘤組織遷移,抑制Treg在腫瘤組織內擴增,並解除Treg對效應T細胞的抑制作用,增強腫瘤微環境中CD8+ T細胞的數量和活性,從而抑制腫瘤生長和轉移。另外,對於CCR8高表達的腫瘤細胞,IPG7236顯著抑制腫瘤轉移。臨床前研究表明,IPG7236顯著抑制多種腫瘤的生長(腫瘤抑制率超過70%),顯示其廣譜抗腫瘤活性,且與PD-1抗體藥協同增效,展現與免疫檢查點抑制劑聯合用藥的良好前景。艾美斐醫藥正在有序地準備II期臨床試驗,並不斷拓展其臨床適應症,加速該專案的研發上市速度,爭取早日造福患者。
關於艾美斐醫藥
艾美斐醫藥是一家處於臨床階段的新藥研發公司,由資深海歸醫學專家創立,核心管理團隊成員來自GSK、諾華等全球知名的跨國製藥公司以及哈佛大學、中科院等全球知名的學術機構。自2016年成立以來,公司致力於開發全球性創新藥,已實現包括南京、上海、悉尼、舊金山在內的全球化佈局。艾美斐醫藥的第一梯隊的專案中,除IPG7236已分別獲得美國FDA和中國CDE的臨床批件外,IPG1094也是全球第一款進入臨床試驗的MIF小分子抑制劑,已獲得5項中美兩國臨床批件,適應症為多發性骨髓瘤、實體腫瘤、多發性硬化症、系統性紅斑狼瘡、銀屑病。關於該藥的臨床適應症的拓展工作正在有序進行,預計2022年中旬將有多項新的適應症(包括ALS, AD等)獲批中美兩國IND。艾美斐醫藥已發展成為擁有小分子和大分子雙研發平臺,研發管線超過15條(全部是first-in-class),覆蓋腫瘤、自身免疫性疾病、神經退行性疾病等領域的創新藥研發公司。