環狀RNA(circRNA)作為表觀遺傳調控分子參與了腫瘤發生、惡性進展、免疫逃逸和耐藥等多種生物學過程。轉錄組測序資料顯示存在一類circRNA在腫瘤患者外周血中水平明顯升高,而在腫瘤組織樣本中表達卻明顯降低。 然而這種差異表達模式的機制和生物學意義仍不清楚。
2022年2月11日,浙江大學基礎醫學院病理學與病理生理學系張紅河/來茂德教授課題組在Molecular Cancer雜誌上線上發表了題為“Tumor-suppressive circRHOBTB3 is excreted out of cells via exosome to sustain colorectal cancer cell fitness”的研究論文。該研究不僅闡明瞭circRHOBTB3在結直腸癌中發揮抑癌作用的分子機制,而且提出腫瘤細胞能夠主動透過外泌體將具有抑癌作用的cirRNA分泌出胞外維持癌性的理論。此外,該研究還鑑定了circRHOBTB3環化和外泌體特異性分選的功能原件,採用ASO靶向環化和外泌體分泌調節元件增加腫瘤細胞內circRHOBTB3水平,達到抑制結直腸癌惡性進展的治療效應,為結直腸癌治療提供了一個新的干預策略。
該研究對公共資料庫中多種型別癌症患者的血漿外泌體中的circRNA水平進行了全面分析,結合臨床佇列的血清及組織樣本,發現circRHOBTB3在外周血中水平明顯升高,而在腫瘤組織樣本中表達卻明顯下降。
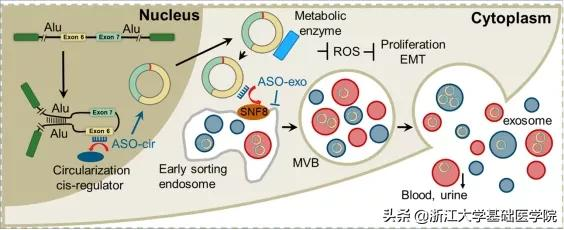
透過體內外實驗證明circRHOBTB3主要透過抑制代謝降低細胞內ROS水平從而抑制腫瘤細胞的進展和轉移。進一步發現ESCRT-II複合物的關鍵組分SNF8透過結合circRHOBTB3上特定的序列參與將circRHOBTB3分揀到外泌體中,透過外泌體將細胞內的circRHOBTB3排出以降低胞內circRHOBTB3水平。有趣的是,發揮促癌作用的環狀RNA並沒有被分選至外泌體排出胞外,而是被保留在腫瘤細胞內。
此外,我們還鑑定了調控circRHOBTB3環化的關鍵元件,並針對環化和外泌體分選的功能元件設計併合成了ASO,以增加circRHOBTB3的環化並阻斷circRHOBTB3外泌體的分泌;體外和體內試驗證實了這些ASO能夠增加結直腸癌細胞內circRHOBTB3水平抑制腫瘤細胞生長和轉移。
綜上,circRHOBTB3在結直腸癌中發揮作用,腫瘤細胞必須透過外泌體將其排出胞外以維持其癌性。透過針對環化和外泌體分泌提高腫瘤細胞內具有抑癌作用的circRHOBTB3水平的ASO可能會成為一種新的抗腫瘤策略。
浙江大學基礎醫學院張紅河教授和來茂德教授為論文的共同通訊作者,浙江大學基礎醫學院博士生陳超一、俞鴻飛和博士後韓豐豔為論文的共同第一作者。專案受到國家自然科學基金和中國醫學科學院醫學與健康科技創新工程專案資助。