撰文 | 望夜
責編 | 兮
每年全球仍有近200萬人感染人類免疫缺陷病毒(HIV-1),但目前尚無獲批的疫苗【1】。囊膜病毒入侵宿主由囊膜表面的糖蛋白介導,對HIV-1而言就是其Env蛋白,負責識別結合宿主細胞表面受體並完成膜融合過程,是中和抗體的唯一靶標,也是疫苗設計的主要靶蛋白。Env蛋白是由前體蛋白pg160切割成熟而來,含gp120和gp41兩個亞基,兩者由非共價鍵連線成異源二聚體進而組成Env同源三聚體,其中gp41可透過其跨膜區錨定在病毒囊膜上,C末端的胞漿結構域(CTD)位於病毒腔體內。在HIV-1出芽過程中,Env的CTD與未成熟的Gag蛋白的基質結構域(MA)互作,形成一個與膜結合的格柵(lattice),位於病毒雙層膜的內層。
為獲得均一穩定的Env三聚體結構,研究者此前透過在gp120和gp41間引入一對二硫鍵(SOS),同時將gp41 HR1螺旋上的異亮氨酸突變為脯氨酸(IP)的改造,構建出稱為SOSIP的Env三聚體,並基於此構建解析出一系列Env結構【2】。但由於SOSIP含有多處人為改造,是否可以真實反映天然狀態Env三聚體的結構,目前仍有許多未知。
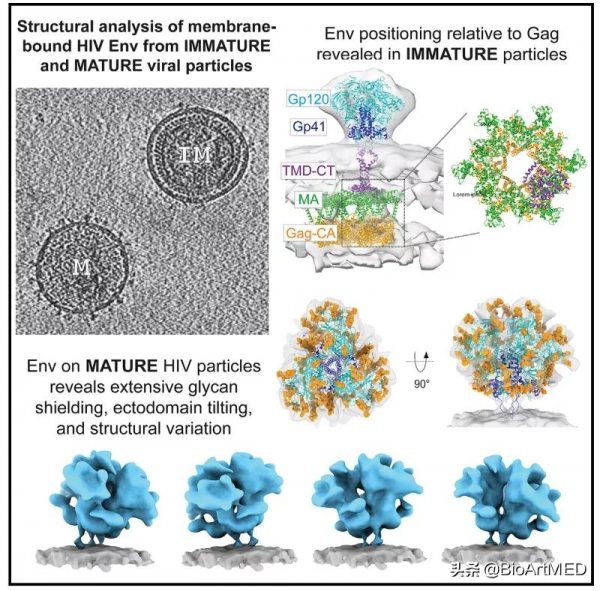
為分析在病毒顆粒表面的Env與其胞外可溶部分在結構上的差別,2022年2月4日,美國華盛頓大學的Kelly K. Lee和 Scripps研究所的Michael B. Zwick研究組合作在Cell上發表了文章Cryo-ET of Env on intact HIV virions reveals structural variation and positioning on the Gag lattice,藉助冷凍電子斷層成像(cryo-ET)技術,綜合子斷層掃描圖平均化(sub-tomogram averaging)和結構質譜技術分析了成熟和未成熟狀態下帶有Gag的HIV-1病毒樣顆粒結構,揭示出天然狀態下的HIV病毒顆粒結構的多變性。
在HIV-1病毒粒子表面,同時存在有功能但不穩定的Env三聚體及非天然狀態的Env蛋白。為克服Env蛋白的異質性和不穩定性問題,Michael B. Zwick組此前已透過直接進化獲得一系列Env蛋白變體【3】,本文使用的ADA.CM Env即來自B型分離株ADA的一個變種並截去其C端結構域(CTD)C末端的102個氨基酸。本研究使用稱為hVLP的病毒樣顆粒作為研究樣本,其帶有組裝在Gag蛋白層之外的雙層囊膜,而Gag的成熟需要經過酶切處理。hVLP含有與真實HIV-1顆粒相同的成分只是不具備複製能力,因為其包裹的病毒基因組缺乏Env基因,因而必須在表面表達有ADA.CM Env的HEK 293細胞中方能包裝出完整病毒顆粒【4】。純化後的hVLP還需經過一種溫和氧化劑二硫二吡啶-2(AT-2)的處理以破壞核衣殼與RNA的相互作用,確保顆粒不再具有感染性。抗體結合實驗顯示AT-2處理未影響Env蛋白的抗原性;儘管不具有感染性,AT-2處理的hVLP處理仍可誘導被感染細胞產生合胞體及細胞毒效應,表明Env依然具備介導病毒入侵的能力。利用此種表面Env蛋白密度較高的hVLP,作者收集到足夠的cryo-ET資料並最終處理獲得解析度9.1Å的HIV-1病毒粒子結構。
在獲得的結構資料中,大部分hVLP都處於成熟狀態,另有約3%的顆粒處於未成熟狀態,其囊膜下顯示出一層清晰規則的Gag格柵。對此部分子資料進行處理可獲得較低解析度的密度圖,但其Env結構非常接近由完整資料獲得的亞奈米解析度的Env結構及此前已發表的Env胞外域結構。可將已發表的Env胞外域和六聚體Gag-CA結構匹配到相應密度中,但Env TMD-CTD的密度未能出現在平均化後的結構中,表明跨膜區(TMD)未與Env胞外段或Gag-CA緊密連線。基於推測的TMD-CTD與Env胞外段的相對位置,可將前者結構匹配入密度圖中。
未成熟狀態Gag N端的MA結構域以同源三聚體的形式沿著病毒囊膜內層組裝成六聚體,MA透過一段柔性連線區與Gag-CA格柵層相連。在未成熟hVLP的斷層圖上可以清晰辨認出對應Gag-MA的規則排布的密點,就位於膜內層之下;但在平均後的密度圖中卻無法分辨出Gag-MA層的密度,作者推測Gag-MA格柵的排列可能相較於Gag-CA或Env的對稱軸存在微小的差別。於是只能基於Gag-MA相對於Gag-CA的推測位置,將MA格柵的結構匹配入密度圖中(圖1)。於是Env CTD與Gag-MA並排出現在膜內層底部,剛好與粗斷層圖吻合。而且在該複合模型中,Env CTD的相對位置剛好位於Gag-CA格柵邊沿的二次軸處,這就排除了此前研究中推測其位於中心孔的假設【5】。在此種構象下,Env CTD可以與MA上關鍵殘基發生直接相互作用,而這些殘基被認為是Env包裝所必需的。為進一步確認結構分析結果,作者還收集了帶有ADA.CM全長三聚體的未成熟hVLP冷凍電子斷層資料,分析顯示其中Gag多聚蛋白的組織形式與前述模型中相似,Env三聚體同樣位於Gag-CA格柵的邊沿而非中心孔處。
圖1 未成熟HIV-1病毒顆粒Env-Gag的複合模型
而在成熟病毒顆粒結構中,Gag多聚蛋白已被酶切開,MA層呈斷裂狀而非前述未成熟顆粒中的連續狀態,表明在病毒粒子成熟過程中MA結構需要發生重構。而且此時Env三聚體已不再與MA層位於同一位置。作者推測膜結合的Gag格柵的打斷可能有助於Env三聚體獲得足夠的移動能力以便於介導膜融合過程。
接下來重點分析Env三聚體的結構。作者發現hVLP-Env基本都處於閉合的融合前構象,其胞外段透過一個薄的三腳架樣莖環與病毒膜相連(圖2)。與未成熟hVLP中的Env結構類似,儘管可在粗斷層影象中確認其存在,此子斷層平均化結構中Env跨膜區的密度同樣不可見。在每個成熟的hVLP上分佈有不同數目的Env,數目介於8-82,這些三聚體似乎是隨機分佈的,無明顯的聚集或與其他三聚體形成緊密互作。hVLP基本都呈球狀構型,平均直接約100 nm,故大體估算出一個hVLP上最多可容納429個Env三聚體,因此hVLP上存在的Env三聚體數目遠低於其理論上限,這就使得每個Env三聚體有充足的表面區域供其移動。此外,作者還使用氫氘交換質譜(HDX-MS)分析天然hVLP上的Env,確認其處於閉合的融合前構象,且其構象是異質性的;同時透過比較可溶的BG505.SOSIP構建,發現兩者的整體構象類似,尤其是gp120亞基的組織形式,但hVLP-Env在結構上更加規則。
圖2 平均後的Env密度圖與匹配的結構模型側檢視
那gp41亞基呢?hVLP與現有結構的最大差別就在於此。此前發表結構中,Env的HR2螺旋幾乎都呈長桿狀構象,遠端由Asp664形成,而在本文獲得hVLP-Env中,其HR2螺旋長度減少10個氨基酸,改為由Gln653形成遠端。HR2 C端的其餘氨基酸彎折形成一個薄的莖環用以連線胞外段與病毒膜,該三腳架樣的莖環使得Env胞外段被抬升遠離病毒膜約10Å。這也使得膜近端外部區域(MPER)的大部分基本都嵌入膜中,這段區域被認為是可以誘導產生某些最廣譜中和抗體的理想疫苗靶點【6】。此外,作者還觀察到hVLP-Env向膜傾斜,導致子斷層平均密度圖中莖環區的密度降低。作者推測這種傾斜可能有助於病毒抵抗靶向MPER的中和抗體,中和實驗分析也驗證了這個猜想。hVLP-Env gp41亞基另一大結構差異是在均一化的結構中位於中心的HR1 C末端螺旋(570-595)的完整密度不可見。作者排除了解析度和引入對稱性的可能影響,HDX-MS分析顯示該區域的部分割槽段具有更強的主鏈氫鍵相互作用,對照此前已報道結構說明中心區也存在結構變異性。
最後,作者將目光聚焦在糖基化修飾。此前報道的結構中糖基化位點上的糖修飾往往只能看到核心的N-乙醯葡糖胺,但本文解析的hVLP-Env結構中,延伸的糖基化密度在整個蛋白上均可見到,尤其是在gp120和gp41亞基上解析出多個經典位點的糖修飾其密度範圍超過現有結構,顯示出所謂的“糖被(glycan shield)”。作者分析了受體CD4結合區附近、幾株重要中和抗體表位區及融合肽臨近區域的糖修飾,顯示糖側鏈可以透過空間位阻對相應位點提供保護作用。但V3-loop和V1-/V2-loop抗體結合超級位點處的糖修飾則不產生或僅產生微弱的空間位阻,而靶向這些位點的抗體往往需要結合臨近的糖側鏈方能實現其功能,作者由此推測這可能也是這些位點可以被抗體有效靶向的原因之一。此外,作者還發現某些糖修飾在Env三聚體每個單體上的密度存在差異,顯示出糖修飾的異質性。
回顧全文,作者透過冷凍電子斷層成像技術解析出天然狀態HIV-1病毒顆粒結構:在未成熟顆粒上,Env在底部Gag柵格上的取向呈多樣性,該狀態的捕獲為Env包裝的問題提供了一些線索;子斷層掃描圖平均重建的病毒粒子結構結合結構質譜分析,顯示出gp41亞基組成的中心的結構多樣性,不同Env單體上的糖基化修飾呈異質化,靈活的莖環允許Env蛋白的傾斜及中和表位的不同暴露方式。上述結果的獲得也為HIV-1組裝和Env表位呈現的結構多樣性提供了新的資訊。
原文連結:
https://doi.org/10.1016/j.cell.2022.01.013
製版人: 十一
參考文獻
1、 Pandey, A., and Galvani, A.P. (2019). The global burden of HIV and prospects for control. Lancet HIV 6, e809–e811.
2、 Ward, A.B., and Wilson, I.A. (2015). Insights into the trimeric HIV-1 envelope glycoprotein structure. Trends Biochem. Sci. 40, 101–107.
3、 Leaman, D.P., and Zwick, M.B. (2013). Increased functional stability and homogeneity of viral envelope spikes through directed evolution. PLoS Pathog. 9, e1003184.
4、 Stano, A., Leaman, D.P., Kim, A.S., Zhang, L., Autin, L., Ingale, J., Gift, S.K., Truong, J., Wyatt, R.T., Olson, A.J., and Zwick, M.B. (2017). Dense array of spikes on HIV-1 virion particles. J. Virol. 91, e00415-17.
5、 Tedbury, P.R., Novikova, M., Ablan, S.D., and Freed, E.O. (2016). Biochemical evidence of a role for matrix trimerization in HIV-1 envelope glycoprotein incorporation. Proc. Natl. Acad. Sci. USA 113, E182–E190.
6、 Rantalainen, K., Berndsen, Z.T., Antanasijevic, A., Schiffner, T., Zhang, X., Lee, W.H., Torres, J.L., Zhang, L., Irimia, A., Copps, J., et al. (2020). HIV-1 Envelope and MPER Antibody Structures in Lipid Assemblies. Cell Rep. 31, 107583.
轉載須知
【原創文章】BioArt原創文章,歡迎個人轉發分享,未經允許禁止轉載,所刊登的所有作品的著作權均為BioArt所擁有。BioArt保留所有法定權利,違者必究。