甲基化主要調節基因的表達和關閉,包括DNA甲基化和蛋白質甲基化(組蛋白甲基化研究最多),這兩種修飾都是在不改變DNA鹼基種類與數量的前提下使生物體表型呈現出多樣化,與癌症、衰老、老年痴呆等許多疾病密切相關,是表觀遺傳學的重要研究內容之一。因此甲基化在近年的研究中也呈現明顯的遞增趨勢。
今天給大家分享兩篇文章,帶你瞭解Alpha技術。
一、Nature解析DNMT3A2/DNMT3B3與核小體的結合模式
該研究團隊利用Cryo-EM技術首次解析了de novo DNA甲基轉移酶(DNMT3A2/DNMT3B3)和天然底物核小體的高解析度結構,闡述了DNMT3A2/DNMT3B3與核小體的結合模式,提出了全基因組DNA甲基化的模型。
a.利用AlphaScreen實驗測定His標記的DNMT3A2-DNMT3B3複合物與生物素標記的NCP相互作用。
二、Nat Genet解析DNMT3調控的新機制
研究者發現DNMT3A1的N末端區域與Polycomb抑制複合物1(PRC1)催化的組蛋白H2A第119位賴氨酸泛素化(H2AK119ub)修飾之間存在一種新的相互作用,並與之前報道的DNMT3A受PWWP引導與H3K36me2結合發生作用處於競爭關係。DNMT3A透過這兩種競爭募集機制調節CpG從頭甲基化的動態平衡。
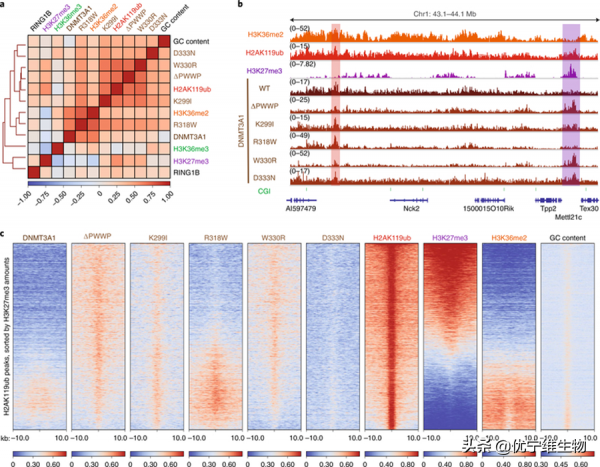
之前研究表明,DNMT3A受 PWWP 結構域引導與H3K36me2 和 H3K36me3結合,為了更好地瞭解 DNMT3A 突變體靶向調控作用,作者在間充質幹細胞MSCs中構建了DNMT3A1 的野生型、PWWP結構域缺失(ΔPWWP)、和 DNMT3A1突變體(K299I、R318W、W330R 和 D333N),透過使用染色質免疫沉澱和測序(ChIP-seq)獲得每個突變體的全基因組圖譜,將其與MSCs中組蛋白翻譯後修飾(H3K36me2、H3K36me3、H3K27me3和H2AK119ub)和PRC1亞基RING1B的基因組分佈模式進行比較,同時發現DNMT3A1從H3K36me2修飾富集區域重新定位到了Polycomb調控的CpG島上,無論PRC2催化三甲基化組蛋白H3賴氨酸27 (H3K27me3)生成多少,DNMT3A PWWP突變體會在由PRC1介導的單泛基化組蛋白H2A賴氨酸119 (H2AK119ub)生成的區域積累,攜帶PWWP突變的DNMT3A與H2AK119ub修飾的共定位水平遠強於PRC2催化的H3K27me3修飾(圖1圖2)。
圖1 由於PWWP 結構域缺失,促進了疾病突變體中DNMT3A與 H2AK119ub 的共定位。
圖2 DNMT3A 定位到 CGI 需要 PRC1 催化的 H2AK119ub 沉積
作者推斷野生型DNMT3A 可能具有結合 H2AK119ub 的潛在能力,當PWWP 域功能喪失時,這種能力在細胞中增強。因此採用AlphaLISA技術來驗證DNMT3A1與不同修飾的核小體間的結合能力,觀察到 DNMT3A1 與H2AK119ub 修飾的核小體有強烈的結合,與H3K27me3修飾的核小體間則不存在。接下來作者將DNMT3A1的N端結構域替換在刪除了PWWP結構域的DNMT3B上,DNMT3B 與 H3K36me3 和H3K36me2 修飾的核小體結合,但與 DNMT3A1 不同,在體外不能與H2AK119ub 修飾的核小體相互作用。DNMT3B 的氨基末端部分也缺乏界限分明的有序結構域,表明UDR 介導的 H2AK119ub 識別可能對 DNMT3A1具有特異性,表明DNMT3A1和H2AK119ub修飾的相互作用是透過其N末端區域介導的(圖3)。
圖3 DNMT3A 透過 N 端 UDR 直接與 H2AK119ub 相互作用
最後,研究者透過在攜帶PWWP結構域突變DNMT3A的細胞中敲除PRC1(Ring1a/b),但保留PRC2(Ezh2),觀察到富含 H2AK119ub 的 CGI 處的 DNA 高甲基化被 PRC1 的缺失和伴隨的DNMT3A1 K299I 和 W330R 突變募集的缺失所消除,在全基因組範圍內,DNMT3A1K299I 和 W330R 突變體的表達以依賴於 PRC1 的方式促進 H2AK119ub 富集區域的高甲基化,K299I 和 W330R 突變細胞中的 CGI 高甲基化同樣需要PRC1,證明了敲除能夠破壞攜帶PWWP突變的DNMT3A與CpG島的結合。這進一步證明了DNMT3A透過與PRC1催化的H2AK119ub修飾相互作用,最終導致CpG島超甲基化(圖4)。
圖4 DNMT3A 介導的 CGI 高甲基化依賴於 PRC1
Alpha技術介紹
Alpha(Amplified Luminescent ProximityHomogenous Assay)是一項基於微珠靠近的均相檢測技術(無需洗滌),幾乎可以勝任所有的分子相互作用研究。
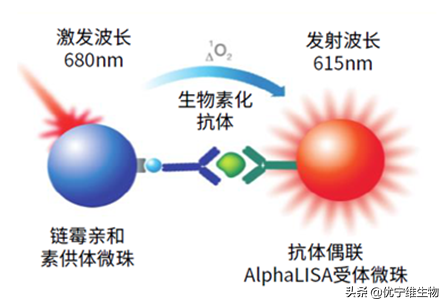
檢測原理:細胞裂解液,細胞上清或血清樣品中的待測物分別被生物素化抗體和受體微珠偶聯的抗體識別,形成三明治形式。之後加入鏈黴親和素包被的供體微珠結合生物素化抗體。在680nm鐳射的激發下,表面塗布高濃度光敏劑的供體微珠被啟用並使周圍環境中的氧分子轉化成高能活躍的單體氧(singletoxygen),在4微秒的半衰期內,單體氧在溶液中擴散觸發受體微珠上的化學分子,並瞬間激發化學級聯放大反應後最終使受體微珠產生615nm光訊號,產生的光訊號與被檢測的濃度成正相關(圖1)。Alpha技術幾乎是萬能的,因為微珠表面可以包被上不同的生物分子以滿足特定物質的檢測。
圖1 Alpha技術的一般原理
技術優勢:
長波長高強度單色鐳射激發,短波長檢測,減少干擾。
化學發光訊號檢測,低背景,高信噪比,訊號半衰期達4us。
102擴散距離可達200nm,應用範圍更廣,更適合大分子檢測。
檢測靈敏度高達10-17mol,節省樣品,節省成本。
高動態檢測範圍、無需稀釋、均相檢測無需洗滌。
VICTORNivo多模式微孔板讀板儀
最新的VICTORNivo多模式微孔板讀板儀配置了高靈敏Alpha技術的所有硬體,680nm鐳射光源用來激發供體微珠,D660專業二向色鏡和Alpha 專用發射濾光片。同時,VICTOR Nivo透過特殊的設計,阻攔激發時發射訊號的檢測,從而降低了背景訊號。配置吸光度、化學發光、熒光強度、時間分辨熒光、熒光偏振、Alpha技術六種檢測模式,絕大多數模式可以實現頂部和底部檢測,搭配32位濾光片轉輪,實現更好的靈敏度和更大範圍的高信價比。