

IgG4相關性疾病(IgG4‐RD)幾乎可累及全身所有臟器,臨床表現複雜多樣。然而由於該病較為罕見,以及學界對其認識時間較短,IgG4‐RD的整體診治水平參差不齊。2021年上半年,我國首次釋出《IgG4相關性疾病診治中國專家共識》(以下簡稱共識),極大地促進了IgG4‐RD臨床診療水平的改善。
共識提到,對於IgG4‐RD,建議依據2011年日本製定的IgG4‑RD綜合診斷標準及2019年美國風溼病學會(ACR)/歐洲抗風溼病聯盟(EULAR)制定的IgG4‑RD分類標準進行診斷。那麼,這兩個標準都包括哪些內容?診斷的敏感性和特異性如何?本文將對此進行簡要總結。
2011年日本製定的IgG4‐RD綜合診斷標準
2011年日本製定的綜合診斷標準是IgG4‐RD領域最早的綜合性分類診斷標準,亦是迄今為止臨床醫師應用最廣泛的標準之一。主要包括特徵性臨床表現、血清IgG4升高和典型的病理特徵三個方面。具體包括以下3條標準:
①臨床檢查顯示1個或多個臟器特徵性的瀰漫性/侷限性腫大或腫塊形成
②血清IgG4升高(>1350mg/L)
③組織病理結果顯示:
- 大量淋巴細胞和漿細胞浸潤,伴纖維化;
- 組織中浸潤的IgG4+漿細胞/IgG+漿細胞比值>40%,且每高倍鏡視野下IgG4+漿細胞>10個。
符合以上3條標準可確診,符合①和③者為可能診斷,符合①和②者為可疑診斷。
該標準中除臨床特徵性表現之外,強調患者應具有血清IgG4水平升高和病理特徵。然而,血清IgG4升高可見於多種非IgG4-RD,例如胰腺癌、ANCA相關性血管炎、過敏性疾病等,且有文獻報道約40%的IgG4-RD患者血清IgG4並不升高。因此,該標準診斷的敏感度和特異度並不十分理想。
2020年,日本學者討論更新了2011年IgG4‐RD綜合診斷標準:①臨床及影像學特徵方面,如果單一器官受累,單純的淋巴結腫大不適用於這一診斷標準;②病理學診斷方面,在原有2條病理診斷標準的基礎上新增1條病理標準:典型的組織纖維化,尤其是席紋狀纖維化,或閉塞性靜脈炎。符合3條病理學診斷標準的任意2條,即支援IgG4‐RD的病理診斷。目前,該標準暫未得到國內指南的推薦。
2019年ACR/EULAR制定的IgG4‑RD分類標準
2019年ACR/EULAR制定的IgG4‑RD分類標準是繼日本2011年制定的綜合診斷標準後的首個國際分類標準,對指導IgG4-RD的診斷和分類具有重要意義。該標準納入了常見器官受累的特徵性臨床表現,並強調排除疑似IgG4‐RD的多種疾病(表1)。
表1 2019年ACR/EULAR制定的IgG4‑RD分類標準
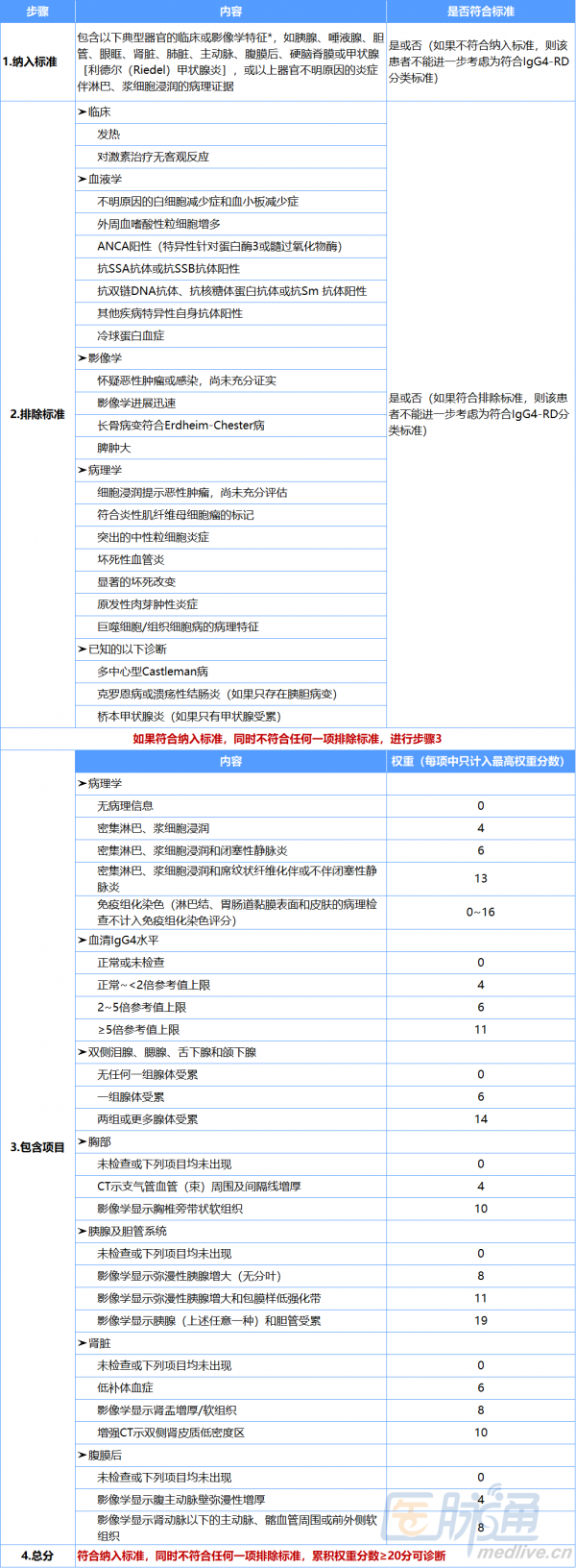
受累器官腫大或腫瘤樣腫塊,但以下器官受累常為非腫塊病變,(1)膽管,更傾向發生狹窄;(2)主動脈,典型特徵是管壁增厚或動脈瘤形成;(3)肺部,常見支氣管血管束增厚
經兩項獨立佇列驗證顯示,該標準的特異度分別為99.2%和97.8%,敏感度分別為85.5%和82.0%。相比於2011年診斷標準,2019年標準的優勢在於,即使在缺乏病理診斷或血清IgG4不升高時仍可以將患者歸類為IgG4‐RD。
然而,2019年標準涉及條目較多,積分複雜,在臨床工作中應用比較困難。因此,目前臨床中2011年日本製定的綜合診斷標準更為常用,而科學研究多采用2019年ACR/EULAR制定的IgG4‑RD分類標準。
最後需要強調的是,IgG4‐RD可模擬多種疾病,而多種其他疾病也可模擬IgG4‐RD,因此上述兩個標準均強調該病的診斷需排除腫瘤、系統性血管炎、慢性感染等疾病。
1.張文,董凌莉,朱劍,等.IgG-4相關性疾病診治中國專家共識[J].中華內科雜誌,2021,60(03):192-206.
2.師千與,劉燕鷹. 免疫球蛋白G4相關疾病的診治進展[J]. 中華風溼病學雜誌,2021,25(8):564-569. DOI:10.3760/cma.j.cn141217-20201120-00438.
3.劉航,楊娉婷,肖衛國,等. 解讀"2019年ACR及EULAR IgG4相關性疾病分類標準"[J]. 中華臨床免疫和變態反應雜誌,2019(6). DOI:10.3969∕j.issn.1673-8705.2019.06.003.




















