關於晶研談
晶研談是由晶泰科技發起的藥物固態研究交流專欄,旨在與學術專家及業界同行就藥物固體形態研究中的問題與挑戰進行深入交流,分享最新研究進展,討論前沿創新技術,探索有效解決方案,共同促進國內藥物固體形態研究的發展及繁榮。
為什麼要做晶型預測?
相同的藥物分子因其晶型不同而具有不同的理化性質,而理化性質的不同決定了藥物在人體內的生物利用度,生物利用度又最終影響藥效、給藥形式以及計量等問題。
因此在現代藥物研發的臨床期研究中,進行完備的晶型篩選實驗是非常重要的一個環節。但單純地透過實驗進行晶型篩選是投入時間長、人力成本高,且沒有明確終點的事情。換句話說就是——即使已經透過實驗發現了多種晶型,依舊無法判斷是否還存在其他穩定晶型!
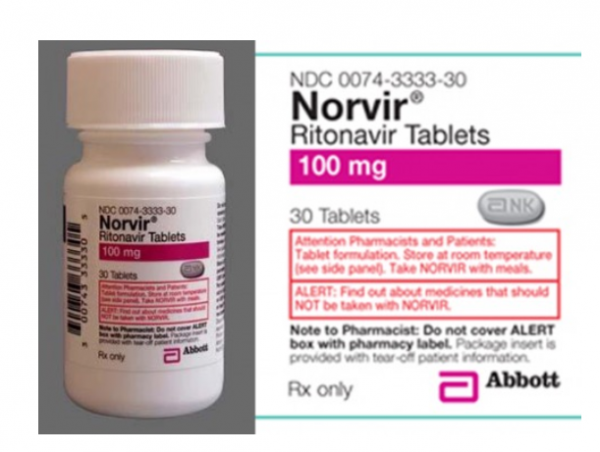
以美國雅培在 1996 年上市的抗艾滋病特效藥利托那韋為例,它上市時是以晶型I存在的;但兩年後即 1998 年市面上在售的利托那韋被檢測出存在晶型II,因此雅培又重新進行了晶型研究;而僅僅四年後(2002年) TransForm 公司卻又發現了它的第三種晶型!
什麼是晶型預測?
透過計算機模擬來進行或輔助藥物晶型篩選,一方面可以縮短實驗週期;另一方面可以給出晶型研究是否完備的理論預估。隨著計算機演算法和算力的快速發展,自 2016 年以來,晶型預測技術就被逐步深入應用到藥物研發流程的各個環節中。
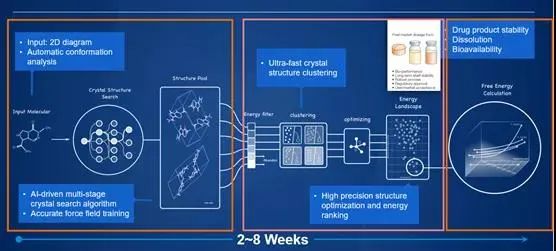
晶型預測(Crystal Structure Prediction,簡稱CSP)是指給定分子的二維結構式透過計算模擬獲得它的所有可能的穩定晶型。CSP 流程共包含三個主要階段,晶體搜尋、能量排位和室溫穩定性計算。其中每個階段都包含一些關鍵難點,接下來會詳細介紹。
Stage 1. 晶體搜尋
晶體搜尋在數學上表達為一個高維空間的全域性最佳化問題。即構造一個關於晶體所有自由度的能量函式,求解這個能量函式的全域性最小點和一部分局域極小點的問題。晶體自由度包含分子的內稟自由度、晶胞引數、分子在晶胞中的位置,以及晶體的對稱性即空間群型別。其中分子內稟自由度包括柔性二面角的個數和環異構數目以及可能的手性;晶胞引數包含三個晶格常數和三個晶軸夾角;分子在晶胞中的位置包含分子在晶體座標系中的質心座標和分子相對於座標系的方向;而晶體對稱性可以是自然界中 230 個空間群中的任意一種。而搜尋問題的計算複雜度還隨著晶體自由度的增加呈指數級增長。
針對這樣一個困難的高維最佳化問題,我們採用了三種主要的解決思路:首先是隨機演算法和啟發式演算法結合的全域性最佳化演算法,隨機演算法採用並行蒙特卡洛,這個演算法在數學上是可以嚴格證明當取樣充分時總能到達全域性最小點的,但它的問題在於取樣效率低,因此這裡還結合了粒子群演算法這類啟發式演算法提高搜尋速度和效率;其次是使用隨機和局域最佳化結合的結構生成演算法,這是因為複雜體系隨機生成結構生成效率低,因此採用隨機生成加局域最佳化來提高結構生成效率,能夠將預先知道的化學資訊和規則加入局域最佳化器,使得生成化學合理的虛擬結構比例大幅度提高;第三是引入機器學習演算法主動識別低能區並增強取樣,進一步提高搜尋效率。通常在晶體搜尋階段能得到數百萬甚至千萬量級的具有化學合理性的虛擬晶體結構。
Stage 2. 能量排位
通常來說,量子化學精度的計算可以得到較為可靠的相對穩定性和晶體結構,但搜尋階段產生的虛擬結構數量級過大,如果全部使用量子化學精度的計算則非常昂貴且耗時,且常規精度的量化計算的時間複雜度隨體系複雜度呈 O(N3)~O(N4) 增長,當體系過於複雜之後,這就成了不可解決的問題,更不用說高精度的量子化學計算了。而另一方面,基於經典力學的力場方法速度快,但它與量化能量相關性不高。所以在實際計算中,我們採用多輪精度不同的排位策略逐步篩選的方法,使得 CSP 在藥物工業中變得真正實用。多輪精度不同的排位策略可以逐步篩除掉部分高能結構,從力場到半經驗方法可以將結構數從百萬減少到萬或者十萬量級,從半經驗方法到量子化學計算,可以進一步將結構數減少到千量級。最終階段只對極少數結構進行高精度量子化學計算,將相對能量誤差控制在 1.5kJ/mol 以內。
Stage 3. 室溫穩定性計算
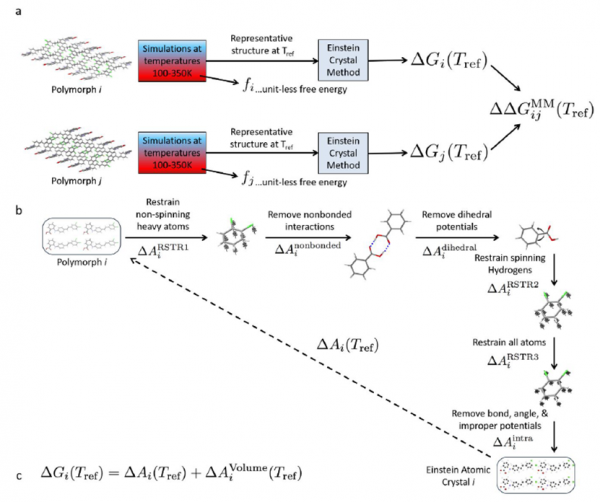
量子化學計算的是晶體在絕對零度下的能量,但實際上藥物研發中所需要考慮的晶體穩定性通常是室溫穩定性,這就需要進行有限溫度的自由能計算。這裡我們採用兩種不同框架的計算在低溫段互相驗證,確定最終的室溫穩定性。基於簡諧近似或準簡諧近似的晶格動力學理論,可以透過計算聲子態密度的積分來獲得絕對零度附近的任意低溫區的赫姆霍茲自由能,從赫姆霍茲自由能可以判斷有限溫度的穩定性,這種方法是基於量子的,通常認為精度較高,但由於它的理論基礎是準簡諧近似,所以計算結果只在低於 150K 的低溫下可靠,溫度稍高一點結果就不再可信了。所以實際計算室溫 300K 的穩定性就需要用到基於嚴格熱力學迴圈和構型取樣的準超臨界路徑方法 PSCP(pseudo super-critical path)【1】。這個方法需要用到假想的愛因斯坦晶體,某一個晶體結構它對應的愛因斯坦晶體是指跟它的原子的空間三維座標一致,但去掉全部相互作用的虛擬體系。當比對兩個化學成分相同但構型不同的晶體結構時,只需要對這兩個結構分別構建熱力學過程從有相互作用的狀態逐漸去相互作用變到他們各自的愛因斯坦晶體態,那麼這兩個結構的自由能差等同於他們分別變化到各自的愛因斯坦態的自由能變化的差。這樣就避免了採用分子動力學模擬計算一個晶體昇華過程絕對自由能由於構型變化導致的取樣不充分問題,可以用較少的模擬時長就能得到兩個晶體之間較精確的自由能差。但 PSCP 方法的結果可靠性非常依賴力場引數對動力學過程中的結構描述的準確性,所以在實際應用中我們通常會擬合多版專有力場引數,並將它們的低溫段(<150K)的分子動力學模擬自由能趨勢與前面介紹的基於諧振近似的晶格動力學自由能趨勢進行對比,選擇二者符合較好的一版力場引數,使用 PSCP 方法計算室溫下的自由能。
晶型預測在藥物研發中的多元化應用
接下來從具體例子介紹晶型預測(CSP)在藥物研發中的 3 個主要應用場景:
1. CSP 最直接的應用就是轉晶風險評估
這是晶泰科技和美國阿斯利康合作研究的一個工作【2】。AZD1305(圖4)是一種治療心血管疾病的分子,通常這樣柔性自由度高、分子複雜的體系,它的多晶型現象會很複雜,晶型之間的相對穩定性情況也會比較複雜,阿斯利康透過實驗篩選到了兩種晶型,但是不確定篩選是否完備,即是否還有可能存在其他更穩定的晶型。於是晶泰科技藥物固態研發團隊做了 CSP 研究,併成功地找到了兩種實驗晶型 Form A 和 Form B,在 landscape 中對應的虛擬晶型分別為 X1 和 X23 。此外,自由能計算證明室溫下(300 K)Form A 和Form B是兩種最穩定晶型,其他虛擬晶型的室溫穩定度均不如這兩個,理論計算(圖5,6)基本上排除了室溫下存在其他更穩定晶型的風險。
2. CSP 第二個應用場景是指導實驗製備新晶型,比如推薦結晶條件。
這是一個透過理論計算的資訊幫助實驗選擇非常規條件,獲得異丙煙肼最穩定晶型的例子【3】。大量常規實驗結晶包括溶液相結晶、凝膠相結晶、昇華結晶等方法都只能得到 Form I 和 Form II。但 CSP 發現在晶格能低於 Form I 的區域還存在一個虛擬晶型,那虛擬晶型有一定可能性是能真實存在的。從能量-密度圖(圖8)中觀察到這個結構的密度大於所有其他結構。進一步進行加壓晶格能計算發現這個結構隨著壓力增加晶格能持續下降(圖9),且始終低於 From I。綜合密度大和加壓穩定性增加兩方面的資訊,猜測高壓可能可以穩定這個虛擬晶型。隨後的高壓結晶實驗確實證實了理論預測的結果,在 Merrill−Bassett diamond anvil cells DACs(diamond anvil cells)中壓縮常壓下長出來的晶體,當壓力增加到 2.1 GPa 時,實驗觀察到 Form I 發生了轉晶,透過單晶X射線衍射證明新發現的晶型確實為 Form III。(本案例來自文獻報道,晶泰科技與藥企合作加壓結晶預測的案例由於保密性要求沒有在這裡展示)

圖7 異丙煙肼(左),Form I (中),Form II(右)
3. CSP 的第三個用途是藥物發現早期的溶解度預測
由於溶解度直接影響藥物的生物利用度並最終影響藥效,因此在藥物發現早期,獲得溶解度資訊對於先導化合物的選擇和最佳化都有重要意義。但由於處在藥物發現早期,先導化合物數量大,如果全部使用實驗方法精確測定溶解度,則面臨合成任務重,合成困難以及週期長的問題。因此如果透過計算在不需要合成的時候能夠又快又準地得到溶解度則能直接加速藥物研發過程。但它的一個較大的困難是先導化合物分子之間較相似,在沒有晶體資訊的情況下透過理論預測這些相似分子的溶解度區分度不高。
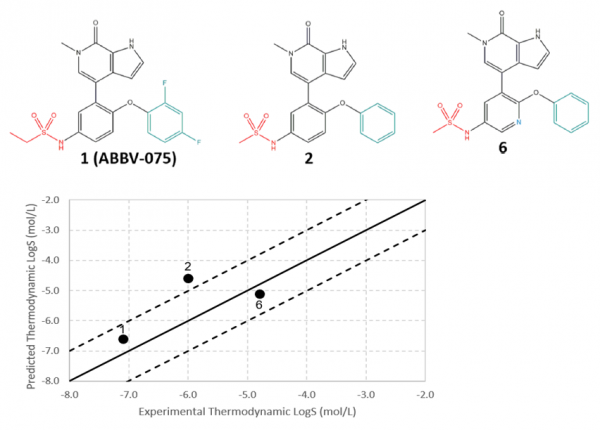
這裡展示的例子是晶泰科技和美國 AbbVie 公司合作研究的一個早期溶解度預測的工作【4】,文章中針對 AbbVie 早期設計出的 8 個相似分子(圖10)進行了溶解度預測。傳統的溶解度預測,無論是 QSAR 方法,還是基於無定型態構建熱力學迴圈計算溶解自由能的方法,由於都無法將晶體堆積作用對溶解度的影響考慮到模型中,因此預測出來的溶解度資料很難區分開具有相似骨架的同系列分子,如圖 11 中的白色空心方點所示;但基於晶體結構資訊的溶解度預測資料在相似分子間更具有區分度,如圖 11 中黑色圓點所示。且和已有的熱力學溶解度資料對比,預測溶解度和實驗溶解度的誤差更小(圖12),因此可以用作先導化合物篩選的資訊。最終, Abbvie 根據我們的溶解度預測值和其他 ADMET 值一起進行綜合考慮,選擇了 8 個分子中的一個進行後續開發。
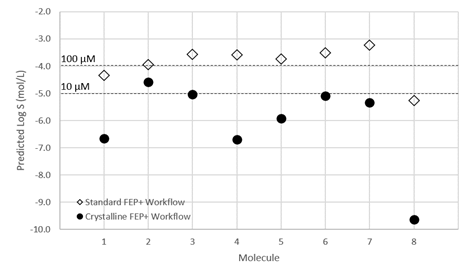
圖11 基於無定型態(空心方點)和基於晶體(黑圓點)的溶解度預測
結語
綜上所述,晶型預測(CSP)在技術層面可有效評估現有晶型間相對穩定性,及當前晶型研究的合理性,從而更為精準地評估藥物後期的轉晶風險並加速決策;在戰略層面可評估現有晶型研究是否完備,從而對於藥企智慧財產權佈局及藥品全生命週期管理提供可靠的依據。
CSP 技術無需實驗資料輔助,因此可根據各型別創新藥專案的推進計劃靈活選擇研究時間。同時也因其高效、準確的服務質量,眾多國內外頂級藥企已將 CSP 納入小分子藥物研究的標準流程。在過去幾年裡,晶泰科技已透過 CSP 技術加速了客戶 100 多款創新藥的開發,經過5年的經驗積累和精益求精的技術迭代,近 3 年 CSP 預測的準確率始終保持在 100%。
未來我們會進一步最佳化 CSP 的演算法,縮短週期並降低成本;同時結合 AI 演算法,進一步精準推薦結晶條件,致力於為國內外客戶提供更為優質的固研服務。
如果您有相關問題,歡迎給本篇文章「留言」或點選文末「閱讀原文」按鈕聯絡我們,期待與您進一步交流與探討。業務諮詢請聯絡:[email protected]
參考文獻:
[1] Cryst. Growth Des. 2020, 20, 8, 5211–5224
[2] Cryst. Growth Des. 2021, 21, 4, 1972–1983
[3] Taylor, C.R., Mulvee, M. T. , Perenyi, D. S. , Probert, M. R. , & Steed, J. W. . J. Am. Chem. Soc., 2020
[4] J. Chem. Inf.Model. 2021,61, 3, 1412–1426
文中 圖 2 - 圖 12 均來源於晶泰科技
未經授權,請勿轉載使用
關於晶泰科技
晶泰科技是一家量子物理與人工智慧賦能的藥物研發公司,透過提高藥物研發的速度、規模、創新性和成功率,致力於實現藥物研發的行業革新。作為一家立足中美、服務全球的企業,晶泰科技始終堅持探索最優解決方案,以充分利用前沿的研發與計算資源,最大化滿足客戶與合作方的需求。
晶泰科技的智慧藥物研發平臺將基於雲端超算數字化研發工具與先進的實驗能力進行整合,形成高精度預測與針對性實驗相互印證、相互指導的研發系統。作為全球先鋒人工智慧藥物研發公司之一,晶泰科技已建立起一整套量子物理幹實驗室與先進溼實驗室緊密結合的研發迭代流程,挑戰傳統研發的效率瓶頸,賦能新藥研發實現創新速度與規模的突破。