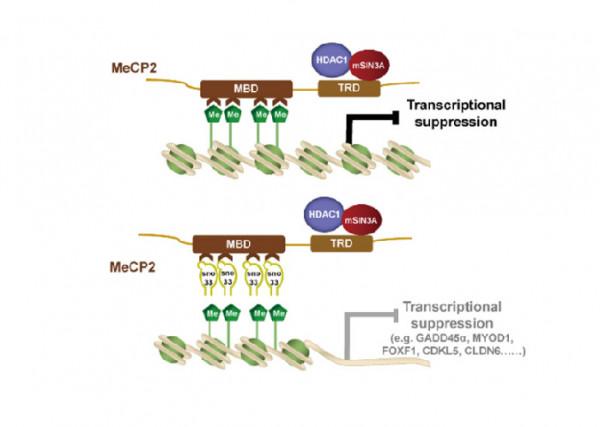
SNORD33調控三陰性乳腺癌細胞鉑類敏感性的機制示意圖(受訪者供圖)
近日,《分子腫瘤》線上發表了復旦大學附屬腫瘤醫院教授王碧芸、胡夕春團隊聯合復旦大學基礎醫學院研究員陳舌團隊一項關於三陰性乳腺癌化療效果預測的研究成果。該研究首次發現小核仁RNA SNORD33在接受含鉑類藥物治療方案、但療效不同的三陰性乳腺癌患者群中,表達水平呈現出明顯差異,可作為預測該治療方案效果的標誌物。
此外,研究團隊還結合腫瘤轉移情況,繪製出可以預測鉑類方案治療轉移性三陰性乳腺癌患者生存情況的列線圖。
一直未找到有效標記物
三陰性乳腺癌約佔所有乳腺癌中的15%,因其惡性程度高、缺乏精準治療靶點、患者復發轉移風險大、總體生存率較其他乳腺癌亞型低,而被公認為是“最難治”的乳腺癌。
鉑類化療藥物是三陰性乳腺癌治療中常用的一種方案,這類藥物主要透過影響癌細胞基因的合成和修復起到抗癌的作用。在臨床上,許多患者需要接受鉑類藥物治療。然而,仍有一些三陰性乳腺癌患者接受鉑類藥物治療無效。
王碧芸表示,如果能夠預先篩選出三陰性乳腺癌患者中對鉑類藥物耐藥的人群,則可以“分類而治”,讓“預測耐藥”的人群避免“無效用藥”,進而提升鉑類方案治療效果、實現對該類患者群體更精準治療、延長患者生存時間。
然而,此前醫學界尚未找到能精準預測三陰性乳腺癌鉑類藥物方案療效的生物標誌物。
發現SNORD33的預測作用
據瞭解,小核仁核糖核酸(snoRNA)是細胞遺傳物質的一種,在多種腫瘤中發揮了促癌或抑癌的作用,且這種遺傳物質在血漿等體液中有一定分佈,因而被視為液體活檢的潛在生物標誌物。
在前期研究中,該研究團隊透過二代基因測序技術深度檢測發現,小核仁RNA SNORD33在三陰性乳腺癌順鉑治療方案耐藥的患者中表達水平顯著低下。此外,SNORD33下調在體外促進了三陰性乳腺癌細胞對順鉑的耐藥。
SNORD33是否可以作為探索已久的三陰性乳腺癌鉑類方案預測標誌物?為此,研究團隊基於209例一線接受含鉑方案治療的轉移性三陰性乳腺癌患者的血漿樣本,發現血漿中SNORD33低水平的患者生存時間顯著短於SNORD33 高水平組。
研究證實了血漿SNORD33是使用含鉑方案治療三陰性乳腺癌患者生存時間的獨立預測因子。另外,在45例一線接受非鉑類藥物方案治療的患者樣本中,血漿SNORD33水平與生存時間無顯著相關性,提示SNORD33對於鉑類療效預測的特異性。
為更好預測鉑類治療三陰性乳腺癌療效,本研究還透過綜合基線肝轉移狀態、轉移灶數目以及血漿中SNORD33 水平這3個重要指標,製作了可以預測含鉑一線治療轉移性乳腺癌患者生存時間的列線圖。
胡夕春表示,透過對列線圖的分析,可對每個患者進行個體化的計算,進而得到對應的不同月份發生進展的機率。即在基線時透過簡單的計算判斷患者使用含鉑方案生存時間長短的機率,彌補了僅透過SNORD33 表達的高低進行預後判斷的相對“簡略粗糙”的缺點,更加完善血漿SNORD33作為鉑類藥物預測分子靶標的可行性。
不斷探尋耐藥機制
隨後,該研究團隊又進一步探索了SNORD33在三陰性乳腺癌鉑類方案耐藥中發揮的作用,以進一步明確該物質調控三陰性乳腺癌鉑類敏感性的機制,為後續治療策略提供參考方向。
研究利用SNORD33結合蛋白質譜分析技術,發現SNORD33存在與甲基化結合蛋白MeCP2的結合。資料顯示,SNORD33水平下調會增加MeCP2與下游靶基因啟動子甲基化區域的結合,釋放MeCP2的轉錄抑制活性,進一步抑制包括GADD45α、MYOD1、FOXF1、CDKL5、CLDN6在內的凋亡相關的基因的表達,致使細胞凋亡減少,從而使得三陰性乳腺癌細胞對鉑類的抵抗增加。
“後續的成果進一步揭示了SNORD33調控三陰性乳腺癌對鉑類藥物耐藥的機制,”王碧芸表示,“這也啟發我們從該調控過程入手,開展更深層次的研究,以提升鉑類藥物治療效果,讓更多三陰性乳腺癌患者從中受益。”(張思瑋 黃辛)
相關論文資訊:https://doi.org/10.1186/s12943-022-01504-0
來源: 中國科學報