來源:湖城麻醉
01
前 言
上肢手術鎮痛方案包括全麻和臂叢神經阻滯。阿片類藥物是控制中、重度疼痛的首選全麻藥物。臂叢神經阻滯能減少甚至避免全麻藥物的使用。臂叢神經阻滯途 徑包括肌間溝、鎖骨上、鎖骨下及腋路等入路。 研究表明,肌間溝入路100%會造成膈神經阻滯,鎖骨上與鎖骨下入路均有造成氣胸的風險。經腋路實施臂叢神經阻滯可避免膈神經阻滯和氣胸的發生。腋神經(AN)支配肱骨上段的三角肌等部位,開展AN輔助腋路臂叢神經阻滯用於上肢手術研究具有臨床探討價值。本文就近年來超聲引導下腋神經阻滯(UGBAN) 相關研究進行綜述。
02
AN超聲解剖學
AN源於C5和C6脊神經的前支,發自臂叢神經的後束。在腋窩內,AN於腋動脈後方、肩胛下肌前面下行, 與旋肱後動脈 ( PCHA)一起穿過四邊孔(QS)。QS上緣 為小圓肌,下緣為大圓肌,外側緣為肱骨外科頸,內側緣為肱三頭肌長頭。 AN進入QS內分為前後兩支,前支相對較粗, 後支較細。AN 前支為三角肌支,與旋肱後血管伴行,繞過肱骨外科頸分佈於三角肌的前外側部,其神經末端入肌處寬大,呈扇面形進入肌肉,支配三角肌,主要是三角肌的前、中 兩個亞部。 AN後支沿著三頭肌附著點行於後內側、關節盂之下,發出三角肌後部肌支、小圓肌肌支、肩關節支和臂外側皮支。 透過對21具屍體進行雙側解剖以確定AN的分支,描述了兩種AN分支模式。
主要分支模式:三角肌筋膜與肩胛下肌之間的AN沒有分支(62.5%)、有前後分支 (17.5%) 以及有3條小關節分支 (20.0%)。
次要分支模式:指向肩關節的細小神經從AN主幹出現並向腹側延伸到肩胛下肌肌腱前外側,27.5%的案例存在這種分支模式。識別 AN 的感覺關節分支及其與附近解剖結構的關係,有助於實施神經阻滯時不損害運動神經 。
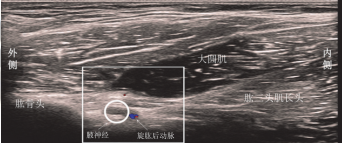
AN前路超聲解剖學特點(圖1):
使用能顯示小神經的行動式高頻線陣超聲探頭掃描,將超聲探頭橫向放置在胸大肌的外側邊緣處,臂外展以識別腋窩中的臂叢神經,短軸平面顯示臂叢位於背闊肌和背闊肌肌腱前面。 將探頭稍微向頭側移動,一旦大圓肌的上邊緣消失即可確認QS。QS是肱骨和大圓肌之間的狹窄間隙,其中AN表現為伴有PCHA的高回聲蜂窩狀橢圓形結構。 PCHA的起源和走行變化很大,僅作為識別AN的輔助結構之一。進入QS或在肩胛下肌之前,可以看到AN。手臂從90°外展180°使神經透過關閉QS更緊密貼近面板。
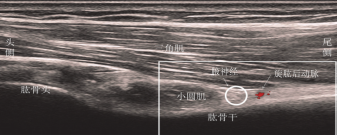
AN後路超聲解剖學特點(圖2):
受檢者取坐位,肩膀內旋45°呈直立位,肘部彎曲90°,將手掌放在膝蓋上。高頻線陣超聲探頭平行於肱骨長軸,放置於肩峰後外側下方約2cm處。重要的解剖結構包括肱骨頭、肱骨幹、橫切面的小圓肌、縱切面的三角肌和肱三頭肌。
三角肌、小圓肌和肱三頭肌之間的間隙可見PCHA。AN位於小圓肌、三角肌後部的深處、肱三頭長頭和肱骨幹之間的神經血管間隙中,超聲顯示PCHA短軸聲像及 PCHA上方呈篩網狀的AN短軸聲像。
03
AN阻滯路徑
AN的走行分佈相對深的部位,超聲輔助手段是目前為止最佳的選擇。透過超聲定位小圓肌、三角肌、肱三頭肌和肱骨幹來識別PCHA,並利用神經刺激儀將穿刺針定位於PCHA周圍,注入局麻藥物,評估AN所支配部位的感覺與運動情況。
結果表明,在12名健康志願者中,有10名志願者出現感覺和運動神經阻滯,另外兩名志願者只出現感覺阻滯而未出現運動阻滯。首次論證經後路超聲引匯入路的可行性。
但是, 在臨床實踐中, 超聲引導下檢查PCHA可以觀察到兩個或更多分支血管,並且AN通常在超聲檢查中不可見。另外,PCHA起源的變化很常見,有時會出現變異。因此,以PCHA聲像為標誌,可能會阻滯失敗。同時,後路AN分支模式在個體之間存在顯著差異。
研究表明,PCHA存在變異可能,依賴其定位可能會給UGBAN效果帶來諸多的不確定, 因而首次提出“筋膜間隙” 概念。 一項前瞻性、隨機、單盲臨床試驗透過三角肌與小圓肌之間的“筋膜間隙” 和PCHA血管周圍注射局麻藥,透過針刺感覺的喪失以及三角肌運動阻滯效果評估AN阻滯的成功率,在阻滯後30min差異無統計學意義,發現筋膜間注射無需以PCHA和AN作為標誌,而且不受PCHA解剖結構變異的影響。 研究表明,在筋膜間隙注入局麻藥,可能會透過上中部肱盂韌帶之間的天然莢膜通道,稱之為Weibrecht孔,到達肩關節囊的表面甚至關節腔,阻滯AN感覺分支,即所謂的肩前囊阻滯。筋膜間隙內組織結構及局麻藥擴散機制有待進一步研究。 嘗試在腋區實施UGBAN,將高頻線陣超聲探頭放置在腋窩皺襞上,依次識別背闊肌、肱骨小結節、大圓肌及肱三頭肌長頭,即在QS平面內,然後探頭沿肱骨長軸向內側移動,直到肱骨頭顯示出來。 肱骨頭的明顯特點是具有構成低迴聲覆蓋的軟骨的球形結構。在軟骨處,PCHA環繞肱骨頭,AN與PCHA平行。探頭平面內,穿刺針從外側入路,針尖直至PCHA周圍。 對6具屍體進行初步解剖研究,在46具防腐屍體上進行超聲引導雙側AN,確定QS中AN的關鍵超聲標誌是肱骨、大圓肌和肩胛下肌。研究表明,AN穿過QS所佔比例達到99%,再次論證瞭解剖學依據,同時提供了前路腋區入路的超聲標誌。 假設將高頻線陣超聲探頭放置在鎖骨下方並與其平行,確定喙突聲像,然後讓手臂外旋,避免內收,以觀察肩胛下肌和三角肌。 研究表明,於肩胛下肌和三角肌之間的間隙注入0.25%布比卡因10ml對AN有阻滯效果,同時對肌皮神經、胸外側神經、鎖骨上神經外支和肋間臂神經分支所支配區域也有阻滯效果。該路 徑將可以作為前路腋區QS阻滯路徑的補充方案,其臨床效果有待進一步研究。
04
UGBAN的常用藥物
長效醯胺類局麻藥羅哌卡因在神經阻滯中被廣泛應用, 具有明顯的感覺與運動阻滯分離特點,是圍術期鎮痛類局麻藥物的首選。 對UGBAN出現感覺運動分離時羅哌卡因的有效濃度進行研究,結果表明,0.125%羅哌卡因16ml用於UGBAN中實現感覺阻滯(鎮痛)僅伴有侷限的非進行性運動神經阻滯。隨著局麻藥濃度的增加,起效時間縮短,鎮痛時間延長,同時,局麻藥吸收入血致心臟毒性增強。 一項隨機、雙盲、對照試驗,實施超聲引導下選擇性AN阻滯,認為該阻滯方式能緩解肩部疼痛。但是, 這種阻滯方式難以準確預測效果,可能原因是AN在肩部變異,而與羅哌卡因濃度無關。
05
UGBAN的局麻藥佐劑
局麻藥中加入腎上腺素的目的是減少局麻藥在迴圈系統中的吸收,減輕全身毒性反應,同時延長局麻藥作用時間。 研究表明,對於已知存在神經病變,例如糖尿病多發性神經疾病,局麻藥阻滯神經後,腎上腺素對神經功能改變等病理生理過程發揮了一定作用,但這只是理論上分析,尚未得到證實。
2、阿片類藥物 周圍神經阻滯中,局麻藥聯合阿片類藥物,如嗎啡、舒芬太尼及芬太尼等,作用機制是結合軸突上阿片類藥物受體。 鎮痛效果與劑量有關,研究表明,劑量過高不能排除引起阿片類藥物潛在的全身作用,只有在排除阿片類藥物全身作用的情況下,周圍神經旁給予阿片類藥物才適用。 丁丙諾啡 是局麻藥的理想佐劑,因為它具有高親脂性、細胞膜滲透性以及與μ阿片受體特異性結合的特點。研究表明,與單獨給予局麻藥比較,神經鞘內給予丁丙諾啡 0.1-0.3mg會顯著延長鎮痛時間。 局麻藥聯合阿片類藥物用於AN阻滯仍有待進一步研究,《外周神經阻滯併發症防治專家共識》建議慎用局麻藥佐劑。
3、右美託咪定
右美託咪定是一種選擇性α₂腎上腺素受體激動藥,因其具有鎮靜、抗焦慮和鎮痛作用而被廣泛應用。
超聲引導下腋路臂叢神經阻滯輔助神經周圍注入右美託咪定,可顯著延長感覺阻滯時間並縮短起效時間,同時,應注意短暫性心動過緩和低血壓的風險。
研究表明,右美託咪定(0.5-1.0 μg/kg)作為腋路臂叢神經阻滯的佐劑延長了術後鎮痛的持續時間,並呈劑量依賴正相關,認為右美託咪定理想劑量為1.0μg/kg。而又有研究表明,右美託咪定作為局麻藥佐劑的最佳使用劑量仍需進一步研究。
地塞米松被用作局麻藥佐劑,用於周圍神經阻滯。神經周圍和經靜脈注射地塞米松用於外周神經阻滯時具有同等的鎮痛效果。
行內收肌管阻滯實施前交叉韌帶關節鏡手術,與單純使用布比卡因比較,局麻藥新增地塞米松可提供更長的術後鎮痛時間,且減少術後鎮痛藥物的使用。
研究表明,地塞米松經靜脈給藥可延長AN阻滯時間。無論是經靜脈還是神經周圍注射地塞米松,均不延長羅哌卡因感覺阻滯時間。
迄今為止, 尚未闡明地塞米松對局麻藥作用的確切機制。另外,有證據顯示,使用地塞米松有誘發周圍神經毒性的風險。因此,地塞米松用作局麻藥的佐劑仍存在爭議。
06
UGBAN的臨床應用及侷限性
近年來,隨著超聲技術的發展,影象質量、解析度以及便攜性均得到了飛速發展。超聲引導下穿刺術可以實時監測到穿刺針進針路線以及目標神經周圍的結構,最大程度減少損傷神經或血管等。
使用超聲三維(3D)和四維 (4D)技術,可以幫助提高穿刺成功率並降低局麻藥對患者的損傷 。
在超聲引導下將1.5%甲哌卡因20ml注入PCHA平面的AN周圍,該方案為三角肌膿腫切開引流提供良好的肩部面板區域以及包括三角肌在內的較深組織的鎮痛,表明該部位手術實施UGBAN優於肌間溝阻滯或使用鎮靜藥。
在肩部手術中,神經阻滯有一定的優越性。選擇性 AN 阻滯用於關節鏡下肩峰下減壓的方式有一定的鎮痛效果,但是這種效果不可預測,可能與試驗樣本量小有關, 也可能與AN肩關節分佈變異有關。
在肩關節關節鏡術後即刻,肩胛上神經聯合AN阻滯在減少術後疼痛和阿片類藥物的使用方面不如肌間溝臂叢神經阻滯,但呼吸困難和主觀不適的發生率較低。
隨著阻滯效果的消失,疼痛評分和對阿片類藥物需求的差異逐漸減小,術後第 1晚和 24h後疼痛評分無明顯差異。UGBAN用於肩部手術圍術期鎮痛需要進一步研究。
回顧性分析78例接受UGBAN實施貴要靜脈吻合術患者,發現AN阻滯前後貴要 靜脈直徑差異有統計學意義,並提出該技術是血管通路的有效選擇。
誤傷血管
AN和PCHA是透過QS的兩個重要解剖結構,而透過三邊孔的重要結構是旋肩胛動脈。因此,應避免將旋肩胛動脈識別為PCHA。通常透過識別血管間接識別AN,因而在穿刺過程中,應避免損傷到血管。
研究認為,PCHA刺激會導致動脈血栓形成或動脈瘤, 並有栓子形成引起遠端缺血而出現症狀。實施區域性神經阻滯時,為了預防局麻全身毒性,建議使用小劑量,分次給藥, 在使用羅哌卡因和左旋布比卡因等低毒性藥物時,應進行回抽試驗。
誤傷神經
AN損傷通常是因外源性或醫源性造成 ,臨床表現為肩部不適、活動範圍受限,甚至三角肌萎縮,透過肌電圖檢查予以明確診斷,提示操作過程中應避免損傷AN。
對9例用於治療單純性AN損傷而接受肱三頭肌運動支移植術的患者進行至少22個月的隨訪並評估所有患者的肩外展情況,發現所有患者肩外展均恢復≥90° (平均137°)且肘部活動沒有明顯減弱。
07
小 結
隨著對AN及周圍組織解剖結構和超聲下解剖學特點的深入認識,UGBAN為圍術期提供針對性更強、全身影響更小的鎮痛方式,可以聯合肩胛上神經阻滯,也可以單獨應用, 該方法將更多被應用於三角肌及肩部鎮痛和治療QS綜合徵等。
參考文獻: 楊雄眺. 彭小敏. 劉先保. 超聲引導下腋神經阻滯的研究進展[J]. 臨床麻醉學雜誌, 2021, 37(6): 664-666.
【來源:中國網醫療頻道】