本篇將繼續銜接上一篇文章(神經系統疾病的指明燈——biomarker)介紹生物學標記物在神經系統具體的疾病中的應用情況。眾所周知,神經系統結構和功能複雜,對其致病機制的探索造成困難。而相關檢驗檢查,如頭顱MRI、腦脊液(CSF)和血液學檢驗結果對於疾病的診治帶來巨大的幫助。此類生物學標記物目前正在神經系統疾病的診治中扮演了“指明燈”的角色。
本文為作者授權醫脈通釋出,未經授權請勿轉載。
阿爾茨海默病(AD)
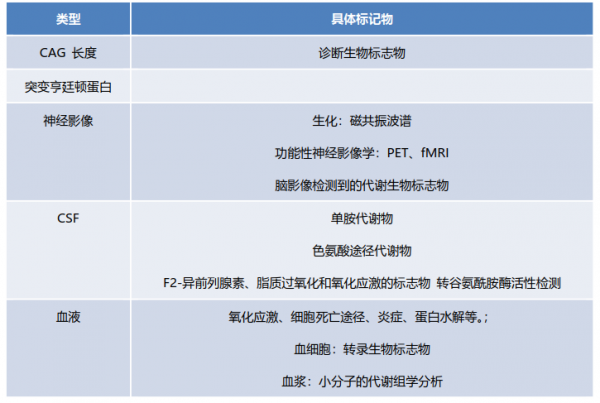
與AD相關的多個生物學標記物正在被研究,包括基於體液的生化檢查、基因組學和腦影像的標記物。一項研究表明,腦基因表達和DNA甲基化失調與腦組織的改變(腦萎縮)有關,從而可提示腦老化。
➤腦影像學生物標誌物
臨床可用的AD生物標誌物技術包括MRI和PET。MRI可現實患者早期階段的海馬體體積減少,晚期的腦萎縮。PET可透過放射性藥物現實完整大腦中的a β沉積,有助於AD症狀前診斷。11C-PiB(Pittsburg compound B)-PET被認為是澱粉樣蛋白影像的金標準,但因研究存在異質性、準確性不明以及高成本,目前尚未被納入臨床應用。FDA建議使用Florbetapir-PET、Florbetaben-PET和Flutemetamol-PET來替代11C-PiB-PET。
➤血漿蛋白生物標誌物
對AD早期患者與健康對照組的血漿樣本透過蛋白質組學技術-二維差異凝膠電泳,結合基質輔助鐳射解吸電離飛行時間串聯質譜技術進行分析比較後發現,載脂蛋白A-4和纖維蛋白原γ鏈被發現在輕症AD患者的血漿中上調,提示這些蛋白表達水平的改變可作為早期疾病診斷的候選生物標誌物。
生物標誌物在AD早期診斷中具有重要作用,包括CSF中的Aβ1-42、T-tau、P-tau,MRI提示的基線海馬體積小,以及Aβ-PET中的異常徵象。大腦中Aβ沉積是AD早期病理表現,可在其臨床症狀出現前幾年甚至幾十年出現,而識別Aβ沉積的唯一有效方法是Aβ-PET成像或CSF 中的Aβ 檢測。根據AD病理生理過程,其早期可用於檢測的生物學標記物可分為用於提示Aβ病理(Aβ-PET提示異常代謝,CSF Aβ 水平下降),以及提示神經元退化的生物學標記物(CSF tau水平增加,FDG-PET提示FDF攝取減少、結構MRI提示腦萎縮)。此外,基於生物標誌物的預後模型可在個體水平上確定輕度認知障礙患者的表現的任何型別的痴呆。
帕金森病(PD)
在過去的20年裡,在識別和評估帕金森病的生物標誌物方面已經取得巨大的進展,但目前尚無完全有效的生物標誌物(表1)。PD患者大腦中發現的嗜酸性包涵體(路易小體)與黑質異常一起成為該病公認的病理生物標誌物,而多巴胺轉運蛋白是FDA承認的PD臨床試驗的分子神經影像生物標誌物。黑質紋狀體多巴胺能系統的放射性示蹤劑成像有助於分析PD的發生發展,預測預後;而嗅覺的進行性變化被認為是膽鹼能去神經和認知能力下降的生物標誌物。遺傳已被明確為PD的病因之一,在運動症狀出現時影像學評估多巴胺能生物學標記物丟失,結合病理生物學和分子遺傳機制的生物學標記物,以及發病和疾病進展期間臨床症狀的異質性有助於全面繪製PD的風險和進展。疾病發生前的生物標記檢測是另一個挑戰。多個蛋白組學標記物的聯合使用有助於區分PD與其他疾病。
表1 PD相關生物學標記物
HD主要透過基因檢測識別,相關的生物學標記物也可用於疾病的診斷與預測(表2)。HD蛋白檢測非常重要,檢測HD蛋白水平、其物理狀態、蛋白水解產物,或其與其他分子的相互作用都將具有不同的價值,尤其是作為藥效學指標。
表2 HD相關生物學標記物
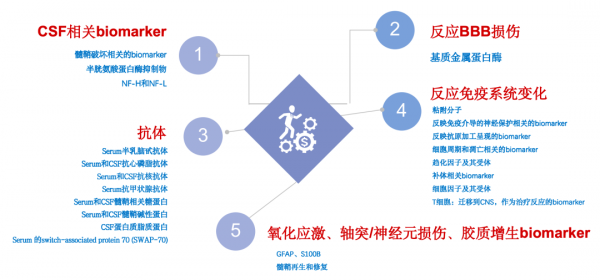
影像學生物標誌物在MS診斷及疾病預測過程中起重要作用,已被用作新療法臨床試驗的替代生物標誌物。早期MS研究顯示,MRI上新發炎症活動發生率比臨床事件高7-10倍;Gd+病變中檢測到的活動性炎症的存在與更高的復發活動有關。Gd+增強病灶的數量和體積是MS短期殘疾進展最可靠的MRI 生物標誌物之一,但目前仍缺乏可用於長期結果預測的可靠的生物標誌物。此外,在III 期臨床試驗中,除降低複發率或減緩殘疾進展的主要結果指標外,MRI檢測到的病變負荷變化仍是重要的次要結果指標。值得注意的是,除目前常用的MS疾病活動性生物學標記物外(全腦萎縮和T2高訊號病變),皮層脫髓鞘並在,即軟腦膜下、皮質內和白皮質病變,可能是疾病進展的生物標誌物。
在MS病理生理過程中,包括神經炎症、脫髓鞘、軸突損傷、神經變性和參與這一複雜疾病過程的修復機制,多個蛋白作為MS的生物學標記物被研究,包括神經絲、tau、14-3-3蛋白質、N-乙醯天冬氨酸(NAA)和Nogo。
卒中
對於急性卒中而言,快速準確地識別疾病潛在病理機制非常重要。影像學技術對於疾病的診斷十分關鍵,如CT或MRI進行腦成像,使用CT血管造影、多普勒或磁共振血管造影等進行血管成像。而可用於反映疾病過程(如腦缺血)表現的血液生物標誌物目前也是研究熱點。
表3 卒中相關生物學標記物型別及意義
生物標誌物可用作TBI的診斷、預後和監測輔助手段,特別是在神經重症監護中。同時,生物標誌物可根據損傷的嚴重程度對患者進行分層,預測不良的次要事件或結果,並監測治療干預的有效性。血清生物學標記物與CSF相比具有多種優勢,包括易於獲取和降低患者風險。此類生物標誌物仍需進一步臨床驗證,並探討其作為開發神經保護療法的潛在靶標的價值。
表4 TBI的生物學標記物
癲癇發作的型別和病因繁多,除腦電圖外尚無通用的生物標誌物。一些生物學標記物能檢測出以癲癇為表現的疾病。除了監測癲癇發作和治療反應外,沒有特發性癲癇的特徵生物學標記物。需要癲癇和癲癇持續狀態的診斷生物標誌物來支援臨床檢查、腦電圖和神經成像。與標準的癲癇治療試驗相比,癲癇預防試驗更復雜、更冗長、更昂貴,使用生物標誌物可能是解決這些問題的一種方法。尋找可靠的癲癇生物標誌物將是癲癇治療的一個重大進展。
表5 癲癇相關生物學標記物的分類
在一項病例對照研究中,與發作性偏頭痛和無頭痛對照組患者相比,慢性偏頭痛患者的紅核和導水管周圍灰質鐵沉積增加。使用 3T MRI 和 NIH 軟體平臺 ImageJ 測量的導水管周圍灰質中的含鐵量可正確識別出慢性偏頭痛患者,並且與內皮功能障礙和BBB的生物標誌物升高有關。
肌萎縮側索硬化(ALS)
遺傳可能在少部分ALS中起作用,ALS的檢測基於生物流體的表觀遺傳變化將使基因組資訊能夠用於疾病診斷。而必需元素缺乏和有毒金屬過量可能是ALS的病因之一。
總結
生物標誌物在個性化神經病學發展中的起了重要作用,包括:有助於疾病的早期診斷並促進治療的最佳化;提供治療靶點加速適合個體化治療的新藥的發現; 經驗證的生物標誌物在個性化治療的臨床試驗中的作用;基於生物標誌物的藥物療效監測將指導疾病的個性化管理。總體而言,神經系統相關生物學標記物是未來神經病學發展的方向之一,對於疾病的診斷、機制的探索、治療反應的預測等具有重要作用。
參考文獻:
1、Bain L, Keren NI, Posey Norris SM. Biomarkers of neuroinflammation. Proceedings of a workshop. Washington, DC: The National Academies Press, 2017.
2、Bazarian JJ, Biberthaler P, Welch RD, et al. Serum GFAP and UCH-L1 for prediction of absence of intracranial injuries on head CT (ALERT-TBI): a multicentre observational study. Lancet Neurol 2018;17(9):782-9.
3、Bigot-Corbel E, Lanore A, Raulet C, et al. [SARS-CoV-2 and neurological disorders: the relevance of biomarkers?] Ann Biol Clin (Paris) 2021;79(1):7-16.
4、Bonomo R, Cavaletti G, Skene DJ. Metabolomics markers in neurology: current knowledge and future perspectives for therapeutic targeting. Expert Rev Neurother 2020;1-13.
5、Jain KK. Textbook of Personalized Medicine, 3rd ed. Cham (Switzerland): Springer, 2021.
6、Jain KK. The Handbook of Biomarkers, 2nd ed. New York: Springer, 2017.