哈工大全媒體(鄭善亮 文/圖)近日,我校生命學院胡穎教授研究團隊在腫瘤細胞內質網鈣穩態調控機制方面取得重要進展。相關內容以研究論文的形式發表於《美國國家科學院院刊》(PNAS),論文題目為《iASPP透過抑制Gp78介導的TMCO1降解維持Ca2+穩態促進腫瘤生長和耐藥》(iASPP suppresses Gp78-mediated TMCO1 degradation to maintain Ca2+ homeostasis and control tumor growth and drug resistance)。
鈣離子是細胞內重要的第二信使,參與著一系列生命活動過程,對維繫細胞生理功能具有重要意義。近年來,鈣穩態調節蛋白在腫瘤發生和發展中的作用得到越來越廣泛的關注。內質網是細胞內最重要的鈣庫,定位在內質網的鈣離子通道蛋白TMCO1是細胞應對內質網鈣過載,維持鈣穩態的關鍵分子。該基因變異可導致青光眼或顱面畸形、骨骼發育異常和智力殘疾等病理變化。然而,TMCO1是否在腫瘤中發揮作用卻尚未明確。
胡穎教授研究團隊透過生物資訊學分析發現,TMCO1蛋白在多種腫瘤患者的組織標本中高表達,進一步透過腫瘤細胞模型以及裸鼠成瘤模型研究發現抑制該基因表達可有效阻滯腫瘤的惡性增殖,並特異性地提高了腫瘤細胞對鈣訊號依賴性藥物的敏感性,提示TMCO1可以作為腫瘤治療或聯合治療的新的分子靶點。進一步的機制研究則揭示了TMCO1在腫瘤中高表達的分子基礎,為靶向該基因治療腫瘤提供了線索。研究發現,TMCO1的mRNA水平在多種腫瘤組織中並未呈現出明顯升高的態勢,其蛋白水平的升高主要是由E3連線酶Gp78介導的TMCO1降解受阻所致。團隊成員透過質譜分析技術篩選到了Gp78的活性調控因子——癌基因iASPP。分析發現,iASPP可與TMCO1競爭性結合Gp78,進而抑制了Gp78對TMCO1的降解活性。團隊基於該機制,發現特異性抑制iASPP表達可有效抑制TMCO1,影響鈣穩態,並達到抑制腫瘤生長和提高化療敏感性的作用。研究明確了iASPP-Gp78/TMCO1軸透過調控鈣穩態促進腫瘤生長,導致腫瘤耐藥的新機制,豐富並拓展了鈣穩態參與腫瘤惡性表型形成的科學觀點,為打破鈣穩態治療腫瘤提供了重要的靶點和潛在的干預策略。
胡穎團隊一直致力於腫瘤耐藥分子機制研究,為高效抗癌、建立預測腫瘤患者治療響應程度的分子標誌物以及實行個體化治療方案提供科學依據。
該研究得到自然科學基金委專案經費支援。生命學院博士生鄭善亮為第一作者,胡穎教授為通訊作者。生命學院博士生趙東、張文馨,副研究員王星文參與其中。該研究獲得華大基因侯桂雪博士、林梁博士,中國科學院動物研究所唐鐵山研究員、博士生趙松,哈爾濱醫科大學腫瘤醫院李慄醫生的大力支援。
原文連結:
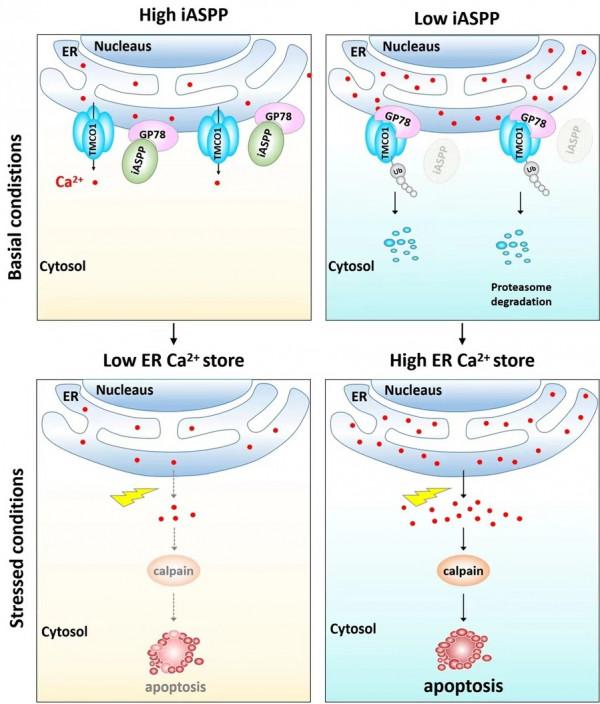
iASPP-Gp78/TMCO1軸透過調控鈣穩態促進腫瘤生長導致腫瘤耐藥的模式圖
【來源:哈爾濱工業大學新聞網_學校要聞】