植入型心律轉復除顫器臨床應用中國專家共識(2021)[J]. 中華心律失常學雜誌, 2021, 25(4) : 280-299. DOI: 10.3760/cma.j.cn.113859-20210315-00054.
通訊作者:
宿燕崗,Email:[email protected];
黃德嘉,Email:[email protected];
張澍,Email:[email protected];
摘要
心臟性猝死(SCD)愈發成為臨床和公共衛生問題。植入型心律轉復除顫器(ICD)是目前預防SCD最為有效的治療措施。目前臨床應用的ICD分為經靜脈植入型心律轉復除顫器(TV-ICD)和全皮下植入型心律轉復除顫器(S-ICD),無論器械本身還是相關臨床研究近年都得到了長足進展。ICD對SCD的預防包括二級和一級預防,符合SCD一級預防或1.5級預防的人群遠多於二級預防,且相關臨床研究及獲益證據也更加充分。針對術後引數設定的多個臨床試驗對ICD診斷和治療引數個體化調整提供了普適性的原則。本共識將ICD適應證按SCD一級預防和二級預防以及不同疾病(如缺血性和非缺血性等)分別進行了闡述。針對ICD不同型別(單腔、雙腔、三腔及S-ICD)的選擇及除顫閾值測試分別進行了推薦。ICD術後隨訪至關重要,依據相關臨床研究結果提出了針對心動過緩起搏引數、心動過速診斷和治療引數設定的共識。此外,對ICD植入注意事項及系統故障處理原則也提出了指導性意見。
一、前言
心臟性猝死(sudden cardiac death,SCD)是目前主要的公共衛生問題之一,其定義是指由於各種心臟原因引起的突然發生、進展迅速的自然死亡,死亡發生在症狀出現後1 h內。心電監測技術顯示,SCD多數由心室顫動(室顫)引起,大部分患者先出現室性心動過速(室速),持續惡化發生室顫,由於不能得到及時有效的除顫治療而發生死亡。冠心病是SCD最主要的病因,文獻報道有20%~25%的冠心病患者以SCD為首發症狀,發生過心肌梗死(心梗)的患者,其SCD的發生率比正常人高4~6倍[1]。此外,心肌病和遺傳性心律失常患者也是SCD的高危人群。
SCD發病突然,病情極其兇險,而且大多發生在院外,搶救成功率極低,即使在歐美髮達國家也僅為5%[2],在中國甚至不到1%[3-4],患者常常因為得不到快速、有效的心肺復甦而失去生命。因此,識別SCD的高危人群並進行積極的預防,對於降低SCD的發生率和病死率具有重要意義。植入型心律轉復除顫器(implantable cardioverter defibrillator,ICD)的問世對於預防SCD無疑具有跨時代意義,多項大型臨床試驗證據已經充分證實ICD是目前預防SCD最為有效的治療措施[5]。隨著ICD療法的進展,特別是近年來國內外重要臨床研究的陸續公佈[6-7]和新的ICD技術的應用,美國心臟病學會(ACC)/美國心臟協會(AHA)/美國心律學會(HRS)於2017年釋出了《室性心律失常及心臟性猝死防治最新指南》[8],而國內亦公佈了《2020室性心律失常中國專家共識(2016共識升級版)》[9]。鑑於此,有必要對2014年制定的《植入型心律轉復除顫器治療的中國專家共識》[10]進行更新。
此次專家共識將植入ICD的適應證推薦級別分為以下3類:
Ⅰ類適應證:根據病情,有明確證據或專家們一致認為ICD治療對患者有益、有用或有效。相當於絕對適應證。
Ⅱ類適應證:根據病情,ICD治療給患者帶來的益處和效果證據不足或專家們的意見有分歧。Ⅱ類適應證中又進一步根據證據和/或觀點的傾向性分為Ⅱa(意見有分歧傾向於支援)和Ⅱb(支援力度較差)兩個亞類。相當於相對適應證。
Ⅲ類適應證:根據病情,專家們一致認為ICD治療無效,甚至某些情況下對患者有害,因此不需要、不應該植入ICD,即非適應證。
其中證據水平分級(level of evidence,LOE)採用新的分類方法:
A級證據:來自一項以上高質量的隨機對照試驗(randomized controlled ttrial,RCT)的證據;高質量RCT的薈萃分析;一項或以上由高質量註冊研究證實的RCT。
B級證據又分為:B-R級(randomized,隨機),來自一項或以上中等質量的RCT證據;中等質量RCT的薈萃分析;B-NR級(nonrandomized,非隨機),來自一項或以上設計及執行良好的非隨機、觀察性或註冊研究或上述研究的薈萃分析。
C級證據又分為:C-LD級(limited data,有限資料),設計或執行有侷限的隨機或非隨機觀察性或註冊研究或上述研究的薈萃分析,對人類受試者的生理或機制研究;C-EO級(expert opinion,專家意見),基於臨床專家經驗的共識。
二、心臟性猝死的流行病學
SCD是一種較為常見的臨床和社會公共問題。有資料顯示全球每年SCD發生大概為370萬[11],但實際上許多國家的SCD資料並不清楚,不同地域報道的SCD的發生率各不相同[12]。
心血管疾病流行病學及人群研究的方法是在20世紀40年代至50年代由Dawber等在弗萊明翰心臟研究(Framingham Heart Study)和Keys等在7國研究(Seven Countries Study)中建立起來的[13]。但這些回顧性的資料評估是基於預設院外死亡是SCD大致推斷的。該方法對認定SCD的敏感性好,但缺乏特異性,故而會高估SCD發病率。相反,因SCD的時間定義是從症狀出現後1 h內,而嚴格的時間限定標準又可導致SCD病例數丟失,加上可能會排除了許多無見證人的SCD病例,故SCD的發生率又有可能被低估。因此,不同的資料來源、SCD定義以及病例估算及診斷方法的差異,導致了不同研究中SCD的發病率範圍跨度較大。
來自美國1998年的人口動態統計資料顯示:黑種人、白種人、美國印第安人/阿拉斯加土著人以及亞洲/太平洋島民的年SCD發生率分別是0.05%、0.041%、0.026%和0.021%[14]。因此,SCD的發生率存在明顯的人種差異。現將主要國家/地區報道的SCD資料彙總(表1),以便我們對全球主要地區的SCD流行病學狀況有個較為全面的瞭解。
我們國家SCD的流行病學資料主要源自於2009年的研究報道[3]。該專案採用人群監測的方法,從我國4個地區(北京、廣東、新疆和山西)選擇了共67.8萬人,監測時間從2005年7月1日至2006年6月30日。SCD發生率約為0.042%。以13億人口計算,我國每年約有54.4萬人發生SCD,發生率雖然低於美國,但考慮人口基數,SCD總人數位居全球各國之首。
心肌病、遺傳性心律失常病、冠狀動脈起源異常等是35歲以下青少年SCD的主要病因,而冠心病、心肌病則是35歲以上成人SCD的最主要病因。在血運重建的時代,雖然急性心肌梗死(AMI)後SCD的發生率有所降低,但其佔全因死亡率的構成比仍然高達24%~40%,依然是AMI後最常見的死因[15]。一項來自德國和芬蘭的研究證實:血運重建能降低AMI患者SCD風險,在所有最佳化治療方案中,血運重建對降低SCD的貢獻最大[16]。但CREDO-Kyoto註冊研究則顯示在裸金屬支架時代,血運重建的方式[經皮冠狀動脈介入術/冠狀動脈旁路移植術(PCI/CABG)]對於SCD的發生率沒有影響[17]。來自丹麥的一項研究納入了2 804例行直接PCI的患者,平均隨訪4.7年[18]。在院外死亡原因中,SCD位居第一,超過其他所有心源性死亡的總和。而STICH研究中,接受CABG完全血運重建的缺血性心力衰竭(心衰)患者5年SCD累計發生率為8.5%[19]。由此可見,即便進行了完全血運重建,缺血性心臟病患者仍有較高的SCD發生率,因此,冠心病患者SCD的防治工作仍充滿挑戰。
三、植入型心律轉復除顫器的發展歷程
目前,用於臨床的ICD分為兩大類:經靜脈植入型心律轉復除顫器(transvenous ICD,TV-ICD)和全皮下植入型心律轉復除顫器(subcutaneous ICD,S-ICD)。
20世紀60年代後期,美國Mirowski醫生最先提出了用植入型除顫器轉復室顫的設想[20],並於1969年在犬身上進行實驗成功;1972年,Mirowski等與美國匹茲堡Medrad公司合作,成功研製了可臨床應用的植入型自動除顫器(automatic implantable defibrillator,AID)。1980年2月Mirowski和他的同事在美國約翰霍普斯金大學醫院採用開胸手術的方法植入了世界上第1臺AID[21]。1985年美國食品藥品監督管理局(FDA)批准其用於臨床。1988年經靜脈除顫導線第1次應用於臨床,避免了開胸手術;隨後開發了具有程控功能的第2代ICD(Ventak. P,美國CPI公司生產);1989年第3代ICD開始用於臨床,它的最大特點是能夠分層治療(tiered therapy),即抗心動過速起搏(antitachycardia pacing,ATP)、低能量心律轉復和高能量電除顫,不但減輕了患者的痛苦,還具有多項引數程控功能。1995年雙腔ICD問世,可提供DDD或DDDR起搏,並能提高ICD對持續性室性快速心律失常識別的特異性,一定程度上減少了誤識別和不適當放電。進入21世紀後,經靜脈ICD又取得了兩個重要發展:一是隨著電子裝置的進展,帶有遠端監測功能的ICD進入臨床,可遠端、定時及實時對ICD及患者進行監測,完善了患者的術後管理;二是心臟再同步治療除顫器(CRT-D)的廣泛應用,它除了預防SCD外,同時還能改善伴有心室收縮不同步的心衰患者的心功能。
TV-ICD的除顫導線需透過靜脈系統植入右心室。長期臨床觀察發現,TV-ICD可出現導線相關感染、導線脫位、三尖瓣損傷、靜脈通路閉塞、血栓形成和導線拔除困難等諸多問題和併發症[22]。S-ICD是第1個可不在心臟內放置電極導線而具有感知和除顫功能的新型除顫治療系統。Bardy等[23]於2001年開始進行S-ICD人體試驗研究,第1代S-ICD於2009年獲得歐盟CE(European Conformity)認證、2012年獲得FDA認證並逐漸開始應用於臨床。S-ICD的導線與脈衝發生器均埋於皮下,除顫電極置於與胸骨中線平行的胸骨左緣或右緣處,近端感知電極位於劍突附近,遠端感知電極置於胸骨柄旁;脈衝發生器則置於左腋下前鋸肌與背闊肌之間。除顫導線不直接接觸心臟及相關靜脈,進而避免了導線導致的靜脈及心臟相關併發症。第2代S-ICD(EmblemTM,美國波士頓科學公司)於2015年獲得FDA認證,體積明顯變小(90 cm3對60 cm3),使用壽命可達7.3年並具有遠端監測功能。目前S-ICD已發展至第4代(第1代SQ-RXTM、第2代EMBLEMTM、第3代EMBLEMTM MRI、第4代S-ICD+無導線起搏器)。
S-ICD最大的問題是捨棄了傳統ICD的起搏和ATP功能,因此,不能用於需要起搏或ATP的患者。2018年7月研發成功了靜脈外心律轉復除顫器(extravascular ICD,EVICD,美國美敦力公司),與S-ICD的最大不同是其除顫電極導線置於胸骨後左緣、心包的表面(透過劍突下穿刺建立隧道)。EVICD除具有除顫功能外,還可進行心外膜起搏和ATP治療。在澳大利亞和紐西蘭首次進行了人體臨床試驗,將於2021年完成。EVICD的第2個臨床試驗2019年6月在美國、加拿大等地24家醫院進行,預計2022年12月結束。
四、植入型心律轉復除顫器的臨床試驗
ICD對於SCD的預防包括二級預防和一級預防兩個方面。二級預防是指對已發生過心臟驟停或發生過有血流動力學障礙的持續性室速患者植入ICD預防再次發生心臟驟停,而一級預防是針對從未發生過心臟驟停的高危人群(包括心梗後、心衰等)植入ICD以預防可能發生的SCD。20世紀末至21世紀初,多個關於SCD二級和一級預防臨床試驗的結果充分證實了ICD治療能有效降低SCD高危患者的全因死亡率。
(一)植入型心律轉復除顫器的二級預防臨床試驗
二級預防的主要臨床研究包括抗心律失常藥物與ICD對比研究(AVID)[24]、加拿大植入型除顫器研究(CIDS)[25]和漢堡心臟驟停研究(CASH)[26](表2)。
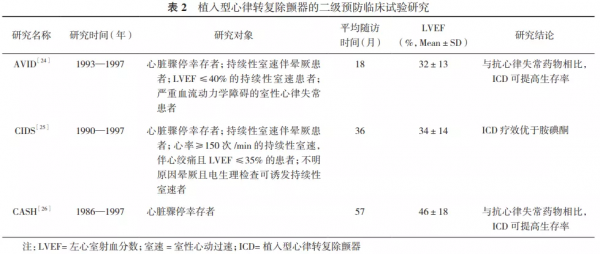
針對上述二級預防臨床試驗的薈萃分析結果表明,對於心臟驟停和有血流動力學障礙的室速患者,ICD可使SCD的相對危險度降低50%,病死率下降25%,尤其對於左心室射血分數(LVEF)<35%的患者獲益更大[27]。
(二)植入型心律轉復除顫器的一級預防臨床試驗
1.多中心自動除顫器植入試驗(MADIT)[28]:
MADIT研究入選心梗超過3周均有非持續性室速(NSVT)的患者,且LVEF<35%、無血運重建適應證。隨機分為傳統藥物治療組和ICD組,平均隨訪27個月。結果發現,藥物治療組病死率39%,而ICD組病死率16%,ICD可顯著降低心梗後高危患者的病死率。
2.多中心非持續性心動過速試驗(MUSTT)[29]:
MUSTT試驗入選了2 202例LVEF≤40%伴無症狀性、NSVT的冠心病患者,其中704例患者在電生理檢查中誘發出持續性室速;隨機分配至抗心律失常治療(藥物治療或ICD治療)組與無抗心律失常治療組,主要終點事件為心臟驟停或心律失常致死。中位隨訪時間39個月,結果顯示接受ICD治療的患者主要終點事件風險較僅藥物治療的患者降低76%(P<0.001),而藥物治療的患者主要終點事件風險和全因死亡風險與無抗心律失常治療組差異無統計學意義。
3.多中心自動除顫器植入試驗Ⅱ(MADIT-Ⅱ)[30]:
MADIT-Ⅱ研究是ICD一級預防里程碑式的試驗,共入選了1 232例心梗超過4周,LVEF<30%、無室速病史的患者,隨機分為傳統藥物治療組和ICD組,平均隨訪20個月,因結果差異非常顯著(ICD組與藥物組比較,總病死率下降了31%)而提前結束試驗。隨後的MADIT-Ⅱ研究8年隨訪結果顯示,一級預防患者植入ICD後存活率可持續獲益[31]。
4.心力衰竭心臟性猝死試驗(SCD-HeFT)[32]:
SCD-HeFT研究是目前患者數量最多的ICD臨床試驗,共入選2 521例左心室功能不全、LVEF≤35%、心功能為Ⅱ或Ⅲ級(NYHA分級)的中度心衰患者,所有患者在接受最佳化心衰藥物治療的基礎上,隨機分為3組:安慰劑組、胺碘酮治療組和ICD組。結果發現,在隨訪期5年內,安慰劑組的年病死率為7.2%,ICD治療使病死率降低了23%;胺碘酮組病死率與安慰劑組差異無統計學意義。由此提示,ICD治療能夠延長心衰患者的生存時間,降低LVEF≤35%的中度心衰患者的病死率。
5.非缺血性心肌病(NICM)ICD治療試驗(DEFINITE)[33]:
DEFINITE試驗入選了LVEF≤35%,合併頻發室性早搏或NSVT的擴張型心肌病患者,隨機分為傳統藥物治療組和ICD組,平均隨訪29個月。結果提示ICD可顯著降低因心律失常所致猝死的風險。
DEFINITE研究的亞組分析顯示ICD植入時間不同而獲益卻相似[34]。但也有研究提供了不同的證據:首次診斷為NICM的部分患者經最佳化的藥物治療6~9個月後LVEF會增加,因而不再符合ICD的一級預防標準。因此,對於首次診斷為NICM 9個月內的患者,是否需要植入ICD有不同的意見。但多數研究表明,首次診斷為NICM 3~6個月內的患者,其左心室功能才有恢復可能性,6個月後LVEF很難再有提高[35-36]。
6.非缺血性收縮性心衰ICD治療試驗(DANISH)[6]:
DANISH研究是一項多中心、非盲、隨機對照研究,共納入1 116例LVEF≤35%、心功能Ⅱ或Ⅲ級(NYHA分級)[若計劃心臟再同步治療(CRT),心功能可為Ⅳ級]的非缺血性心衰患者,以1∶1的比例隨機分配至ICD組或對照組,平均隨訪67.6個月。結果表明,與最佳化藥物治療相比,ICD能夠有效降低50%的SCD風險,但在降低長期的心血管病因病死率與全因死亡率上差異無統計學意義。亞組分析結果顯示ICD降低全因死亡率與年齡顯著相關,<68歲的年輕心衰患者植入ICD獲益更為明顯,且這些結果與是否植入CRT無關。
7.心肌梗死後40 d內植入ICD的研究:
①AMI後除顫器的應用研究(DINAMIT)[37],為前瞻性、隨機對照的臨床試驗。674例心梗後6~40 d的患者入選,332例患者接受ICD治療。平均隨訪30個月,發現ICD組和非ICD組全因死亡率差異無統計學意義。ICD組能明顯降低心律失常病死率,卻明顯增加了非心律失常病死率。②即刻風險評估改善生存率研究(IRIS)[38],為前瞻性、隨機對照的臨床試驗,入選心梗後5~31 d的患者共898例,其中445例接受了ICD治療。平均隨訪37個月,發現ICD組和非ICD組病死率沒有差別,但ICD組顯著降低了SCD的發生率。
8.血運重建術後植入ICD的研究:
①CABG-Patch研究入選了LVEF≤35%伴訊號疊加心電圖異常並行CABG的患者共900例,隨機分為ICD組和非ICD組,ICD組患者在CABG術中植入心外膜除顫片狀電極,隨訪36個月發現兩組生存率差異無統計學意義,但心律失常性死亡在ICD組下降45%[39]。②其他,一些ICD一級預防臨床試驗(MADIT-Ⅱ、MADIT-CRT和SCD-HeFT)的亞組分析顯示ICD植入時間隨著血運重建的時間延長而獲益增加[40-41]。MADIT-Ⅱ研究的亞組分析中,有951例患者接受了冠狀動脈血運重建,血運重建6個月後植入ICD的患者可額外獲益[41]。
9.瑞典心衰登記處(SwedeHF)前瞻性傾向評分匹配研究[42]:
篩選出16 702例符合歐洲心臟病學會一級預防ICD標準的患者,其中只有1 599(10%)例患者進行了ICD植入,1∶1傾向評分匹配1 305例ICD患者和非ICD患者進行比較。平均隨訪2.64年,ICD可降低1年和5年的全因死亡率。該結論在所有亞組中都一致,包括缺血性與非缺血性心臟病患者、性別、年齡<75與≥75歲患者、較早期與較晚期納入的患者以及有或無心臟再同步治療的患者。
10.歐洲ICD一級預防療效比較研究(EUCERT-ICD)[43]:
該研究是一項前瞻性、非隨機對照、多中心佇列研究。共納入歐洲15個國家、44箇中心的2 247例符合ICD一級預防的缺血性及擴張型心肌病患者,排除擬植入CRT、心功能Ⅳ級(NYHA分級)的患者。其中ICD組1 516例,對照組731例,平均隨訪2.4年,ICD組年病死率5.6%,對照組9.2%(P=0.001 6)。多因素校正後,ICD組全因死亡率較對照組降低27%。亞組分析結果顯示:糖尿病、高齡(≥75歲)患者植入ICD後獲益不明顯。
上述有關ICD一級預防臨床試驗的結果充分證明了對於SCD的高危患者,即使臨床上無室速病史,ICD仍能顯著降低病死率;ICD作為對SCD一級預防的獲益程度超過二級預防。
(三)植入型心律轉復除顫器的1.5級臨床研究
絕大多數SCD高危人群難以有機會接受ICD的二級預防,而ICD一級預防的植入率仍然很低,部分原因是ICD對一級預防患者的益處存在異質性。而SCD-HeFT、MADIT-Ⅱ等研究顯示有暈厥及類暈厥症狀、ICD植入患者常規程控中出現NSVT及頻發室性早搏者更易發生室顫。因此,為更有效篩選真正高危患者及提升ICD的治療效能,由中國專家開創性地提出"1.5級預防"的概念。"1.5級預防"是指在符合一級預防適應證的基礎上,同時滿足以下1項或以上高危因素:①暈厥或先兆暈厥;②NSVT;③頻發室性早搏(>10次/h);④LVEF<25%。Improve SCA研究是一項前瞻性、非隨機、國際多中心臨床研究,也是在發展中國家開展的最大規模的關於ICD預防SCD的前瞻性臨床研究[44]。在全球17個國家或地區的86箇中心共納入符合ICD/CRT-D植入適應證的一級及二級預防患者3 889例,隨訪(20.8±10.8)個月。在隨訪過程中共收集到4 870例ATP或除顫治療的室顫/室速事件,其中86%為恰當治療。結果顯示,1.5級預防組恰當治療率顯著高於一級預防組,接受ICD植入的1.5級預防患者較未植入患者的全因死亡率降低49%[7]。
此外,最近國外也有研究在一級預防患者中應用某些臨床指標以提高患者從ICD中的獲益。EUCERT-ICD的研究結果發現年齡、LVEF、NYHA分級、慢性阻塞性肺疾病等是植入ICD後患者死亡的預測因子[43]。該研究亞組分析顯示夜間呼吸頻率>18次/min的患者從ICD中獲益有限,<18次/min的患者可從ICD中明顯獲益[45]。
(四)有關S-ICD及ICD術後引數設定的臨床研究
1.針對S-ICD的臨床研究:
包括Effortless研究[46]、S-ICD上市後註冊研究[47]和PRAETORIAN研究[48]等,均顯示S-ICD預防SCD與TV-ICD等效,並有減少導線相關併發症的趨勢;開啟SMART Pass程式後誤治療率低於TV-ICD。
2.ICD術後引數最佳化的臨床試驗
(1)專門以診斷引數為研究物件的臨床試驗①延長診斷時間程控策略的有效性和安全性研究(RELEVENT)[49]:共入組324例患者,平均隨訪6個月。結果表明透過延長診斷時間,90%的室性及室上性心律失常可自行終止,ICD放電次數明顯減少(P<0.001),心衰住院率顯著降低(P<0.004),且不增加暈厥及死亡事件。②減少不適當治療的多中心自動除顫器植入試驗(MADIT-RIT)[50]:該研究共入選1 500例ICD一級預防患者,隨機按照1∶1∶1分為傳統程控組、提高診斷頻率組和延長診斷時間組。平均隨訪1.4年,結果顯示與傳統程控設定組相比,提高診斷頻率或延長診斷時間,首次不適當治療分別減少了79%(P<0.001)和76%(P<0.001),病死率分別減少了55%(P=0.01)和44%(P=0.06),而首次暈厥的發生率差異無統計學意義。③避免治療非持續性室性心律失常研究(ADVANCE Ⅲ)[51]:該研究入選了1 902例首次植入ICD的患者,其中75%為一級預防,25%為二級預防。患者按照1∶1隨機分配至延長診斷視窗組和標準診斷視窗組。平均隨訪1年後發現,與標準診斷視窗組相比,延長診斷視窗組顯著減少ICD治療,不恰當放電和住院率也顯著降低,而病死率和暈厥率差異無統計學意義。
(2)專門以治療引數為研究物件的臨床試驗①ATP減少放電研究(PainFREE RXI)[52]:共入選220例首次植入ICD的冠心病患者,平均隨訪6.9個月。結果顯示ICD患者中快頻率室速(FVT,診斷頻率為188~250次/min)常見,ATP可以有效治療約75%的FVT事件,其加速或暈厥風險較低。②比較經驗性ATP與放電兩種方式治療自發的快速室速研究(PainFREE RxⅡ)[53]:也是第1個比較ATP和電除顫對FVT(周長240~320 ms)療效的大規模隨機試驗。入選634例患者,按照1∶1隨機分配到電擊治療組(n=321)和經驗性ATP治療組(n=313)。平均隨訪11個月,結果顯示與電擊治療相比,經驗性ATP治療對於FVT是安全有效的,並能提高患者的生活質量。
(3)以診斷引數及治療引數為研究物件的臨床試驗:①一級預防引數設定評估研究(PREPARE)[54]:是第1個專門探討ICD一級預防引數設定的臨床試驗。共入選700例患者,隨訪時間為1年。該研究的程控策略:a. 避免對頻率較慢的室速進行診斷;b. 避免對NSVT進行診斷;c. 對FVT區應用ATP;d. 開啟室上性心動過速(室上速)鑑別功能,避免將室上速誤診斷為室速/室顫;e. 第1陣高能量電擊(shock)治療。結果表明對於一級預防的ICD患者,策略性程控可以減少ICD的放電次數、心律失常性暈厥和對持續性室速/室顫治療缺失的聯合終點發生率。②標準化和醫生個體化ICD程控的比較研究(EMPIRIC)[55]:旨在評價與醫師個體化的設定方法相比,標準化的ICD程控策略能否在減少ICD放電的同時,保證治療的有效性。共入選900例患者,其中一級預防患者416例,1∶1隨機分組,隨訪時間為1年。結果顯示標準化程控策略顯著減少了發生5次以上電擊的患者數量及住院率,但兩組在全因死亡率、暈厥等方面差異無統計學意義,提示標準化程控策略可行、有效,不增加電擊相關的病死率。③透過程控ICD引數延遲一級預防患者首次放電出現時間的研究(PROVIDE)[56]:入選1 670例一級預防的患者,並按照1∶1隨機分配至試驗組和對照組。與對照組相比,試驗組程控特點為:檢測頻率更高,檢測時間更長,設定更多ATP治療,採用室上速鑑別功能。平均隨訪1.5年,該研究再次證實上述程控策略可以有效減少ICD治療,降低總病死率而不增加心律失常性暈厥事件。
總而言之,透過延長診斷視窗、提高診斷頻率、對於FVT給予經驗性ATP等程控策略,可減少不必要電擊,安全有效,提高患者生活質量,並能降低總死亡率。
五、植入型心律轉復除顫器的適應證
(一)ICD適應證的發展歷程
ICD應用於臨床已有40多年,ICD器械本身及植入技術一直在不斷進步,其適應證也在不斷擴充套件,後者主要是依據大規模多中心前瞻性隨機對照臨床試驗的結果。美國FDA於1980年首次提出,對於有兩次心臟驟停發作病史的倖存者可植入ICD,之後在FDA及相關學會制定的指南中ICD的適應證得以拓寬,但仍侷限於二級預防[57]。直至2002年,隨著MADIT、MADIT-Ⅱ及MUSTT等ICD用於SCD一級預防的大規模隨機對照臨床試驗結果的公佈,ACC/AHA/北美心臟起搏和電生理學會(NASPE)聯合釋出的ICD指南中才將ICD適應證正式由SCD的二級預防擴充套件到一級預防[58,59]。2015年歐洲心臟病學會(ESC)釋出了《室性心律失常治療和心臟性猝死的預防管理指南》,豐富了心梗48 h後至40 d以內這一時間段內的ICD推薦,且首次提出了S-ICD的植入適應證[60]。2017年,AHA/ACC/HRS聯合釋出了《室性心律失常患者的管理和猝死預防的指南》,該指南納入了多項新的ICD預防猝死相關隨機對照臨床試驗證據,且以疾病為單元闡述ICD植入適應證,並提高了S-ICD的推薦級別[8]。
(二)我國ICD適應證的建議
我國關於ICD植入適應證的第1個和第2個專家共識先後釋出於2002年和2014年[61,10],分別主要參照了1998年ACC/AHA和2008年ACC/AHA/HRS制定的相關指南。由於新的臨床研究及相關指南的出臺,有必要對原共識進行更新。本次專家共識是在以往兩個中國專家共識的基礎上,結合2015年ESC和2017年AHA/ACC/HRS的相關指南以及一些最新的臨床研究結果討論制定。考慮既往習慣並參照最新推南推薦,本共識將適應證按SCD一級預防和二級預防以及不同疾病分別進行了扼要的分類和闡述,以利相關從業者查閱、參考。
1.以疾病為單元的ICD適應證推薦。參考2015年ESC及2017年AHA/ACC/HRS關於室性心律失常患者管理和SCD預防的指南,本共識以疾病為單元將ICD適應證用表格形式列出(表3~12)。









2.ICD在SCD一級預防中的推薦。Ⅰ類適應證:①心梗40 d後及血運重建90 d後,經最佳化藥物治療後心功能Ⅱ級或Ⅲ級,LVEF≤35%;或者心功能Ⅰ級,LVEF≤30%(證據水平A)。②既往心梗導致的NSVT,LVEF≤30%,電生理檢查能夠誘發出持續性室速、室顫者(證據水平B)。③非缺血性心臟病患者,經最佳化藥物治療3~6個月後心功能Ⅱ級或Ⅲ級,LVEF≤35%(證據水平B)。Ⅱ類適應證:詳見表3、表5、表7~12。
3.ICD在SCD二級預防中的推薦。Ⅰ類適應證:①非可逆原因導致的特發性室顫或血流動力學不穩的持續性室速,引起心臟驟停後存活者(證據水平A)。②伴有器質性心臟病的自發持續性室速或室顫患者,無論血流動力學是否穩定(證據水平B)。③心梗48 h後發生的非可逆性原因導致的室顫或血流動力學不穩的室速患者(證據水平A),以及血流動力學穩定的持續性單形性室速患者(證據水平B)。④心梗48 h後不明原因的暈厥,電生理檢查能夠誘發出持續性單形性室速患者(證據水平B)。⑤非缺血性心臟病,出現非可逆原因的室速/室顫導致心臟驟停或血流動力學不穩定的持續性室速患者(證據水平A),以及血流動力學穩定的持續性單形性室速患者(證據水平B)。⑥各種離子通道疾病,如出現過心臟驟停或持續性室速,藥物(如β受體阻滯劑)治療無效或無法耐受者(證據水平B)。⑦不明原因的暈厥患者,電生理檢查誘發出血流動力學不穩定的持續性室速或室顫(證據水平B)。Ⅱ類適應證:詳見表4、表6~12。
關於ICD植入的Ⅲ類適應證,因其存在共性,故未以疾病型別分類,推薦如下:①滿足ICD適應證,但患者不能以較好的功能狀態生存1年以上,需要綜合判斷並與患方充分溝通;②無休止室速或室顫,需待室速、室顫控制且病情穩定後再計劃ICD植入;③存在明顯的精神疾病,可能由於ICD植入而加重,或不能進行系統隨訪者;④不合並器質性心臟病及離子通道疾病的不明原因暈厥,且未能誘發室性心律失常;⑤手術或導管消融可治癒的室顫或室速,主要是指無器質性心臟病患者;⑥由完全可逆因素(如電解質紊亂、藥物或創傷)引起的室性快速性心律失常。
六、植入型心律轉復除顫器型別的選擇及除顫閾值測試
(一)型別選擇
1.單腔和雙腔ICD的選擇:
根據2002年ACC/AHA/NASPE和2008年ACC/AHA/HRS指南描述,如果患者需要雙腔起搏治療或者伴有室上性快速心律失常有不恰當放電可能性時,可考慮選擇雙腔ICD治療。目前由於缺乏臨床依據及明確的指南推薦,臨床上對於單腔和雙腔ICD的選擇出現了很大差異,有些中心只植入單腔ICD,而另一些中心則只植入雙腔ICD[62]。
雙腔ICD的優勢在於可提供心房感知和起搏,且能透過觀察房室分離有助於鑑別室速與室上速。但實際上,美國國家心血管資料註冊的ICD資料庫分析顯示,二度、三度房室傳導阻滯僅佔5%,竇性停搏需要心房起搏者佔12%[58]。而隨著現代ICD程控策略的最佳化,心房導線在輔助鑑別室速與室上速方面的優勢逐漸降低。PAPRURE研究入選了100例雙腔ICD患者,隨機程控為單腔或雙腔模式,隨訪1年發現,兩組不恰當治療發生率差異無統計學意義,均為2%[63]。雙腔ICD的劣勢包括增加了手術相關併發症、手術花費、脈衝發生器壽命縮短和心室起搏比例的增高。DAVID研究顯示,在不需要心動過緩起搏的患者中,雙腔ICD組心衰住院率增加,病死率增加,並證實與高比例右心室起搏相關[64]。
2014年HRS/ACC/AHA聯合發表了針對未納入臨床試驗患者植入ICD的專家共識,建議在選擇單、雙腔ICD時,需綜合考慮患者是否有心動過緩起搏適應證、基礎心臟疾病、心功能狀況以及室性心律失常型別等,以選擇適合患者的ICD型別[65]。推薦如下:①症狀性竇房結功能障礙的患者,推薦植入心房導線;②竇性心動過緩和/或房室傳導功能障礙患者,需要使用β受體阻滯劑或其他具有負性變時功能作用的藥物時,推薦植入心房導線;③記錄到二度或三度房室傳導阻滯伴竇性心律的患者,推薦植入心房導線;④由心動過緩誘發或長間歇依賴的室性快速心律失常(例如長QT綜合徵伴尖端扭轉型室速)的患者,植入心房導線有益;⑤記錄到房性心律失常(排除永久性房顫)的患者,可以考慮植入心房導線;⑥肥厚型心肌病患者,若靜息或激發狀態下出現明顯的左心室流出道壓差,可以考慮植入心房導線以透過短AV間期起搏右心室減輕梗阻程度;⑦未記錄到房性心律失常且無其他原因需要植入心房導線的患者,不推薦植入心房導線;⑧永久或長程持續房顫患者,並且不考慮恢復或維持竇性心律,不推薦植入心房導線;⑨非心動過緩誘發或長間歇依賴的室速患者,不推薦植入心房導線。
2.心臟再同步治療除顫器的選擇:
依據相關指南,具有心臟再同步治療起搏器(cardiac resynchronization therapy pacemaker,CRT-P)適應證者(QRS時限>130 ms,LVEF<35%),除非預期生存期<1年,都是ICD的適應證。在器械功能上,心臟再同步治療除顫器(cardiac resynchronization therapy defibrillator,CRT-D)為ICD和CRT的組合,因此理論上講,需要植入CRT者都應植入CRT-D。但目前CRT的相關指南並未對選擇CRT-P或CRT-D做出明確規定。一方面,既往的研究主要是針對CRT-P與藥物以及CRT-D與ICD的對比研究,缺乏CRT-P與CRT-D頭對頭的隨機對照研究證據(僅有的COMPANION研究顯示CRT-D與CRT-P在全因死亡和心衰住院風險上差異無統計學意義[66]),而已有的回顧性研究的結果並不一致[67];另一方面,臨床的淨效應並非全部歸因於器械本身功能的增減,不同病因和心功能都會左右CRT與ICD功能所起作用的權重,加之CRT-D的併發症(除顫導線高故障率、不適當電擊等)和高費用等[68],針對個體患者並非CRT-D一定優於CRT-P。結合2013年ESC起搏與CRT指南中有關CRT-P和CRT-D的推薦意見[69],本共識推薦植入CRT-D的情況:①具有CRT適應證,同時符合ICD二級預防適應證者,推薦植入CRT-D。②具有CRT適應證,即使無ICD二級預防適應證,若滿足以下條件之一者,也優先考慮CRT-D:a.缺血性心臟病;b.心功能Ⅱ級;c.顯著的左心室擴大和更低的LVEF;d.預防SCD作為CRT療法的主要目的;e.預計CRT效果差者(選擇CRT-D至少保證了ICD預防SCD的療效)。③心功能Ⅳ級,預期壽命<1年者不建議植入CRT-D,但需綜合考慮患者意願,與患者共同探討其風險獲益比。
3.全皮下植入型心律轉復除顫器的選擇:
結合2017年AHA/ACC/HRS相關指南[8],S-ICD推薦級別如下:①符合ICD植入標準,但缺乏合適的血管入路或預計感染風險高;目前不需要、預期將來也不需要起搏來治療心動過緩或者終止心動過速;目前無CRT適應證、預期將來也不需要植入CRT的患者(Ⅰ類推薦,證據水平B-NR級)。②符合ICD植入標準,目前不需要、預期將來也不需要起搏來治療心動過緩或者終止心動過速;目前無CRT適應證、預期將來也不需要植入CRT的患者(Ⅱa類推薦,證據水平B-NR級)。③雖然符合ICD植入適應證,但合併心動過緩需要起搏器治療;合併心衰需要CRT治療;或者需要ATP終止室速的患者(Ⅲ類推薦,證據水平B-NR級)。
(二)心室除顫閾值的測試
除顫閾值(defibrillation threshold,DFT)概念於1963年第1次提出,定義為終止室顫所需的最小能量[70]。但是"閾值"這個概念並不適用於臨床實踐中的除顫,此處的除顫閾值只是指除顫成功的機率。
1.TV-ICD的DFT測試方法:
常用的兩種模式為10 J安全範圍法及逐級降低能量測試法。前者是以低於脈衝發生器最大除顫能量至少10 J以上的能量進行除顫,僅需誘發1次室顫,是目前臨床最為常用的方法;逐級降低能量測試法需多次誘發室顫,精確但臨床少用。早期ICD只有除顫功能,僅用於室顫患者的治療,因此,DFT作為ICD植入術中的標準流程以確認ICD的感知和除顫功能,其作用毋庸置疑。隨著ICD適應證的拓寬、臨床應用經驗的積累以及ICD工藝和技術的改進(如ATP、高輸出能量),DFT測試是否仍有其必要性,許多學者產生了不同觀點。
支援DFT測試的理由:①DFT測試是ICD植入過程的標準流程;②DFT測試中發現高DFT可以及時調整,使患者能接受更有效的除顫治療;③較精確的DFT測試,可程控較低的除顫能量,而低除顫能量具有充電時間短、對心肌損傷小和節約電能等優點;④DFT是測試ICD能否正確感知室顫波及除顫系統連線是否正常等的重要判斷依據;⑤自發性室顫者除顫失敗是ICD患者猝死的主要原因。據報道,沒有達到10 J的安全範圍是在雙相波、TV-ICD患者發生SCD的獨立預測因子[71]。若ICD患者出現不明原因死亡,而醫生未按標準流程進行DFT測試,可能使醫生處於不利和被動的局面,出現醫學倫理問題[72]。
不支援DFT測試的理由:①誘發性室顫不同於自發性室顫,臨床最常見的需要ICD治療的心律失常是室速而非室顫;②DFT測試成功與否並不能預測臨床除顫功能的成敗;③有研究報道DFT測試與否不影響長期預後[73];④DFT測試有一定風險[74];⑤ICD植入術後發生猝死未必與DFT有關,可以由導線和ICD故障所致,也可以是除顫成功但後續發生電機械分離引起。
SIMPLE(Shockless implant evaluation)研究的主要目的是評價在ICD植入過程中進行DFT測試對患者長期臨床預後的影響[75]。前瞻性、多中心、隨機對照納入2 500例新植入ICD/CRT-D患者,隨機分為DFT組和非DFT組,平均隨訪3年。結果顯示,首次除顫成功率兩組間差異無統計學意義,隨訪期間全因死亡率差異亦無統計學意義。結論為ICD植入過程中,推薦不必常規進行DFT測試。
建議:ICD植入過程中,針對一級預防的患者,推薦不常規進行DFT測試。而對二級預防的患者,可根據患者基礎心臟疾病、心功能狀況以及室性心律失常型別等,由植入醫生決定是否進行DFT測試。
2.S-ICD的DFT測試方法:
目前臨床上多采用15 J安全能量範圍測試法,即以低於S-ICD最大除顫能量(80 J)15 J的能量(65 J)進行除顫。測試前醫生根據需要可考慮X線下再次確認導線和脈衝發生器位置(心影應在脈衝發生器及導線除顫線圈之間)。閉合囊袋及劍突和胸骨柄切口處的皮下組織時,需排盡切口和隧道中的空氣。關閉條件電擊區,電擊區設定為170次/min,開啟電擊後起搏功能(按需起搏,起搏頻率50次/min,最長30 s)。測試時患者處於中度至深度鎮靜或全身麻醉下,以200 mA/50 Hz交流電3~10 s誘發室速/室顫,首次電擊能量為65 J,標準極性;如首次除顫失敗,系統會再次用80 J除顫,如仍未成功,應及時體外電擊復律。DFT失敗患者可嘗試轉化除顫極性,必要時調整脈衝發生器和/或除顫電極位置。
目前用於評估S-ICD安全性及有效性的大型臨床研究中,絕大多數案例均接受DFT[46,47,76],尚無S-ICD不行DFT測試的大型臨床研究資料。正在進行的前瞻性、隨機對照研究PRAETORIAN-DFT有望為此提供資料支援。
建議:S-ICD植入過程中,推薦常規進行DFT測試。但在臨床實際工作中也可根據患者基礎心臟疾病、二級預防或一級預防、心肺功能狀況及鎮靜麻醉可行性等,結合植入時PRAETORIAN評分,由植入醫生決定是否進行DFT測試。
本共識結合2015年HRS/ EHRA/ APHRS/ SOLAECE關於ICD程控和測試專家共識對ICD植入術中DFT測試作出如下推薦(表13)[77]。
(一)植入型心律轉復除顫器的隨訪
對已接受ICD治療的患者進行定期隨訪是ICD治療過程中的重要環節。相對於普通心臟起搏器,加強ICD術後管理顯得尤為重要。一方面,ICD器械本身較為複雜,尤其是針對快速室性心律失常診治的精細演算法和程控;另一方面,植入ICD的患者多伴有較為嚴重的心臟疾病。透過隨訪可瞭解ICD治療的效果,及時發現和處理手術及ICD本身可能出現的併發症及故障,瞭解ICD是否處於最佳工作狀態,使患者得到最優治療效益[78-79]。
1.隨訪目的:
ICD隨訪的主要目的有4個方面。①瞭解患者情況;②評價器械狀況;③關注疾病變化;④相關溝通。具體包括評估器械效能和最佳化引數設定、識別和校正ICD系統的異常情況、預測電池壽命並確定擇期更換時機、儲存患者及ICD程控引數變化的記錄並建立資料庫,以及對患者和家屬進行宣傳教育。
2.隨訪方式和頻度
(1)隨訪方式:ICD的隨訪方式主要有診室隨訪和遠端隨訪兩種。①診室隨訪:診室隨訪是目前主要的隨訪方式,即由專科醫師和/或從事ICD的醫護技術人員在診室進行檢測的隨訪方式。透過程控儀詢問讀取ICD資料和資訊,同時瞭解患者的病情、用藥和生活工作情況,最後決定是否調整器械引數設定以及其他治療措施。②遠端隨訪:遠端隨訪能提供及時、準確的ICD工作資料和資訊,某種程度上具有與傳統診室隨訪相當的功能[80-81]。遠端詢問可以減少患者來醫院就診次數,增加隨訪頻度,尤其適於路途遙遠、交通不便的患者;而遠端監測可及時發現器械及患者發生的問題,減少不適當放電,並降低ICD患者住院率和病死率[82-86]。當然,遠端隨訪亦有其侷限性,例如當患者病情有變化或不穩定時(ICD患者多存在器質性心臟病及心衰),遠端隨訪不能做到針對疾病本身,包括器械引數設定的及時調整。因此,ICD患者仍然需要每半年至少1次的診室隨訪。
(2)隨訪頻度:出院後隨訪通常分為3個階段。①早期:植入後4~12周內應來院隨訪1次;②中期:依據患者臨床情況,每3~6個月應進行1次診室隨訪或遠端詢問,ICD隨訪間隔通常不應超過6個月;③後期:當ICD接近擇期更換適應證時,應該考慮增加診室或遠端隨訪次數(每次間隔1~3個月);④緊急隨訪:在ICD電風暴或遠端監測出現紅色報警時需緊急隨訪。若懷疑導線或脈衝發生器功能障礙時,應提高隨訪頻度。
3.隨訪內容:
ICD隨訪評估內容應根據患者臨床情況、ICD型別以及患者用藥情況等的不同而異。隨訪應包括但不限於以下內容。①病史採集:注意植入前症狀是否消失、延續或再現,有無被電擊感等;②體檢:檢查囊袋有無紅腫、破潰、導線膨出以及脈衝發生器是否移位等;③起搏心電圖記錄:常規心電圖及動態心電圖記錄有無持續或間歇性起搏、感知功能異常,包括確定是否存在房性或室性快速心律失常等;④X線胸片:確定有無導線移位、斷裂、心肌穿孔以及導線與脈衝發生器連線問題等;⑤程控檢查:ICD儲存資料回顧、起搏感知等引數測試、ICD系統功能狀態、電池消耗情況評估及是否需要進行診斷及治療引數的調整。其中,最為重要的是回顧ICD的事件記錄(主要是心律失常是否出現及頻率等)以及判斷ICD是否為正確識別和治療,並給予相應的引數程控最佳化。
(二)植入型心律轉復除顫器的程控建議
ICD的程控引數設定包括抗心動過緩的起搏設定、心動過速檢測設定和心動過速治療引數設定[77]。
1.抗心動過緩起搏引數的設定:
需根據患者基礎心臟疾病、心功能狀況及存在的緩慢心律失常等,調整相關起搏引數[87]。程控設定要點:①伴有變時功能不全的患者(尤其是年輕或運動量較大患者),需開啟頻率應答功能;②植入單、雙腔ICD的患者,均需透過程控引數調整以達到最小化右心室起搏;③合併肥厚型梗阻性心肌病的患者,將AV間期個體化程控為短於自身PR間期,用盡量多的右心室起搏減輕流出道梗阻;④植入CRT-D的患者,應透過AV間期最佳化增加雙心室起搏比例,並儘可能提升至98%以上。推薦使用自動最佳化AV/VV間期功能,以獲得更窄的起搏QRS時限和更好的血流動力學效果。
2.心動過速檢測引數的設定:
需根據患者室性心律失常發作時的血流動力學改變調整室速識別頻率,避免對頻率較慢的室速給予過度治療。心動過速檢測引數包括基本識別標準和輔助識別標準。基本識別標準包括頻率標準和持續時間標準,用於室速/室顫的初始識別和再識別。輔助識別標準包括突發性、穩定性及形態學標準,用於室速與室上速的鑑別。開啟室上速鑑別功能,有助於避免將室上速誤診為室速/室顫。雙腔ICD還可透過分析P波與QRS波的關係,進行室速與室上速的鑑別。心動過速檢測設定要點:①提高診斷頻率,延長診斷成立間期數以減少適當及不適當治療,無論是針對SCD一級或二級預防。一級預防心動過速診斷成立的標準應當為持續至少6~12 s或30個心動週期,心動過速診斷的下限頻率應當為185~200次/min,二級預防患者的檢測頻率應低於記錄到室速頻率的10~20次/min且不低於188次/min[88-89]。但當患者使用能夠減慢室速頻率的抗心律失常藥物(如胺碘酮)時,要監測室速頻率變化,可能需相應降低ICD的識別頻率。②增強室上速鑑別診斷以及避免感知各種噪聲干擾,提升室上速鑑別診斷頻率區間至200次/min甚至230次/min,關閉室上速鑑別診斷超時功能,能有效降低不恰當治療的風險;對於存在完全性房室傳導阻滯的患者,可不設定室上速鑑別演算法。此外,推薦預先開啟T波過感知識別功能、導線故障早期預警功能及鑑別噪音干擾功能。
3.ICD治療引數的設定:
分為ATP、低能量轉復及高能量除顫。心動過速治療設定要點:①設定充分的ATP治療。對於室速事件推薦無痛性治療,即應首先使用不同策略的ATP治療方案。ATP有兩種基本形式:短陣快速起搏(burst)及周長遞減起搏(ramp)。burst指在同一陣起搏中,周長相等且短於心動過速周長的起搏方式。ramp指在同一陣起搏中,周長逐漸縮短的起搏方式。相比ramp模式,應當優先設定burst模式,以提高ATP終止室速的成功率。離子通道疾病,如長QT綜合徵、短QT綜合徵和Brugada綜合徵等引起的心律失常多為尖端扭轉型室速或室顫,ATP對其終止作用有限。②放電能量合理設定。放電治療可分為低能量電轉復和高能量除顫。若有DFT測試結果,室顫區首次放電能量應至少高出10 J,從第2次放電開始應使用最高能量;若無DFT測試結果,室顫區首次放電能量需程控至最高水平。在所有的室速檢測區都設定電擊治療,以提高終止室速的成功率;室速區首次放電可選用較低的能量,之後的放電也應使用最高能量。室顫區的初始電擊能量應設定為最大除顫能量。放電極性是可程控的另一項引數,其出廠設定在不同的廠家有所不同;若DFT結果較高,可嘗試透過改變放電極性解決。ICD給予治療後可進行再識別,其目的是判斷心律失常事件是否繼續存在以及是否需要發放下一步治療。再識別時一般僅應用頻率標準和持續時間標準,不再採用輔助識別標準,持續時間一般也要短於初始識別時。
4.不同ICD製造商的程控設定推薦:
需要說明的是,這些不一定是製造商推薦的設定,也不一定適用於所有情況。每個患者的ICD程控設定必須依據患者的具體臨床情況,臨床醫師需仔細判斷這些推薦的程控設定是否適合具體的患者。以下就不同ICD製造商的程控設定推薦進行彙總。
(1)美國美敦力公司。①抗心動過緩設定:單腔為VVI 40次/min;雙腔為DDD,可考慮心室起搏管理功能(MVP)±頻率應答;CRT為DDD±頻率應答,房室傳導功能正常伴左束支傳導阻滯(LBBB)患者可考慮Adaptive BiV & LV。②心動過速檢測:無室速病史的患者,室顫區為30/40個心動週期,188次/min;關閉快心率室速區和室速區;室速區監測由程控者自主決定。室速周長已知的患者,室顫區為30/40個心動週期,188次/min;關閉快心率室速區;室速區為24個心動週期,10次/min<室速頻率;室速區監測由程控者自主決定。③心動過速治療:室顫區在充電前ATP治療,開啟ChargeSaver,所有電擊以最大能量電擊(除非有DFT指導)。室速區為Rx1:ATP,≥1陣burst,以室速周長的88%發放8次脈衝,陣間遞減10 ms;Rx2-6:開啟所有電擊。④SVT鑑別診斷:單腔為開啟Wavelet波形鑑別;關閉穩定性和突發性程式;SVT鑑別上限頻率為260 ms(230次/min)。雙腔/CRT-D:開啟PR邏輯和Wavelet波形鑑別;關閉穩定性和突發性程式;SVT鑑別上限頻率為230次/min。⑤避免過感知:開啟導線完整性報警;開啟T波過感知(如果有此功能);開啟右心室導線噪音超時功能(如果有此功能)。
(2)美國雅培公司。①抗心動過緩設定:單腔為VVI 40次/min;雙腔為DDD,可考慮開啟心室自身優先(VIP)±頻率應答;CRT為DDD±頻率應答,若房室傳導功能正常,可考慮開啟SyncAV功能。②心動過速檢測:無室速病史的患者,室顫區為30個心動週期,240或250次/min;室速區2為30個心動週期,187次/min;室速區為監測或根據程控者決定。室速周長已知的患者,室顫區為30個心動週期,240或250次/min;室速區2為30個心動週期,187次/min或10次/min<室速頻率;室速區為10次/min<室速頻率,設為發放治療或監測區。③心動過速治療:室顫區為充電時ATP治療,以室速周長的85%發放8次脈衝,所有電擊以最大能量電擊(除非有DFT指導),第1次電擊能量低於最高放電能量4~6 J。室速區2 ATP治療:≥1陣burst,以室速周長的85%發放8次脈衝,陣間遞減10 ms;開啟重新自適應(最小周長200 ms);開啟所有電擊。室速區與室速區2設定一致,傾向於更多的ATP治療。④SVT鑑別診斷:單腔為開啟遠場形態學(90%,3/10);雙腔/CRT-D,開啟遠場形態學(90%,3/10)、突發性和穩定性程式(滿足以上全部標準,才發放治療);開啟模板獲取時的起搏頻率滯後功能或關閉遠場形態學自動更新(CRT模板自動更新週期為30 d);SVT鑑別上限頻率為230次/min;關閉SVT鑑別超時功能和室速治療超時功能。⑤避免過感知:開啟低頻濾波;開啟右心室SecureSense導線噪音鑑別。
(3)德國百多力公司。①抗心動過緩設定:單腔為VVI 40次/min;雙腔為DDD,可考慮開啟IRS Plus/I OPT±CLS(閉環刺激)或DDD開啟Vp Suppression±頻率應答;CRT為DDD,程控者自主決定開啟DDD-CLS或頻率應答。②心動過速檢測:無室速病史的患者,室顫區為30/40個心動週期(如不能程控,則選擇24/30個心動週期),231次/min;室速區2為30個心動週期,188次/min;室速區1為監測,或根據程控者決定。室速周長已知的患者,室顫區為24/30個心動週期,231次/min;室速區2為30個心動週期,188次/min(或10次/min<室速頻率);室速區1為10次/min<室速頻率,設為發放治療或由程控者決定設為監測區。③心動過速治療:室顫區為開啟ATP One Shot,1陣burst,以室速周長的88%發放8次脈衝,以最大能量電擊(除非有DFT指導)。室速區2 ATP:≥1陣burst,以室速周長的88%發放8次脈衝,陣間遞減10 ms,開啟所有電擊。室速區1與室速區2設定一致,傾向於更多的ATP治療。④SVT鑑別診斷:單腔為開啟MorphMatch波形鑑別;關閉突發性、穩定性和持續室速計時器。雙腔/CRT-D:開啟SMART程式(預設設定或根據室速設定)。⑤其他:開啟導線完整性檢查(如果有此功能);開啟家庭監測(如果有此功能)。
(4)美國波士頓科學公司。①抗心動過緩設定:單腔為VVI 40次/min;雙腔為DDD,可考慮RYTHMIQ或AV搜尋±頻率應答;CRT為DDD±頻率應答,可考慮開啟Smart Delay功能最最佳化AV延遲。②心動過速檢測:無室速病史的患者(a)選擇延遲治療,室顫區為8/10個心動週期,持續5 s,250次/min;室速區為8/10個心動週期,持續12 s,185次/min;室速區1為監測或根據程控者決定。(b)選擇高比例治療:室顫區為8/10個心動週期,持續2.5 s,200次/min;室速區1為監測,或根據程控者決定。室速周長已知的患者,室顫區為持續5 s,250次/min;室速區為持續12 s,185次/min或10次/min<室速頻率;室速區1為10次/min<室速頻率,持續≥12 s發放治療或設為監測區。③心動過速治療:室顫區為開啟QuickConvert到300次/min;所有電擊以最大能量電擊(除非有DFT指導)。室速區為ATP-1:≥1陣burst,以室速周長的84%發放8次脈衝(最小周長200 ms),陣間遞減10 ms;ATP-2:關閉;開啟所有電擊。室速區1:與室速區設定一致,傾向於更多的ATP治療。④SVT鑑別診斷:ICD為開啟RhythmID;CRT-D為開啟突發性/穩定性或RhythmID程式;關閉SRD;SVT鑑別上限頻率:230次/min。⑤避免過感知:可考慮開啟非生理性訊號檢測。⑥其他:開啟每日導線檢測"超出正常範圍蜂鳴音提示"功能;可考慮開啟右心室導線阻抗驟變預警;可考慮開啟右心室起搏百分比預警提示(單腔);可考慮開啟非房室傳導阻滯患者右心室起搏百分比預警提示(雙腔);可考慮開啟CRT起搏百分比預警提示(CRT-D)。⑦S-ICD設定:放電區≥230次/min;條件放電區≥200次/min或10次/min<已知室速頻率;開啟電擊後起搏功能。
八、植入型心律轉復除顫器植入注意事項及系統故障處理
(一)TV-ICD植入手術注意事項:
TV-ICD植入手術過程與普通心臟起搏器植入類似,但亦有所不同。需注意以下問題。
1.術前準備:
術前給患者貼上體外除顫電極片並與體外除顫器正確相聯,以備術中突發室速/室顫事件或DFT測試時ICD不能終止室顫時能迅速從容地進行體外除顫。
2.植入部位:
選擇左側以利電擊時覆蓋更多心肌。如多種原因只能植入右側時,建議術中行DFT測試。
3.囊袋製作:
皮下囊袋製作同普通起搏器。但對於體瘦、胸部皮下脂肪少者(如慢性心衰患者),建議製作肌肉間囊袋(胸大肌與胸小肌之間),以避免術後囊袋過於膨出、區域性面板過緊而發生破潰的風險。
4.導線植入:
選擇腋靜脈或肋間隙較寬處的鎖骨下靜脈穿刺送入除顫導線,避免導線受擠壓磨損造成ICD系統故障;此外,因ICD導線較粗,植入操作需輕柔,避免心臟穿孔。
5.引數測定:
對ICD來說心室感知比閾值更為重要,一般要求R波振幅必須>5 mV,最好能>8 mV;電極導線與脈衝發生器連線後,還應測試高壓阻抗,要求為30~100 Ω。其他引數要求同普通起搏器。
6.DFT測試:
具體參見本共識六、(二)"心室除顫閾值的測試"部分。
(二)S-ICD植入手術注意事項:
S-ICD植入與TV-ICD明顯不同,具體需注意的問題。
1.患者篩選:透過患者立、臥位姿勢收集其體表心電訊號,確定至少存在一個向量被脈衝發生器的心電圖模板所接受,否則不能選擇S-ICD。
2.術前準備:X線前後及側位透視下確定脈衝發生器和導線的植入位置,確保除顫線圈和脈衝發生器將心臟完全覆蓋;位置確定後做好標記。另外,必須貼好體外除顫電極片並與體外除顫器正確相聯。
3.在左腋中線附近尋找到背闊肌和前鋸肌之間的深筋膜層,鈍性分離製作適當大小囊袋。
4.胸骨旁皮下隧道應儘量貼近深筋膜層,確保除顫導線在脂肪組織下。
5.兩感知電極需可靠固定;囊袋內充分止血、幹紗布擦拭清理囊袋並排氣(包括脈衝發生器連線口及各切口內)。
6.DFT測試:具體參見本共識六、(二)"S-ICD的DFT測試方法"部分。
(三)ICD系統故障識別與處理:
ICD治療緩慢心律失常功能部分的故障與處理同普通心臟起搏器,不在此贅述。
ICD對快速室性心律失常診治方面的故障包括不識別、誤識別、不治療或誤治療。其原因可能為器械本身硬體問題或引數設定不當等非硬體問題;此外,患者病情變化亦可能導致ICD頻繁電擊或不治療。相對於普通起搏器,ICD系統故障產生的後果更嚴重,有時是致命的,例如ICD不治療、高DFT或ICD電風暴等。如電擊前有暈厥、黑矇等症狀,電擊後消失,則多提示治療是正確及成功的;如電擊前無任何不適,提示該治療事件可能是誤治療或治療相關引數設定太敏感(不必要治療)。程控分析儀檢查主要透過R波振幅、阻抗和起搏閾值等引數測定,判斷心室感知功能、除顫導線完整性及ATP奪獲心室的有效性等;此外透過程控分析,調閱ICD儲存的心律失常事件資訊,也有利於判斷ICD治療是否恰當及其有效性等。X線影像學檢查可發現導線脫位、導線磨損、導線與脈衝發生器連線不當等問題,這些問題均可導致ICD系統故障。實時的心電圖檢查或動態心電圖是判斷患者快速心律失常性質的"金標準",尤其是針對發作頻繁者,可與程控報告相互印證,並協助最終確診個別患者的電擊幻覺。ICD系統常見故障及處理原則簡述如下[77,87]。
1.頻繁電擊的原因及處理:
主要包括兩種情況。①電擊不能終止室速/室顫;②電擊有效,但室速/室顫事件頻繁發生。情況①即為高DFT,雖較少見,但後果非常嚴重。應採取的措施包括增加ICD放電能量、改變除顫方向、改變雙向除顫波的脈寬和斜率等。如上述措施不能解決,則必須透過更換脈衝發生器、更改除顫電極位置或更換、新增新的除顫電極導線等手術方法解決,術中必須進行DFT測試以確保安全。對於情況②,首先應尋找室速/室顫反覆發生的原因,如心衰加重、心肌缺血、電解質紊亂、突然停用抗心律失常藥物等,加強相應的藥物和非藥物治療措施。對於無明確器質性疾病,能耐受一定頻率的室速患者,應調整治療引數,放寬識別和干預標準,並開啟無痛治療措施,包括充電時再確認、ATP策略最佳化等。
目前將24 h內發生≥3次互不相連的ICD治療事件定義為ICD電風暴,治療事件包括ATP或電擊成功的事件,臨床並非少見。ICD電風暴是心臟危急症,應儘快對因治療,同時給予鎮靜、抗焦慮、抗心律失常藥物治療。對於藥物難以控制者,在有經驗的醫療中心可考慮行急診導管消融術[90]。
對於診斷、電擊治療均正確但患者無明顯不適症狀的不必要電擊(雖然並非ICD系統故障)亦要努力避免,因為不論正確還是非正確電擊治療都會惡化患者的預後。預防措施包括個體化提高識別和治療頻率以及採取藥物或非藥物措施預防室速的發生。
2.不適當治療的原因及處理:
引起不適當治療的常見原因為過感知,包括過感知自身的心電訊號(室上性激動下傳的QRS波及T波)及心外噪音(非心電訊號)。①室上性快速心律失常:包括室上性心動過速(室上速)、房性心動過速、心房顫動、心房撲動等,是導致不適當頻繁電擊的最常見原因。主要處理措施:開啟鑑別室上速的程式,包括穩定性、突發性、形態學、房室頻率標準等,同時可針對室上速給予積極的治療,包括藥物和消融手術。②過感知T波和遠場心房感知:相對①少見。過感知T波往往是由於除顫電極周圍心肌自身R波太低所致。需調整自動感知靈敏度的設定,包括程控感知衰減引數、程控感知環路等,如不能奏效,應及時更換感知電極導線的位置或不同品牌功能的脈衝發生器。③過感知心外噪音:包括肌電干擾、導線或絕緣層磨損、與共存的心血管植入型電子器械繫統相互干擾、體外電磁干擾等。針對不同的原因可採取更換導線、拔除廢棄的ICD導線、遠離電磁干擾源等措施。
3.ICD不治療的原因及處理:
ICD不治療可能源於ICD對室速/室顫的感知、識別障礙,也可能發生在治療程式中。①心室感知不足:如系R波感知問題,需重置電極導線位置或另外單獨放置一根起搏感知導線;若導線或脈衝發生器故障時,多需更換新的電極導線或脈衝發生器。②程控設定引數不當:包括設定的室速診斷標準高於患者實際發生室速的頻率、ICD設定的鑑別程式未能正確判斷室速等。此時需重新調整ICD引數,包括開啟形態學鑑別標準或房室鑑別標準等。③ICD脈衝發生器或除顫電極導線故障:如電池耗竭或導線斷裂,通常需要重新手術更換脈衝發生器或除顫電極導線。
九、結語
本共識是在2014年《植入型心律轉復除顫器治療的中國專家共識》基礎上,結合新近的臨床研究及國際上新制定的ICD指南,由中華醫學會心電生理和起搏分會、中國醫師協會心律學專業委員會牽頭,共同組織相關領域專家修訂完成。該共識從SCD的流行病學、ICD發展歷程和臨床試驗、ICD適應證(以疾病型別為基礎)、ICD型別的選擇、隨訪和程控以及常見故障處理等都進行了全面而簡明扼要的闡述。希望透過本共識的出臺,能有效提高對SCD及ICD預防SCD的認識,推動ICD作為預防SCD這一重要手段在國內的進一步合理、合規的推廣使用,真正降低我國SCD的發生率,使SCD高危患者獲益。
執筆人(按姓氏漢語拼音排序)
陳樣新,範潔,華偉,劉兵,宿燕崗,徐偉,許靜,薛小臨,鄭良榮
專家工作委員會(按姓氏漢語拼音排序)
陳柯萍(中國醫學科學院阜外醫院心律失常中心),陳樣新(中山大學孫逸仙紀念醫院心血管內科),範潔(雲南省第一人民醫院心內科),華偉(中國醫學科學院阜外醫院心律失常中心),黃德嘉(四川大學華西醫院心內科),劉兵(空軍軍醫大學西京醫院心血管內科),劉興斌(四川大學華西醫院心內科),蘇晞(武漢亞洲心臟病醫院心內科),宿燕崗(復旦大學附屬中山醫院心內科),王景峰(中山大學孫逸仙紀念醫院心血管內科),徐偉(南京大學醫學院附屬鼓樓醫院心臟科),許靜(天津市胸科醫院心內科),薛小臨(西安交通大學第一附屬醫院心血管內科),張澍(中國醫學科學院阜外醫院心律失常中心),鄭良榮(浙江大學醫學院附屬第一醫院心血管內科),周勝華(中南大學湘雅二醫院心血管內科)
專家工作委員會秘書
汪菁峰(復旦大學附屬中山醫院心內科)