責編|酶美
隨著我國人民群眾飲食習慣和生活方式的現代化,炎症性腸病 (Inflammatory bowel disease, IBD) 發病率呈持續快速增長的趨勢。IBD的發病機制複雜,臨床治療常以水楊酸類藥物、糖皮質激素類藥物和免疫抑制劑等抗炎藥物治療為主,作用單一,效果不佳,容易復發,而長期的藥物治療成本高、副作用大,給患者和社會造成巨大的負擔。
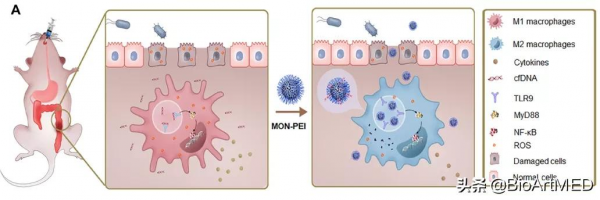
近日,西安交通大學第一附屬醫院佘軍軍教授、華南理工大學邵丹研究員和美國哥倫比亞大學梁錦榮教授團隊合作在Science Advances上發表論文:A nanoparticulate dual scavenger for targeted therapy of inflammatory bowel disease,報道了一種兼具遊離DNA(cfDNA)捕獲和活性氧簇(ROS)清除特性的生物活性奈米材料,這種無藥物負載的奈米清除劑可顯著降低腸組織和腹腔液中cfDNA和ROS水平,透過綜合調控炎症反應和氧化應激,在多種炎症性腸病模型小鼠中均取得了較好的療效和安全性。
基於該材料的炎症組織靶向和滯留特性,可透過延長口服給藥頻率,取得優於臨床一線藥物美沙拉嗪的治療效果,具有一定的轉化潛力;本研究為炎症性腸病的干預提供了新策略,亦為高效安全的炎症性腸病的治療提供了新材料和新藥物。
作者發現cfDNA在IBD患者血清中呈高表達,且與疾病的嚴重程度和預後呈正相關。細胞和動物實驗證實cfDNA可能透過啟用TLR9-MyD88-NF-κB作用於巨噬細胞,逆轉巨噬細胞由M2向M1極化,在IBD發生發展中扮演重要作用,為IBD的治療提供了新靶點。
為進一步提高IBD治療效果,作者提出同時清除cfDNA和ROS的綜合治療策略,並構築出包含結合cfDNA的PEI外殼和清除ROS的二硒鍵橋聯奈米核心的生物材料。該生物活性奈米粒可在體內外水平高效清除cfDNA和ROS,並抑制炎症反應的發生和發展,且效果優於具有單一清除功能的奈米粒子。
生物活性奈米粒子在急性和慢性IBD模型小鼠中均取得了較好的治療效果,透過最佳化給藥方式、劑量和頻率,篩選出適配於口服給藥的最優體系。系統地研究了MON-PEI的給藥方式對治療效果的影響,篩選最佳的給藥劑量及頻率,並證實其透過降低腸組織和腹腔液中cfDNA和ROS水平,綜合調控炎症反應和氧化應激的作用機理。
口服生物活性奈米粒子在炎症腸組織具有更高的聚集和滯留能力,可透過延長給藥頻率,展示出優於臨床一線藥物美沙拉嗪的治療效果,且具備了較好的生物安全性。該生物活性奈米粒子製備簡單,應用方便,且不含任何藥物分子,具有較好的臨床轉化前景,可進一步作為載體擔載相關藥物實現IBD的高效綜合治療。
原文連結:
https://www.science.org/doi/full/10.1126/sciadv.abj2372.
製版人:十一
轉載須知
【非原創文章】本文著作權歸文章作者所有,歡迎個人轉發分享,未經允許禁止轉載,作者擁有所有法定權利,違者必究。