冠狀動脈疾病發病率近年來一直呈上升態勢,如今已經成為人類健康的頭號殺手。冠狀動脈疾病患者大多數喪失勞動力,其中心肌梗死的致殘率達到50%,嚴重危害人民的生命和健康。冠狀動脈可以向心髒供給氧氣和營養物質,從而維持心臟正常的生理功能。然而,當冠狀動脈發生病變,如血管壁發生動脈粥樣硬化,管腔迅速發生持久而完全的閉塞,導致冠狀動脈供血急劇減少或者中斷,使相應的心肌持久而嚴重地急性缺血,從而引發心肌梗死。關於冠狀動脈疾病引起心肌梗死和心衰的研究很多,如何提高損傷心臟的供血機能已是該領域的研究熱點。因此,揭示冠狀動脈的生成方式,闡明冠狀動脈形成的分子機制,將有助於人們進一步瞭解冠狀動脈疾病,併為心臟損傷後血管新生治療提供新的策略或方法。
目前認為,發育過程中心臟的冠狀動脈內皮細胞主要來源於靜脈竇和心內膜。由靜脈竇來源的冠狀血管,定義為第一群冠狀血管群(1st CVP),主要分佈在心臟的外側心肌壁。而心內膜來源的血管(2nd CVP)主要分佈在心臟的內側心肌壁以及室間隔。這些不同來源的血管內皮細胞經過增殖、分化及重塑等過程形成冠狀血管叢。目前觀點認為,冠狀動脈主要由第一群冠狀血管內皮遷移、聚集、合併及動脈化形成,新生期心臟的冠狀動脈形成是否有其他新的生成方式仍需進一步研究。
2022年2月4日,國際學術期刊Circulation Research 以封面文章發表了中國科學院分子細胞科學卓越創新中心周斌研究組和海南大學駱清銘研究組題為 Extension of Endocardium-derived Vessels Generate Coronary Arteries in Neonates 的最新研究成果。在該研究中,他們發現了新生期小鼠冠狀動脈生成的新方式,心內膜來源的管狀結構透過向外擴張、動脈化等一系列過程生成橫跨心臟內外側壁的心肌層冠狀動脈,而這一過程受到Mettl3和Notch訊號通路的調控。進一步研究發現生成的冠狀動脈可以持續到成年,在心臟損傷如心肌梗死中發揮重要的保護作用。該研究利用多種單/雙同源重組酶介導的譜系示蹤技術,並結合熒光顯微光學切片斷層成像fMOST技術,清晰地展示了新生期小鼠心臟中冠狀動脈生成新方式,為損傷心臟的血管修復和治療提供新的研究方向,也為心血管再生醫學提供了新思路。
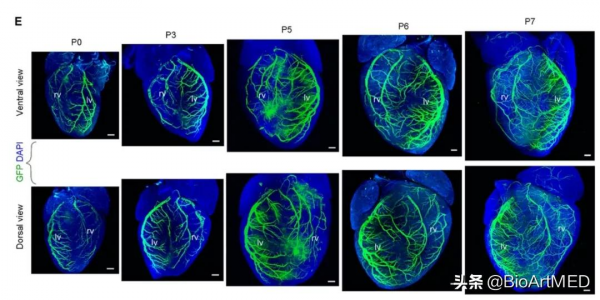
為了系統地研究新生期心臟中冠狀動脈血管發育過程和生成方式,研究者首先利用Tie2 Cre;CX40-LSL-GFP雙譜系示蹤系統,結合組織透明化及光片熒光顯微成像處理,清晰地解析了冠狀動脈在新生期小鼠心臟中的發育過程。研究者發現,新生小鼠心臟中的心肌層中的冠狀動脈數量會隨著心臟的發育而增多,隨著時間的推移,比較出生後3天和出生後7天的小鼠心臟,會發現這一過程中心臟內側壁的冠狀動脈明顯增多(如下圖),那這些冠狀動脈來源於哪裡呢?這為研究者進一步的研究提供了方向。
前期相關研究認為,冠狀動脈主要由分散的內皮細胞透過血管新生、遷移、聚集、重塑形成。在胚胎期,1st CVP的內皮細胞可以透過遷移、融合、分化為冠狀動脈。為了標記這一群來源的冠狀血管,研究者構建了Apln-CreER小鼠,透過譜系示蹤發現1st CVP冠狀動脈主要分佈在心臟外側壁心肌層中,並在出生後一週隨著心臟發育進一步擴張。透過免疫熒光染色發現,在出生後7天的心臟中,1st CVP和2nd CVP的血管內皮細胞分別位於心臟心室壁外側和內側。但發現在1st CVP區域出現了一些未被Apln標記的冠狀動脈,而這些未被Apln標記的冠狀動脈持續到成體小鼠心臟。利用Apj CreER譜系示蹤小鼠,我們發現了同樣的情況。這群存在於心臟1st CVP區域內但未被Apln/Apj-Cre標記的冠狀動脈來源於哪裡呢?為了研究這一群冠狀動脈來源,研究者利用心內膜特異性的Npr3-CreER小鼠進行譜系示蹤,檢測心內膜是否貢獻到這一群特殊的冠狀動脈內皮細胞。他莫昔芬誘導處理懷孕13.5天的小鼠,收集出生後0天到28天的小鼠心臟樣本,對出生後3天和 5天的樣本進行檢測,發現在心臟1st CVP 區域存在心內膜來源的管道或索道狀結構,經過染色發現,這一群細胞既不表達成熟血管標記FABP4和Pdgfb,也沒有招募血管平滑肌細胞,因此並不是冠狀動脈。而檢測出生後7天,14天,28天以及成體小鼠心臟樣本,可以發現在1st CVP 區域存在心內膜來源的冠狀動脈。研究者將出現在出生後3天和5天的這一特殊結構稱為“前體冠狀動脈索道”。研究者進一步發現,前體冠狀動脈索道相較於周邊的血管內皮,具有更高的細胞外基質基因和動脈形態發生的相關基因的表達,而且出生後5天以後才能夠具有成熟的血管功能,能夠完全連線到迴圈系統。綜上,研究者確定了1st CVP 區域存在心內膜來源的冠狀動脈,而這一動脈是由心內膜來源的前體冠狀動脈索道向外延伸生成的。為了進一步證明這一結論,研究者將譜系示蹤技術和透明化技術相結合,收集他莫昔芬誘導處理的Npr3-CreER小鼠心臟,在整體心臟中清晰地觀察到前體冠狀動脈索道在出生後五天的小鼠心臟外側肌肉層出現,更多的被標記的冠狀動脈出現在出生後7天以及28天。綜上,心內膜形成了1st CVP 區域早期的前體冠狀動脈索道,隨著心臟的發育過程,前體冠狀動脈索道透過隨後的動脈化形成成熟的冠狀動脈,將1st CVP和2nd CVP兩個不同起源的冠狀血管群有效連線在一起。
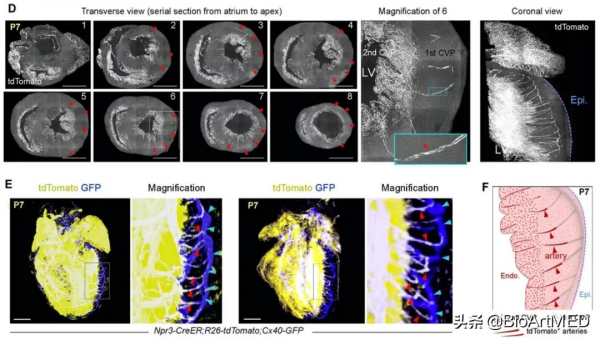
為了進一步闡明這種由心內膜來源內皮細胞向外側心肌層遷移並形成的冠狀動脈過程,研究者採用了熒光顯微光學切片斷層成像(fMOST)方法,對動脈形成過程進行了更為精細的完整心臟單細胞水平的成像。研究者將樣本處理成1.0 µm厚度,然後用水鏡進行成像。依據不同心臟大小,整個資料持續21-74小時,覆蓋整個心臟的1700-5500張冠狀面。資料經過一系列的處理重建,發現出生後5天的小鼠心臟心室壁外側中出現前體冠狀動脈索道,而出生7天后的心臟心室壁外側中出現成熟的冠狀動脈血管。研究者利用亞微米解析度(0.320.321µm3)進行三維重建心臟的橫向檢視,可以清晰地看到形成冠狀動脈的前體冠狀動脈索道。為了進一步確認生成的是一群具有功能的成熟冠狀動脈,研究者收集Npr3-CreER;R26-tdTomato;Cx40-GFP 心臟,透過fMOST成像可以清晰地看到前體冠狀動脈索道生成的冠狀動脈能連線1st 和 2nd CVPs,共同形成心臟的迴圈系統(如下圖)。
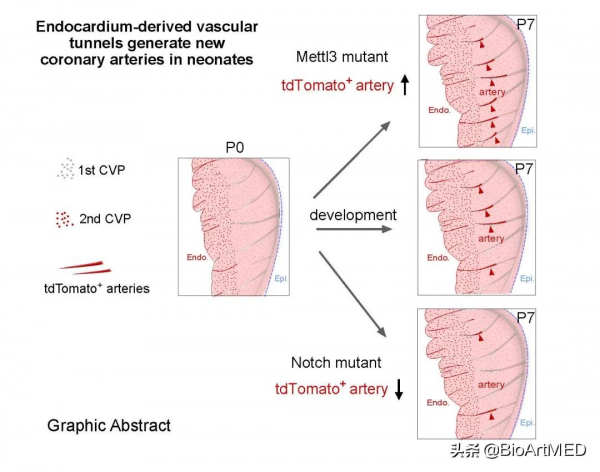
在分子機制方面,研究者透過一系列組織特異性基因敲除的遺傳學方法,闡明瞭Mettl3和Notch訊號通路可以調節前體冠狀動脈索道的形成,從而調控著發育心臟中這一群特殊的冠狀動脈數量。心內膜特異性Mettl3敲除後,心臟出現了更多的冠狀動脈;而在Mettl3敲除基礎上再敲除Notch訊號通路Dll4或者Rbpj基因,心臟的冠狀動脈形成明顯減少,提示Mettl3-Notch訊號通路調控心內膜來源的冠狀動脈生產。進一步功能研究,研究者檢測了這一群冠狀動脈的心臟損傷修復中是否有作用,利用結紮冠狀動脈左前降支構建了心肌梗死模型,發現心內膜來源的前體冠狀索道生成的冠狀動脈數量的增加和減少都會影響著心肌梗死後心臟功能的改變。
綜上,研究者發現心內膜來源的前體冠狀索道結構,可以經過動脈化後形成具有功能的冠狀動脈,這一群冠狀動脈連接出生後心髒的兩個冠狀血管群,而這一過程收到Mettl3和Nocth 訊號通路的精細調控,同時這一群冠狀動脈對成體心臟損傷後心髒功能的維持起著重要作用。
中國科學院分子細胞科學卓越創新中心唐娟博士(現同濟大學研究員)、博士生朱歡以及田雪瑩博士(現暨南大學研究員)為該論文共同第一作者。中國科學院分子細胞科學卓越創新中心周斌研究員和海南大學駱清銘教授為該論文共同通訊作者。華中科技大學龔輝教授、牛津大學Nicola Smart教授、復旦大學附屬中山醫院顏彥教授、中國科學院分子細胞科學卓越創新中心童明漢研究員、西湖大學何靈娟研究員等也為該項研究提供了支援和幫助。
原文連結:
https://www.ahajournals.org/doi/10.1161/CIRCRESAHA.121.320335
製版人:十一
轉載須知
【非原創文章】本文著作權歸文章作者所有,歡迎個人轉發分享,未經允許禁止轉載,作者擁有所有法定權利,違者必究。