PARP抑制劑作為新興靶向藥物,從2017年獲得美國FDA批准用於卵巢癌復發患者開始,在卵巢癌治療的道路上“一路高歌”。PARP抑制劑在卵巢癌維持治療中的多項研究結果充分顯示了其可鞏固初始治療療效、推遲復發、改善患者的生存和預後的應用價值。尼拉帕利等PARP抑制劑已成為卵巢癌一線維持治療的最佳選擇之一。那麼,對於高復發風險、BRCA野生型卵巢癌患者,尼拉帕利維持治療是否可預防或推遲腫瘤的復發和轉移?尼拉帕利的起始劑量該如何選擇?尼拉帕利維持治療期間如何監測患者的狀況?本次病例將分享尼拉帕利一線維持治療在初始減瘤僅達R1、高復發風險的晚期卵巢癌患者中的規範化治療經驗。
福建省腫瘤醫院
福建省醫學會婦科腫瘤專業委員會委員兼秘書
中國醫促會婦科腫瘤學組委員
第一屆全國衛生產業企業管理協會試驗醫學專家委員會委員
福建省海峽腫瘤防治科技交流協會婦科與乳腺腫瘤防治專委會委員
福建省中西醫結合學會婦產科分會第六屆委員會委員
從事婦科腫瘤工作20餘年,熟練掌握卵巢癌、宮頸癌、子宮內膜癌、子宮肌瘤等婦科良惡性腫瘤的診治,參與編譯《女性生殖道病理學》等譯著及多項婦科腫瘤相關的省市級科研專案和臨床試驗,發表多篇婦科腫瘤相關文章。
01 病例回顧
基本資料
患者女性,50歲,平素身體健康狀況良好,無慢性病史,無家族史。
治療經過
第一階段:初始腫瘤細胞減滅術(PDS)+術後化療
患者於2018年11月8日因“腹痛、陰道分泌物增多2月餘,發現盆腔腫物9天”就診外院,初診血CA125 548 U/ml,HE4 101 pmol/L,盆腔MRI示盆腔兩側混雜佔位性病變,伴子宮直腸陷凹種植轉移及盆腔積液。
初步診斷:雙側卵巢癌,轉移瘤不完全排除。
2018年11月19日在外院行卵巢癌PDS,達到R1切除。術後病理:雙卵巢子宮內膜樣腺癌(Ⅲ級),侵及右輸卵管粘膜、肌層及漿膜層。子宮漿膜面見腫瘤侵犯,大網膜、闌尾漿膜面及肌層、腸管表面、陰道後壁、直腸表面見腺癌轉移。
術後診斷:雙卵巢子宮內膜樣腺癌G3Ⅲb期。
術後按TC 3周方案(紫杉醇240 mg+卡鉑600 mg 3周方案)化療7個週期。末次化療時間為2019年4月11日。末次化療後血CA125 15.2 U/ml。化療期間患者一般情況好,無明顯噁心、嘔吐等不適,血常規無異常。
第二階段:PARP抑制劑一線維持治療
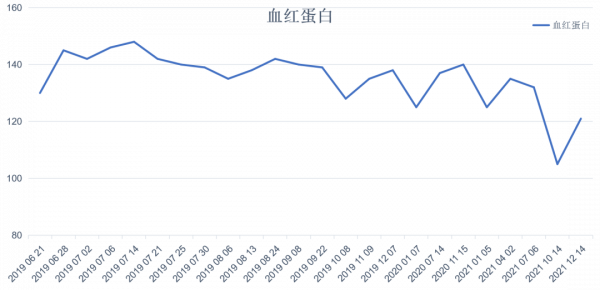
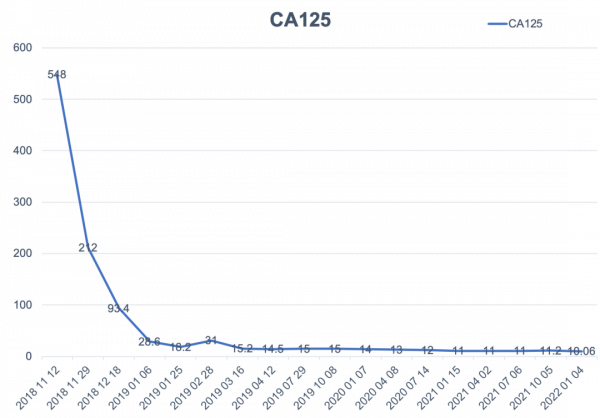
患者在第4次化療期間,行BRCA基因檢測,結果為野生型,未查HRD。為預防或推遲復發及轉移,患者於門診諮詢後,自2019年6月25日起口服尼拉帕利200 mg QD維持治療(初始體重55 kg,血小板計數146×109/L)。服用尼拉帕利期間無明顯胃腸道不良反應,血液學指標平穩,血小板計數未低於100×109 /L(圖1),血紅蛋白維持在正常水平(圖2),血CA125水平在正常範圍內波動(圖3)。患者分別於2019年7月30日、2020年4月28日、2020年7月14日、2021年1月5日、2021年7月6日、2021年10月5日、2022年1月4日(即服藥1、10、13、19、24、28、31個月後)複查7次盆腹腔彩超均未見明顯異常。
病例總結
患者因“腹痛、陰道分泌物增多2月餘,發現盆腔腫物9天”於2018年11月8日初診外院。盆腔MRI提示雙側卵巢癌;血CA125 548 U/ml。於外院行PDS,術中發現盆腔轉移,達R1切除,根據病理結果術後診斷為“雙卵巢子宮內膜樣腺癌G3Ⅲb期”。行TC 3周方案化療7個週期,血CA125水平降至正常。基因結果提示BRCA野生型,未行HRD狀態檢測。2019年6月25日起口服尼拉帕利200 mg QD一線維持治療。至2022年1月維持治療31個月期間,血CA125水平在正常範圍內波動,血液學指標(白細胞、血小板、血紅蛋白)平穩,無明顯胃腸道不良反應。多次複查盆腹腔彩超均未見明顯異常。
03 專家點評
福建省腫瘤醫院
福建省腫瘤醫院婦瘤科九區行政主任,主任醫師
福建省醫學會婦科腫瘤專業委員會主任委員
國家癌症中心國家腫瘤質控中心卵巢癌質控專家委員會委員
中華醫學會婦科腫瘤專業委員會委員
中國抗癌協會婦科腫瘤專業委員會委員
中華醫學會腫瘤分會婦科腫瘤專業委員會委員
中國臨床腫瘤學會(CSCO)婦科腫瘤專委會常委
中國醫促會婦產科專業委員會常委
中國研究型醫院婦科腫瘤專業委員會委員
南方腫瘤臨床研究協會婦科腫瘤分子診療專業委員會第一屆委員會常委
福建省海峽腫瘤防治科技交流協會婦科與乳腺腫瘤防治專委會副主任委員
福建省抗癌協會婦科腫瘤專業委員會副主任委員
福建省中西醫結合婦產科委員會副主任委員
長期從事婦科腫瘤綜合治療,外科治療,擅長宮頸癌、卵巢腫瘤、子宮內膜癌、外陰癌等婦科腫瘤的外科手術及綜合治療。
對於卵巢癌患者而言,大多數患者在發現卵巢癌時已處於晚期,即使完成腫瘤細胞減滅術和化療,臨床複發率依然很高。因此提高其生存率是治療的重要目標,手術、化療和維持治療是實現該目標的三種手段。因此,對於卵巢癌的規範化治療,是在滿意的腫瘤細胞減滅術後給予以鉑為主、標準、足量的化療後,再應用合理的維持治療以延長無進展生存期(PFS)和無鉑間期,從而提高患者生活質量、延長生存時間。隨著PARP抑制劑的問世,其逐漸成為維持治療的推薦藥物之一。多項研究顯示,PARP抑制劑維持治療可延長PFS和總生存期(OS),推遲患者復發及再復發時間,改善生存質量和預後[1]。PARP抑制劑早期臨床研究多圍繞BRCA突變的卵巢癌患者開展。而在真實世界裡,更多的患者沒有BRCA突變。那麼,BRCA野生型的患者使用尼拉帕利一線維持治療效果如何呢?PRIMA研究[2]給出了答案。PRIMA研究是一項應用尼拉帕利單藥作為卵巢癌一線維持治療的Ⅲ期臨床研究,入組患者不計BRCA是否突變和HRD狀態,且僅有0.4%的患者實現了手術R0切除,大多數患者屬於高復發風險人群。研究發現尼拉帕利延長了整體卵巢癌患者人群PFS,相較於安慰劑,尼拉帕利可降低38%的復發或死亡風險(中位PFS分別為13.8個月和8.2個月,HR 0.62,95%CI 0.50~0.75,P<0.001),1年無進展生存率分別為53%和35%;亞組分析顯示,無論BRCA是否突變、HRD狀態如何,尼拉帕利一線維持治療均可實現PFS獲益。該研究同時證實了尼拉帕利長期應用的安全性。正是基於PRIMA的優秀研究結果,美國國立綜合癌症網路(NCCN)指南推薦尼拉帕利單藥用於初始化療未用過貝伐珠單抗的卵巢癌全人群的一線維持治療[3]。所以,對於高復發風險的晚期卵巢癌患者,可選擇尼拉帕利作為一線維持治療藥物。那麼,尼拉帕利的起始劑量又該如何選擇?早期NOVA研究的回顧性RADAR分析顯示,若患者基線體重<77 kg或者血小板計數小於15×109/L,以尼拉帕利200 mg QD作為起始劑量,可在確保療效的同時緩解血液學毒副反應[4]。PRIMA研究也顯示,基於體重和血小板計數的個體化給藥方案,可降低血液學不良事件的發生率[2]。
該患者系BRCA野生型,初始治療中未使用貝伐珠單抗,可選擇尼拉帕利一線維持治療。根據RADAR分析,患者初始體重55 kg,血小板計數146×109/L,故選擇200 mg QD作為起始劑量。該患者服藥期間血小板和血紅蛋白水平平穩,耐受性良好,未觀察到其他非血液學不良反應。該患者初始減瘤僅達R1,系高危復發患者,服用尼拉帕利維持治療期間密切隨訪血CA125水平及影像學檢查,至今無進展生存期已達31個月,獲益時間長於PRIMA研究報道的平均水平。
遵循循證醫學證據的尼拉帕利一線維持治療、嚴密的影像學檢查及腫瘤標誌物等血液指標隨訪檢測為這例高復發風險的晚期卵巢癌患者提供了規範化、常態化的治療策略,成功延緩了腫瘤復發,成為高復發風險的卵巢癌患者的有效管理模式。希望透過本例高復發風險的晚期卵巢癌患者的維持治療藥物合理化選擇經驗分享,能為卵巢癌的規範化、常態化全程管理模式制定帶來啟發,為更廣泛卵巢癌人群帶來最優生存獲益。
參考文獻
[1]Liu MC, et al. Expert Rev Anticancer Ther. 2021. PMID: 33691564.
[2]Gonzalez-Martin A, et al. N Engl J Med. 2019; 381(25): 2391–2402.
[3]NCCN Guidelines. Ovarian Cancer Including Fallopian Tube Cancer and Primary Peritoneal Cancer. Version 1. 2021. available at www. nccn. org.
[4]Mirza MR, et al. N Engl J Med. 2016; 375(22): 2154-2164.