肥胖人口的快速增長已使其成為全球一個主要的健康問題,且肥胖患病率的急劇攀升對慢性腎臟病(CKD)的嚴重程度產生重大影響,尤其是在發展中國家。大量研究報告了肥胖與CKD之間的密切關係,並可作為腎病的獨立危險因素。肥胖所致腎損傷的腎臟組織學變化包括腎小球或腎小管肥大、局灶節段性腎小球硬化(FSGS)或球性硬化。此外,炎症、腎臟血流動力學變化、胰島素抵抗和脂質代謝紊亂均與肥胖相關性腎病的發生和發展相關。但目前尚無針對肥胖相關性腎病的靶向治療。
近日,Int J Mol Sci發表了一篇綜述,介紹了採用腎素-血管緊張素系統(RAS)抑制劑、鈉-葡萄糖協同轉運蛋白2(SGLT2)抑制劑和褪黑素來治療肥胖所致腎損傷。結論顯示,褪黑素可透過抑制炎症和氧化應激來保護由肥胖引起的腎損傷,從而揭示其治療潛力。
肥胖所致的腎病
1 腎小球損傷
肥胖相關性腎小球病(ORG)是肥胖患者最常見的CKD併發症,其發病率從1986年到2015年增加了10倍以上,且ORG 患者的平均身體質量指數(BMI)高於正常人。因此,肥胖患者在早期表現出典型ORG的臨床和組織病理學特徵需更加值得注意。研究發現,ORG患者的特徵性組織學改變之一可能是與腎小球肥大相關的低腎小球密度。換言之,ORG患者腎單位總數的減少可能導致腎小球肥大。最近的一項研究表明,在總的腎單位相似的情況下,與非肥胖或肥胖對照組相比,ORG患者的腎小球體積更大,密度更低,硬化更多。
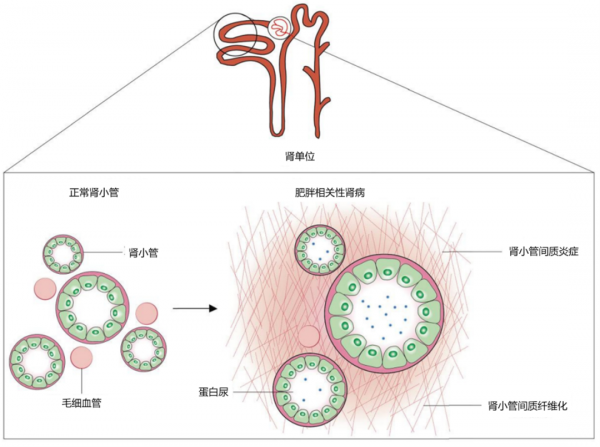
另外,在ORG早期,肥胖導致腎小球肥大,這可能引起腎小球足細胞增大。由於腎小球足細胞不能分裂和去分化,致使足突消失,足細胞脫落,腎小球通透性增強。大量足細胞脫落後,FSGS損傷可能會隨之而來,晚期則發展為腎小球結構和功能喪失(圖1)。
2 腎小管損傷
與ORG相比,肥胖相關性腎小管結構和功能損害的研究很少。在大量動物實驗中,肥胖可引起腎小管損傷,包括腎小管肥大、出現脂質細胞質包涵體、腎小管間質炎症和纖維化(圖2)。
此外,在糖尿病腎病中,腎小管損傷的原因可能與肥胖相關的高濾過性密切相關。腎臟對葡萄糖重吸收的主要部位是近端小管(PT),PT透過SGLT1和SGLT2增加葡萄糖和鈉的重吸收,導致遠端小管鈉負荷減少,進而啟用腎小管-腎小球反饋,導致腎小球血管擴張。
肥胖所致腎病的發病機制
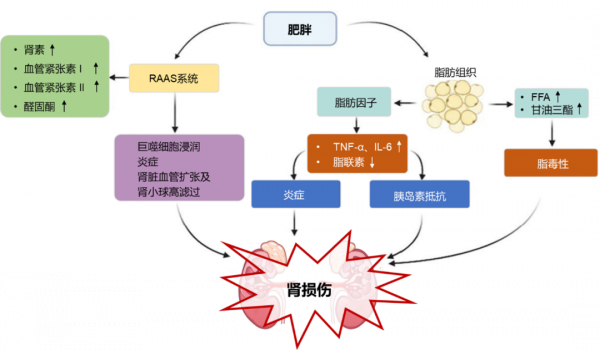
研究顯示,高水平腫瘤壞死因子-a(TNF-a)、白細胞介素-6(IL-6)、脂聯素和血管緊張素II以及代謝紊亂均與肥胖所致腎損傷相關。這些因素增加了腎臟炎症、胰島素抵抗和腎素-血管緊張素-醛固酮系統(RAAS)系統啟用的變化,最終導致腎損傷(圖3)。
1 炎症反應與胰島素抵抗
在肥胖狀態下,聚集在腎臟周圍的脂肪組織可能會釋放過量的促炎脂肪因子(如TNF-α和IL-6),減少有益的脂肪因子(如瘦素和脂聯素)。促炎細胞因子參與細胞肥大、細胞外基質堆積和腎臟纖維化過程,並與尿白蛋白/肌酐比值呈正相關。與TNF-α和IL-6不同,脂聯素與抗炎、抗動脈粥樣硬化和胰島素增敏作用有關,其血清濃度隨著肥胖而降低。
另有研究發現,伴有胰島素抵抗的肥胖患者血液中一些炎症生物標誌物升高,如C反應蛋白、TNF-α和IL-6。而脂肪組織中的脂質代謝功能失調會導致迴圈中的遊離脂肪酸堆積,從而引發炎症訊號級聯反應。促炎細胞因子的反饋作用加劇了這種病理狀態,促進細胞因子的進一步分泌,並以同樣的方式破壞胰島素抵抗。
2 RAAS啟用
越來越多的證據表明,RAAS啟用在肥胖相關腎病的進展中起著關鍵作用。腎素是腎素-血管緊張素系統(RAS)的限速酶,其水平可以調節RAAS活性。腎素釋放蛋白水解酶並刺激血管緊張素I,使其進一步水解成活性血管緊張素II,後者透過啟用其受體在腎臟中發揮作用,同時促進醛固酮的分泌。醛固酮反過來又增強血管緊張素II的作用,誘導血管炎症及重構,並刺激腎臟中的鹽皮質激素受體(MR)。MR啟用促進腎臟血管擴張,進而損害肥胖患者的腎臟排洩功能。
3 脂毒性
由於脂質代謝紊亂,脂肪量超過正常範圍,沉積在不該沉積的器官上,對器官造成毒性和損傷,這種現象稱為脂毒性。腎臟脂毒性導致慢性腎損傷的過程包括細胞內FFA、甘油三酯和毒性代謝物(如腎小球和腎小管間質細胞中的神經醯胺)的堆積。研究表明,脂毒性的所有細胞損傷機制均可引起腎臟損傷,包括炎症、氧化應激、纖維化、細胞內訊號通路改變和脂質誘導的細胞凋亡。
治療肥胖所致腎病的藥物
由於肥胖發病機制的特殊性和複雜性,其他腎臟疾病的治療藥物或方法可能不適用於肥胖相關性腎臟疾病。因此,需制定專門治療肥胖患者腎臟疾病的干預措施。
1 RAS抑制劑
一般來說,RAS抑制劑通常用於治療蛋白尿和糖尿病腎病患者,代表藥物有血管緊張素轉換酶抑制劑(ACEI)和血管緊張素受體拮抗劑(ARB),可有效控制高血壓、糾正腎臟區域性血流動力學異常、減少蛋白尿、減輕炎症以及保護腎功能(圖4)。
圖4 RAAS和RAAS抑制劑在肥胖相關腎損傷中的作用
有研究顯示,與BMI正常的患者相比,肥胖患者可能對RAS抑制劑帶來的腎臟保護更為敏感。服用雷米普利(一種強效ACEI)的肥胖患者腎病進展風險顯著低於非肥胖患者。替米沙坦(一種ARB)透過減少脂肪量、促進脂肪生成消耗和降低瘦素水平來發揮腎臟保護作用。此外,還可透過在ACEI中新增螺內酯(一種MR拮抗劑)來降低肥胖患者的白蛋白尿和血壓。
2 SGLT2抑制劑
隨著對SGLT2抑制劑研究的不斷深入,發現其可有效阻斷腎臟對葡萄糖的重吸收,將尿液中多餘的葡萄糖排出體外,降低血糖,並對腎臟和心臟具有保護作用,還可透過降低脂肪和血壓來作用於腎臟,甚至降低高糖狀態下SGLT2的表達。大量人體和動物研究報道,SGLT2抑制劑有利於調節腎臟脂質代謝、改善炎症、預防腎病,具有促進體重減輕、尿鈉排洩和滲透性利尿的累積效應。此外,透過抑制SGLT2降低近端小管內葡萄糖和鈉的重吸收,可改善肥胖非糖尿病腎小球高濾過,延緩腎臟疾病進展(圖5)。
3 褪黑素
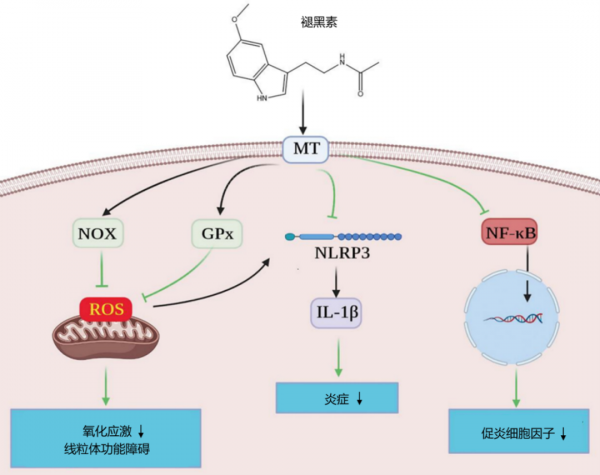
褪黑素具有調節生物鐘的功能,還具有許多機體反應的功能,如抗炎、抗氧化和抗凋亡反應,以及保護內皮細胞功能和抑制交感神經活動(圖6)。腎損傷大鼠模型試驗證實,外源性新增褪黑素可改善腎臟結構和功能。同樣,在肥胖動物模型中也獲得了類似效果,褪黑素減輕了腎損傷後的炎症反應,進而抑制氧化應激通路的後續啟用,其抗氧化作用機制包括增加谷胱甘肽過氧化物酶(GPx)活性、腎臟超氧化物歧化酶(SOD)水平和過氧化氫酶(CAT)活性。而GPx、SOD和CAT用於清除多餘的活性氧(ROS),ROS的產生和釋放會導致炎症、氧化應激、組織損傷和疾病進展。褪黑素還能透過抗氧化酶消除線粒體產生的過量自由基,緩解線粒體功能障礙。因此,維持穩定的抗氧化酶活性和發揮其自身的抗氧化作用是褪黑素作為肥胖相關腎病治療藥物的重要原因。
另外,褪黑素可透過抑制核轉錄因子-κB(NF-KB)減少促炎細胞因子等的轉錄,以及抑制炎症小體發揮抗炎作用。Nod樣受體家族含pyrin結構域蛋白3(NLRP3)炎症小體參與肥胖相關腎病的發生發展,可能是肥胖相關腎病的關鍵調節因子。NLRP3可促進IL-1和IL-18成熟,其中,IL-18可透過單核細胞和巨噬細胞促進TNF-α、IL-1和細胞間粘附分子的產生,從而對腎臟造成損害。因此,褪黑素抑制NLRP3炎症小體啟用,可有效減輕肥胖相關性腎病。
圖6 褪黑素對肥胖相關腎損傷的治療作用
總結
肥胖問題在全球範圍內日趨嚴重,其併發症也越來越受到重視,尤其是與肥胖相關的腎病。臨床上,ACEI和SGLT2抑制劑均可治療肥胖相關性腎病,還有大量資料表明,褪黑素對腎損傷具有潛在保護作用,其透過直接或間接機制在抗氧化應激和抑制腎細胞炎症中發揮有益作用。但仍需進一步深入研究。
參考文獻:
Wang M, Wang Z, Chen Y,et al. Kidney Damage Caused by Obesity and Its Feasible Treatment Drugs[J]. IntJ Mol Sci. 2022 Jan 11;23(2):747.