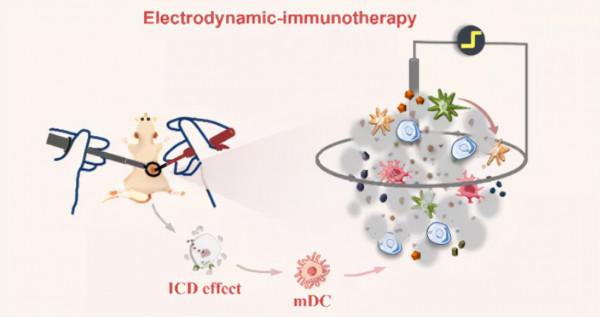
活性氧介導的動力學治療憑藉其免疫原性細胞死亡(ICD)效應,在腫瘤免疫聯合治療中扮演著重要的角色。南方醫科大學於夢、喻志強和國家奈米科學中心梁興傑等人利用這一活性氧策略設計了一種裝載谷氨醯胺拮抗劑DON的奈米載體,可將電動力學療法和免疫療法結合起來對抗腫瘤複合和轉移。相關工作以“Glutamine Antagonist Synergizes with Electrodynamic Therapy to Induce Tumor Regression and Systemic Antitumor Immunity”為題發表在ACS Nano。
電動力學療法(EDT)結合了納米技術和電流,是一種可實現高效癌症治療的手段。在這一療法中,一旦被外源電場觸發,具有巨大催化表面積的奈米材料(特定的金屬和複合金屬)會更傾向於產生高氧化的活性氧物質,而無需過氧化氫或者氧氣的幫助。不僅如此,電極刺激是一種類干預治療策略,可對深層腫瘤進行治療。然而,由於單一治療承擔著腫瘤復發的風險,EDT在長期腫瘤抑制中存在著巨大挑戰。
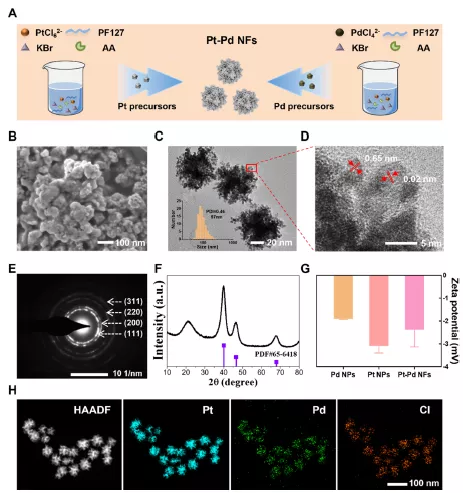
本研究合理設計了一種先進的治療平臺,將DON與多孔Pt−Pd奈米花整合形成奈米載體。其中,鉑和鈀透過一步化學反應合成前驅體,這兩種前驅體混合可得到Pt−Pd奈米花(圖1)。電學表徵顯示,與水基於氧化-還原反應被電催化形成氫離子和氫氧根離子不同,在電動力學治療中,由於溶液中氯離子的參與,電交換髮生在水分子和Pt−Pd奈米花之間而產生羥基自由基,因此不具備明顯的pH梯度。細胞實驗也表明,在方波電流的作用下,複合的Pt−Pd奈米花催化水分子產生的強毒性羥基自由基可高效殺傷腫瘤細胞。
在Pt−Pd奈米花發揮EDT作用的同時,DON則可以抑制谷胱甘肽的形成,並避免電場產生的活性氧被清除以削弱治療效果。基於內源的過氧化氫條件,Pt−Pd奈米花也可協助DON透過緩解乏氧強化樹突細胞的成熟和CD8+ T細胞的浸潤,從而可使EDT聯合谷氨醯胺代謝抑制行為發揮顯著的活體治療作用,透過保護性免疫有效抑制腫瘤的複合和轉移(圖2)。
於夢副教授與喻志強教授均任職於南方醫科大學藥學院。近年來,學院秉承“創新引領發展,特色成就卓越”的理念,整合資源,匯聚人才,形成了一支以中青年教師為主體的師資隊伍。具有博士學位教師佔專任教師總數90.2%,具有留學背景的教師佔比54.9%,更有若干國家級和省部級人才。
於夢,南方醫科大學藥學院副教授,碩士生導師。研究方向為內外源刺激響應型脂質體、高分子奈米載體研究;腫瘤光治療、超聲治療、免疫治療及其作用機制研究等。
喻志強,南方醫科大學藥學院教授,博士生導師。研究方向為新型靶向奈米遞藥系統;小分子前藥自組裝;癌症診療一體化;中藥納米制劑;美容活性多肽或中藥提取物護膚品研發等。
受益於人才建設,近五年來,藥學院先後承擔了國家科技重大專項、國家自然科學基金區域創新發展聯合基金重點支援專案、廣東省“新藥創制”科技重大專項、廣東省重點領域研發計劃等國家、省市級課題227項,研究經費1.68億元。在國際著名期刊上發表了SCI論文580餘篇,申請和獲得國家發明專利、國際PCT專利130餘項,其中授權76項,為學校高水平醫科大學建設做出了卓越貢獻。(資料截止至2021年10月)
關注"南方醫科大學招辦"頭條號,獲取關於南方醫科大學的最新精彩資訊!
部分素材來源:南方醫科大學官微,南方醫科大學藥學院,高分子科學前沿