*僅供醫學專業人士閱讀參考
2021年歐洲腫瘤內科學會(ESMO)大會於9月16日-21日在線上舉行。作為歐洲最負盛名和最具影響力的腫瘤學會議,ESMO已成為集臨床實踐、轉化研究及多學科交叉討論為一體的全球性學術交流平臺。今年受全球疫情影響,來自全球各地的腫瘤學專家學者雲端相聚,分享腫瘤治療領域的最新研究進展。
本次ESMO大會上,多項研究為中國的消化道腫瘤(胃癌、食管癌、膽管癌)帶來全新的治療選擇。其中包括兩項重要的大會口頭報告——信迪利單抗聯合化療一線治療晚期胃癌及食管鱗癌的III期臨床研究,以及一項pemigatinib治療中國晚期膽管癌II期研究的壁報展示。
ORIENT-16研究:信迪利單抗聯合化療顯著延長胃癌總體人群OS,帶來中國晚期胃癌一線治療新標準!
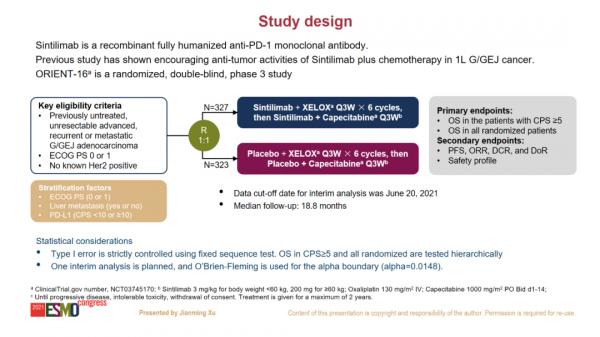
ORIENT-16是一項比較信迪利單抗注射液聯合化療(奧沙利鉑+卡培他濱)或安慰劑聯合化療(奧沙利鉑+卡培他濱),一線治療不可切除的區域性晚期、複發性或轉移性胃及胃食管交界處腺癌的有效性和安全性的隨機、雙盲、多中心、III期研究。由解放軍總醫院第五醫學中心徐建明教授代表中國研究團隊報告中期分析[1]結果:研究達到全部研究終點,顯著延長了總體人群的總生存期(OS)和PD-L1陽性人群的OS。
ORIENT-16研究成為中國首個證實PD-1抑制劑聯合化療一線治療晚期胃癌總體人群顯著延長生存的III期臨床研究。
ORIENT-16研究設計專為中國胃癌患者打造:
- 雙盲研究設計,非開放標籤,避免結果偏移;
- 6週期信迪利單抗或安慰劑聯合奧沙利鉑卡培他濱之後,使用信迪利單抗或安慰劑聯合卡培他濱進行維持,提升治療依從性,降低化療毒副反應;
- 主要研究終點為胃癌全人群OS及CPS≥5人群OS。
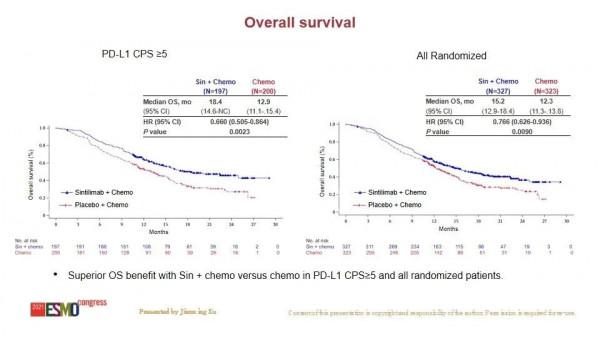
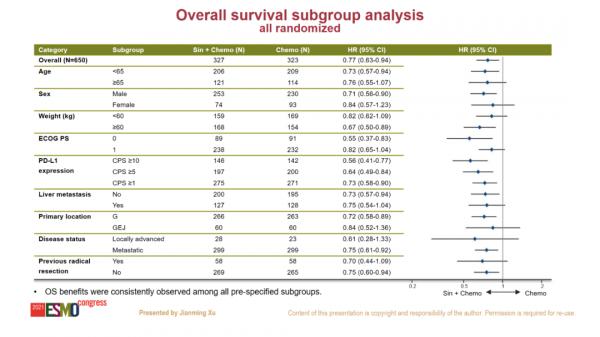
研究顯示,與化療相比,信迪利單抗聯合化療顯著降低總體人群的死亡風險(HR 0.766,95%CI:0.626-0.936,p=0.0090)和CPS≥5人群的死亡風險(HR 0.660,95%CI:0.505-0.864,p=0.0023),達到預設的雙重優效性標準;中位OS在總體人群延長2.9個月(中位OS 15.2月vs.12.3月),在CPS≥5人群延長5.5個月(中位OS 18.4月vs.12.9月)。而且,OS在預設的所有亞組分析中獲益趨勢一致。
同樣,與化療相比,信迪利單抗聯合化療顯著降低總體人群(HR 0.636,95%CI:0.525-0.771,p<0.0001)和CPS≥5人群(HR 0.628,95%CI:0.489-0.805,P=0.0002)的疾病進展風險;中位無進展生存期(PFS)在CPS≥5人群延長1.9個月(中位PFS 7.7月vs.5.8月),總體人群延長1.4個月(中位PFS 7.1月vs.5.7月)。
信迪利單抗聯合化療組相比化療組的客觀緩解率(ORR:58.2%vs.48.4%)更高,中位緩解持續時間(mDOR:9.8個月vs.7.0個月)更長。安全性特徵與既往報道的信迪利單抗相關臨床研究結果一致,無新的安全性訊號。
該研究結果表明,對於中國胃癌患者一線治療,無論PD-L1表達如何,信迪利單抗聯合化療相比單純化療都能顯著延長OS和PFS,為中國胃癌患者提供了一種新的標準一線治療方案。
ORIENT-15研究:再下一城!晚期食管鱗癌患者,信迪利單抗聯合化療顯著延長OS
ORIENT-15是一項比較信迪利單抗聯合化療(順鉑+紫杉醇/5-氟尿嘧啶)與安慰劑聯合化療(順鉑+紫杉醇/5-氟尿嘧啶)一線治療不可切除的區域性晚期、複發性或轉移性食管鱗癌患者的隨機、雙盲、國際多中心III期研究。北京大學腫瘤醫院沈琳教授在本次ESMO大會上代表國際研究團隊報告中期分析[2]結果:達到全部研究終點,顯著延長總體人群的OS和PD-L1陽性人群的OS。這是食管癌治療領域首個由中國專家引領的免疫一線治療的國際多中心研究。
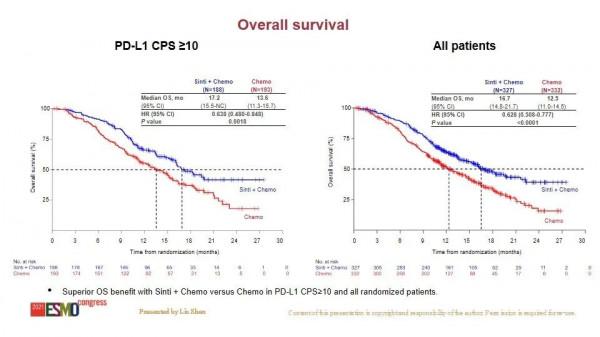
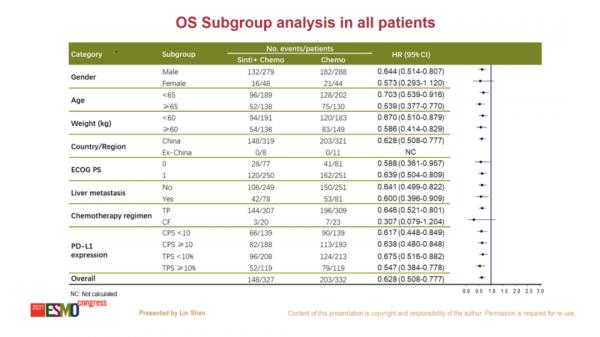
在總體人群中,信迪利單抗聯合化療組較化療組顯著延長中位OS,兩組的中位OS分別為16.7個月和12.5個月,顯著降低死亡風險37.2%,風險比(HR)為0.628。
在PD-L1陽性(CPS≥10)人群中,信迪利單抗聯合化療較安慰劑聯合化療亦顯著延長中位OS,兩組的中位OS分別為17.2個月和13.6個月,降低死亡風險36.2%,HR為0.638,p=0.0018。而且,在預設的所有亞組分析中均觀察到一致的OS獲益。
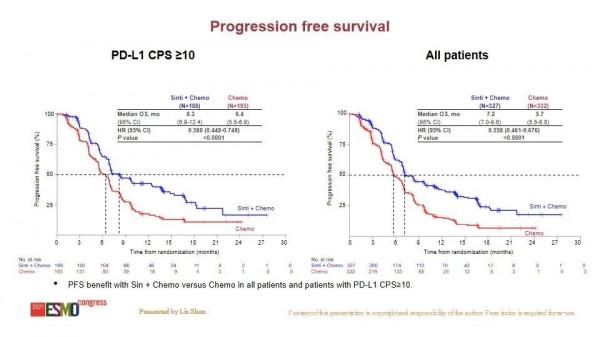
信迪利單抗聯合化療組同樣觀察到中位PFS的顯著延長。在總體人群中,兩組的中位PFS分別為7.2個月和5.7個月,HR為0.558,p<0.0001;在PD-L1陽性(CPS≥10)人群中,兩組的中位PFS分別為8.3個月和6.4個月,HR為0.580,p<0.0001。
此外,在總體人群和PD-L1陽性(CPS≥10)人群中,信迪利單抗聯合化療相比化療,ORR和DOR均顯著改善。信迪利單抗聯合化療,安全性和耐受性良好,未見新的安全訊號。
該研究結果顯示,在不可切除的區域性晚期、複發性或轉移性食管鱗癌患者一線治療中,無論PD-L1表達如何,信迪利單抗聯合化療都顯著改善OS和PFS。信迪利單抗聯合化療為這些患者提供了更優的一線治療方案。
Pemigatinib:疾病控制率100%,中國晚期膽管癌患者二線治療新希望
復旦大學附屬中山醫院施國明教授帶來的一項壁報研究[3]展示了pemigatinib二線治療中國晚期膽管癌人群中的II期研究結果。
本研究是一項II期、開放、單臂、多中心、評價pemigatinib在既往接受過至少一種系統性治療失敗、成纖維細胞生長因子受體2(FGFR2)基因融合或重排陽性的中國晚期膽管癌患者中的療效和安全性的研究,為FIGHT-202研究(INCB 54828-202,NCT02924376)的國內橋接試驗。
肝內膽管癌是第二常見的原發性肝癌,對於晚期肝內膽管癌患者而言,一線治療優選方案是吉西他濱聯合順鉑等,ORR為26%,中位OS約11.7個月,治療效果有限。目前國內一線治療失敗的患者推薦積極症狀控制+mFOLFOX方案進行治療,中位OS僅為5-6個月,亟待可以提高患者生活質量和療效的藥物出現。
FGFR2基因易位形成融合基因是肝內膽管癌中最常見的FGFR變異。Pemigatinib是FGFR亞型1/2/3的強效選擇性抑制劑,對於存在FGFR2融合或重排的患者,國外研究已證明其有效性和安全性。
截至2021年1月29日,第一部分為在中國人群中的PK研究,共納入3例膽管癌受試者;第二部分共納入31例FGFR2基因融合或重排陽性的膽管癌受試者,按照每3週一個治療週期(服藥兩週,停藥一週)口服9mg(第一部分)或13.5mg(第二部分)的pemigatinib,直到疾病進展、不可耐受的毒性或撤回知情同意書等。臨床試驗主要終點為研究第二部分納入的31例受試者達到獨立影像評估委員會(IRRC)依據RECIST v1.1標準評估的ORR。
研究結果顯示,在研究第二部分30例療效可評價人群中(1例受試者入組後因中心實驗室發現FGFR基因變異丰度不符合入選標準而被排除出療效可評價人群),15例患者達到IRRC確認的疾病緩解,主要終點指標ORR達到50%(95%CI:31.3%-68.7%)。中位隨訪5.13個月時,12例患者仍處於病情緩解中,中位DOR尚未達到(95%CI:3.4-NR),中位PFS為6.3月(95%CI:4.9-NR),疾病控制率(DCR)為100%(95%CI:88.4%-100%)。
此外,pemigatinib的安全性良好。安全性分析納入所有34例患者,至資料截止日期,每例受試者均報告至少一項治療相關不良事件(TRAE),其中最常發生的TRAE為高磷酸血癥(73.5%)、口腔乾燥(55.9%)和脫髮(50.0%),≥3級的TRAE發生率為14.7%。試驗期間未發生導致死亡和治療終止的不良事件。
該研究結果提示,對於FGFR2基因融合或重排陽性的中國復發或轉移性膽管癌患者,pemigatinib是一種高效且可耐受的二線治療選擇。
小結:
我國是消化道腫瘤高發國家,胃癌、食管癌和肝膽腫瘤發病均位居惡性腫瘤前列。在2021年ESMO大會消化道腫瘤治療專場總結討論環節,來自紐約紀念斯隆凱特琳癌症中心(Memorial Sloan Kettering Cancer Center)消化腫瘤治療中心主任Yelena Y.Janjigian教授點評道:有關信迪利單抗的兩項大型III期臨床研究,整個研究的執行與結果令人印象深刻,奠定了信迪利單抗聯合化療在一線治療的重要地位。ORIENT-15的研究結果也會改變她在美國的臨床實踐,讓她思考使用PD-1抑制劑聯合順鉑+紫杉醇作為晚期食管鱗癌的一線標準治療。
信迪利單抗聯合化療一線治療晚期胃癌的ORIENT-16研究和一線治療食管鱗癌的ORIENT-15研究均獲得陽性結果,顯著延長OS,為此類患者帶來了新的標準一線治療選擇。
同時,pemigatinib作為首款膽管癌靶向藥物,已在美國、歐洲和中國臺灣獲批上市,中國的上市申請已被國家藥品監督管理局(NMPA)受理。本項中國晚期膽管癌人群中的II期研究,DCR高達100%,ORR達50%,且安全性良好,在不久的將來會為國內膽管癌患者的二線治療提供新的方案。
參考資料:
[1]J.Xu,H.Jiang,Y.Pan,et al.Sintilimab plus chemotherapy(chemo)versus chemo as first-line treatment for advanced gastric or gastroesophageal junction(G/GEJ)adenocarcinoma(ORIENT-16):First results of a randomized,double-blind,phase III study.ESMO 2021,LBA53.
[2]L.Shen,Z.Lu,J.Wang,et al.Sintilimab plus chemotherapy versus chemotherapy as first-line therapy in patients with advanced or metastatic esophageal squamous cell cancer:First results of the phase III ORIENT-15 study.ESMO 2021,LBA52.
[3]G.Shi,X.Huang,T.Wen,et al.Efficacy and safety of pemigatinib in Chinese patients with unresectable,advanced/recurrent or metastatic intrahepatic cholangiocarcinoma with FGFR2 fusion or rearrangement that failed to prior systemic therapy.ESMO 2021,50P.
*此文僅用於向醫學人士提供科學資訊,不代表本平臺觀點
*醫學界力求其發表內容在稽核透過時的準確可靠,但並不對已發表內容的適時性,以及所引用資料(如有)的準確性和完整性等作出任何承諾和保證,亦不承擔因該些內容已過時、所引用資料可能的不準確或不完整等情況引起的任何責任。請相關各方在採用或者以此作為決策依據時另行核查。