近日,日本慶應義塾大學研究團隊表示,他們已成功地將幹細胞移植到一名脊髓損傷患者體內。據悉,這是全球首例利用誘導多能幹細胞衍生細胞治療脊髓損傷的臨床試驗。
脊髓損傷是一種嚴重的致殘性疾病,目前還沒有有效的治療手段來治療嚴重的脊髓損傷引起的癱瘓。該研究團隊探討能否利用誘導多能幹細胞(iPS)治療脊髓損傷。iPS細胞是透過刺激成熟的、已經分化的細胞回到幼年狀態而產生的。然後,再促使它們再次分化成熟為不同種類的細胞,這項臨床試驗使用的是iPS細胞衍生的神經幹細胞。
試驗的第一步是透過手術將200多萬個iPS來源的細胞植入患者的脊髓,初始階段旨在評估移植方法的安全性,患者將接受長達三個月的監測,以評估這項研究是否可以安全地繼續進行,其他受試者是否可以接受移植。此外,該研究團隊還希望觀察干細胞移植是否會改善神經功能和生活質量[1]。
幹細胞有潛力治療不同病理階段的脊髓損傷
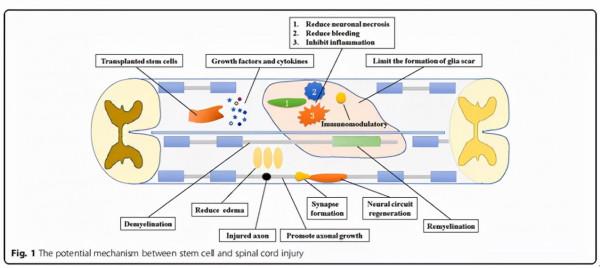
脊髓損傷病理期可根據時間分為三期:急性期(< 48 h)、亞急性期(48 h~14 d)和慢性期(> 6 月)。由於每個時期的病理生理學特點不同,因此必須根據這些獨特的情況選擇合適的細胞治療方法。
在急性期,損傷區域會發生強烈的炎症反應以及氧化應激。因此,在急性期進行抗炎以及抗氧化治療尤為重要。以間充質幹細胞(MSCs)、神經幹細胞(NSCs)等為主的幹細胞型別可分泌抗炎因子、細胞因子、生長因子和細胞粘附因子等,改善損傷微環境,進一步促進脊髓損傷後的自我修復以及抗凋亡作用。
急性期過後的亞急性期,此時期受損和剝落的軸突退化或回縮。在此期間,調節軸突生長的治療應放在首位。胚胎幹細胞(ESCs)和間充質幹細胞(MSCs)通常用於促進軸突的再生和生長。
圖片來自文獻[2]
慢性期應將促進髓鞘重新形成視為首要目標,髓鞘再生與衍生自神經幹細胞(NSCs)或少突膠質前體細胞(OPC)的少突膠質細胞密切相關[2]。
不同型別幹細胞在脊髓損傷治療中的研究進展
目前,大量有關幹細胞治療脊髓損傷的動物和臨床研究證明,細胞療法可能是一種可行的脊髓損傷治療手段。在美國國立衛生研究院的最大臨床試驗註冊庫http://clinicaltrials.gov網站我們發現目前臨床上有63項與脊髓損傷相關的幹細胞治療登記在案,使用的幹細胞型別涉及誘導多能幹細胞,間充質幹細胞,胚胎幹細胞等。
NO.1
誘導多能幹細胞(iPSCs)
iPS細胞是透過病毒介導的基因轉染、靶向插入、基因轉座子插入等手段將成熟的、已經分化的體細胞重程式設計為幼稚細胞。此外,由於體細胞通常是從患者自身的細胞中分離出來的,所以可以防止免疫排斥的發生。上述日本研究團隊所進行的是全球首例利用誘導多能幹細胞衍生細胞治療脊髓損傷的臨床試驗,是在大量動物試驗的基礎上進行的。
研究表明[3],iPS細胞分化形成的神經幹細胞可促進髓鞘再生、軸突再生和神經營養因子的分泌,同時減少炎症。動物試驗顯示[4],當iPS細胞被誘導分化為少突膠質細胞或神經元,然後再移植到大鼠、小鼠或靈長類長尾猴脊髓挫傷模型中,3~5 周後,運動功能明顯改善,且無腫瘤發生。
圖片來自文獻[4]
不過誘導多能幹細胞的臨床發展也面臨著一定的侷限性,比如操作複雜且重程式設計效率低,有誘導突變的可能,長期安全性尚未得到證實等,因此仍然需要大量的臨床研究進行探討。
NO.2
間充質幹細胞(MSCs)
間充質幹細胞(MSCs)因來源易得、生物學效應廣泛、無倫理學問題、免疫原性低等優點,已成為再生醫學領域最受歡迎的種子細胞。間充質幹細胞可從骨髓、臍帶、胎盤和脂肪組織中提取。儘管不同組織來源的MSCs的特性不同,但其在治療各種中樞神經系統疾病方面均顯示出良好的療效。MSCs生物治療作用的機制主要是MSCs進入病灶部位後,透過旁分泌訊號釋放大量抗炎因子、細胞因子、生長因子和細胞粘附因子,改善病變區域性微環境,促進受損組織細胞的自我修復。
國外進行的一項臨床試驗[5]證實了鞘內注射臍帶間充質幹細胞治療慢性完全性脊髓損傷的臨床療效,接受注射後,患者各項功能及生活質量均有不同程度改善。
NO.3
成體內源性幹細胞(AESCs)
成體內源性幹細胞(AESCs)是位於成體神經系統的幹細胞。在脊髓組織中,脊髓中央管附近的室管膜細胞、放射狀膠質細胞和條狀細胞具有幹細胞特徵。
正常情況下,這些細胞處於休眠狀態。一旦脊髓受損,這些細胞就會迅速啟用和增殖,分化為星形膠質細胞和少突膠質細胞,進一步形成膠質瘢痕,抑制病變擴張和再髓鞘形成。一些研究人員已經將這些細胞移植到由於脊髓損傷引起偏癱的動物模型中,觀察到動物運動功能的顯著改善。
這些報告為非侵入性細胞治療帶來了希望,因為這些內源性幹細胞能夠被直接啟用以發揮作用,而不需要外源性細胞移植。
未來:幹細胞聯合生物材料與藥物治療
幹細胞療法在重建受損脊髓和促進功能恢復方面顯示出巨大的潛力,目前有許多臨床前以及臨床研究正在火熱進行中。
正如上述全球首例臨床試驗負責人應義塾大學中村雅教授所說:“這絕對是向前邁出的一大步,但在治療可以投入使用之前,還有很多工作要做。”因此,未來仍然需要進行反覆實踐及論證,以實現臨床轉化和應用。
此外,未來還應形成以幹細胞為中心,聯合生物材料和藥物治療在內的綜合治療方案,以期為脊髓損傷患者提供最大幫助。
參考文獻:
[1]https://www.france24.com/en/live-news/20220114-japan-team-carries-out-world-first-spinal-cord-stem-cell-trial
[2] Shao A, Tu S, Lu J, Zhang J. Crosstalk between stem cell and spinal cord injury: pathophysiology and treatment strategies. Stem Cell Res Ther. 2019 Aug 6;10(1):238.
https://pubmed.ncbi.nlm.nih.gov/31387621/
[3] Yousefifard M, Rahimi-Movaghar V, Nasirinezhad F, Baikpour M, Safari S, Saadat S, Moghadas Jafari A, Asady H, Razavi Tousi SM, Hosseini M. Neural stem/progenitor cell transplantation for spinal cord injury treatment; A systematic review and meta-analysis. Neuroscience. 2016 May 13;322:377-97.
https://pubmed.ncbi.nlm.nih.gov/26917272/
[4] Kawabata S, Takano M, Numasawa-Kuroiwa Y, Itakura G, Kobayashi Y, Nishiyama Y, Sugai K, Nishimura S, Iwai H, Isoda M, Shibata S, Kohyama J, Iwanami A, Toyama Y, Matsumoto M, Nakamura M, Okano H. Grafted Human iPS Cell-Derived Oligodendrocyte Precursor Cells Contribute to Robust Remyelination of Demyelinated Axons after Spinal Cord Injury. Stem Cell Reports. 2016 Jan 12;6(1):1-8.
https://pubmed.ncbi.nlm.nih.gov/26724902/
[5] Albu S, Kumru H, Coll R, Vives J, Vallés M, Benito-Penalva J, Rodríguez L, Codinach M, Hernández J, Navarro X, Vidal J. Clinical effects of intrathecal administration of expanded Wharton jelly mesenchymal stromal cells in patients with chronic complete spinal cord injury: a randomized controlled study. Cytotherapy. 2021 Feb;23(2):146-156.
https://pubmed.ncbi.nlm.nih.gov/32981857/