隨著靶向治療、免疫治療進入臨床晚期肺癌的生存期有了明顯延長,但耐藥之後的後線仍然依賴化療。近年新興的“合成致死”藥物ATR抑制劑進入臨床研究階段,有望提高後線化療療效,在肺癌領域默克的ATR抑制Berzosertib在非小細胞肺癌和小細胞肺癌後線治療上均顯示出潛力。
ATR抑制“合成致死”助力化療
ATR是一種重要激酶,夠啟用細胞應答,進而阻滯細胞週期程序並穩定複製叉及修復DNA,從而回避細胞凋亡。當細胞內DNA複製壓力、DNA損傷產生時(比如放化療),ATR被募集至DNA損傷部位修復斷裂的DNA雙鏈,通俗地講ATR就是DNA的修理工。
“合成致死”是指在腫瘤細胞中,由於一個DNA修復通路發生突變導致的缺陷,使得腫瘤細胞比正常細胞更依賴另一個互補的DNA修復通路,因此抑制互補的DNA修復通路就會對腫瘤細胞造成“合成致死”。而正常細胞由於還有一個DNA修復通路是正常的,因此不會在藥物抑制下死亡。通俗地講“合成致死”就是讓腫瘤細胞依賴的DNA修理工癱瘓,那麼腫瘤細胞在放化療打擊下將很難恢復。
Berzosertib(VX-970,M6620)是默克公司研發的一款首創、強效、選擇性,靜脈輸注的ATR抑制劑,目前非小細胞肺癌和小細胞肺癌的均已進入臨床研究階段。
Berzosertib聯合拓撲替康治療小細胞肺癌
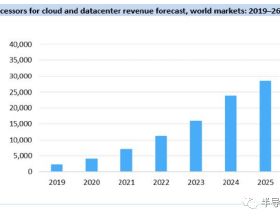
拓撲替康是小細胞肺癌(SCLC) 二線治療的標準化療藥,但緩解率較低(20%左右),特別是治療鉑耐藥患者緩解率更低(10%左右)。但即使如此低的療效,目前仍沒有藥物能撼動拓撲替康SCLC二線標準化療藥物的地位。
圖一 Lurbinectedin、拓撲替康、氨柔比星、納武利尤單抗二線治療SCLC療效
拓撲替康為TOP1 抑制劑,TOP1是一種抑制基因組不穩定性的核酶,拓撲替康透過抑制TOP1,損傷腫瘤細胞的DNA,導致腫瘤細胞死亡。而Berzosertib作為ATR抑制劑可以阻止腫瘤細胞修復DNA損傷,使腫瘤細胞無法從拓撲替康的打擊中恢復,從而增強拓撲替康的療效。
美國國家癌症研究所(NCI)開展一項II期概念驗證研究以驗證上述設想。NCI開展的這項II期概念驗證研究是一項單臂研究,在先前接受過治療後病情進展的SCLC患者中開展,評估了Berzosertib+拓撲替康聯合用藥方案的療效和安全性。共有25例患者可評估研究主要終點客觀緩解率(ORR),研究次要終點無進展生存期(PFS)和總生存期(OS)以及緩解持續時間(DOR)。研究中,患者接受Berzosertib(第2、5天靜脈給藥210mg/m2,21天為一個週期)和拓撲替康(第1-5天靜脈給藥1.25mg/m2,21天為一個週期),治療直至疾病進展。
結果顯示:確認的ORR為36% (95%CI:18.0-57.5;均為部分緩解[PR])。大多數患者(68.0%)出現腫瘤消退。在鉑敏感(60.0% [95%CI:14.7-94.7])和鉑耐藥(30.0% [95%CI:11.9-54.3])患者中均觀察到緩解。中位DOR為6.4個月(95%CI:1.1-14.3),病情緩解的6例鉑耐藥SCLC患者中有4例(66.7%)DOR大於6個月,其中2例超過1年(分別為13個月和24個月)。中位PFS為4.8個月(95%CI:2.8-7.4),4個月和6個月PFS率為60.0%(95%CI:38.4-76.1)和36.0%(95%CI:18.2-54.2)。中位OS為8.5個月(95%CI:5.6-13.6),6個月和12個月OS率分別為68.0%(95%CI:46.1-82.5)和32.0%(95%CI:15.2-50.2)。
在26例可評價安全性的患者中,最常見的治療相關不良事件(AE)為貧血(96.2%)、淋巴細胞減少(96.2%)、血小板減少(92.3%)、中性粒細胞減少(50.0%)、噁心(50.0%)和嘔吐(42.3%)。最常見的3級或4級AE為淋巴細胞減少(69.2%)、血小板減少(57.7%)、貧血(53.8%)、中性粒細胞減少(15.4%)。未發生與治療相關的死亡。大多數AE歸因於拓撲替康,而拓撲替康作為單藥治療與高頻率的骨髓抑制相關。
Berzosertib+拓撲替康治療SCLC顯示出較高的緩解率和持久的緩解,尤其是在鉑耐藥患者中也有持久的療效。NCI還正在進行另一項II期研究(NCT03896503),評估berzosertib+拓撲替康聯合用藥方案對比拓撲替康單藥方案治療複發性小細胞肺癌,進一步驗證berzosertib+拓撲替康的療效。
此外,默克雪蘭諾還啟動了一項全球性、開放標籤、單臂II期研究(DDRiver SCLC 250),以進一步評估Berzosertib+拓撲替康治療複發性鉑耐藥小細胞肺癌的療效,首例患者已入組研究。該研究計劃納入包括亞洲、歐洲和北美約41個研究地點約80例患者。
Berzosertib聯合吉西他濱治療非小細胞肺癌
Berzosertib聯合吉西他濱治療卵巢癌展現出無進展生存期的明顯改善,臨床前已顯示Berzosertib 使肺癌細胞對誘導 DNA 損傷的化療藥物(如吉西他濱)敏感,TP53 突變狀態與對 DNA 損傷劑和 ATR 抑制的反應相關。為此開展一項IB期臨床研究評估Berzosertib聯合吉西他濱治療伴有或不伴有TP53突變的晚期非小細胞肺癌( NSCLC) 患者的安全性、耐受性、藥代動力學 (PK) 和初步療效,還對潛在反應生物標誌物進行了探索性分析。
研究納入38例經治NSCLC患者,多數接受過二線治療。有確定基因狀態的患者中60.5%為TP53突變。所有患者均接受過化療,15.8%的患者接受過免疫治療。
入組患者接受吉西他濱(1000 mg/m 2;第 1 天和第 8 天)後約 24 小時接受 Berzosertib(210 mg/m 2;第 2 天和第 9天),每21天為一個週期。患者接受治療直至疾病進展(PD)或出現不可接受的毒性。
結果有有四例確認的部分緩解(ORR 10.5%),其中兩例患者有特別顯著的緩解,分別持續緩解13.2個月和6.0個月,先前均經過至少兩線治療。中位PFS為 4.0個月 [90%CI: 3.2–5.0],中位OS為7.4個月 [90%CI: 5.4–8.5],中位DOR為6.0個月 [90%CI: 3.6–nd]。
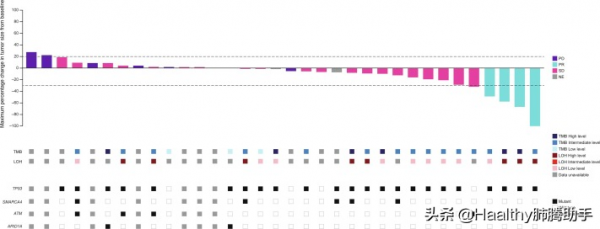
圖二 Berzosertib聯合吉西他濱治療後腫瘤變化瀑布圖及對應的基因特徵
29 例患者NGS檢測結果質量合格。NGS分析未證明臨床結果(ORR 和 PFS)與探索的 324 個基因(包括TP53)和其他潛在的 ATR 抑制敏感性預測生物標誌物(包括ATM、ARID1A和SMARCA4 )的任何改變之間存在明確關聯。就是說TP53、ATM、ARID1A和SMARCA4的狀態不能預測Berzosertib聯合吉西他濱的療效。
19 例患者可測量 LOH(雜合性丟失)。高 LOH 患者的 ORR 為 30.0% (3/10, 90% CI: 9.0–61.0%),低 LOH 患者的 ORR 為 11.0% (1/9, 90% CI: 1.0–43.0%)。
25 例患者可測量 TMB(腫瘤突變負荷)。高 TMB 患者的 ORR 為 33.0%(2/6,90% CI:6.0-73.0%),中等 TMB 患者的 ORR 為 12.5%(2/16,90% CI:2.0-34.0%),低 TMB 患者的ORR為0% (0/3, 90% CI: 0.0–53.6%)。
最常見的治療期間不良事件(TEAE,任何級別)是疲勞(55.3%)、貧血(52.6%)和噁心(39.5%)。最常見的 Berzosertib 相關 TEAE 是疲勞 (44.7%)、貧血 (39.5%) 和血小板減少症 (28.9%)。此外,22 例(57.9%)患者經歷了與 Berzosertib 相關的≥ 3 級 TEAE,14 例(36.8%)患者經歷了與Berzosertib 相關的嚴重 TEAE。
5 例患者經歷了與 Berzosertib 相關的 TEAE(中性粒細胞減少症、血小板減少症、疲勞、天冬氨酸氨基轉移酶和 ALT 升高),並導致 Berzosertib 減量。11 例 (28.9%) 患者終止使用 Berzosertib 治療,其中 7 例 (18.4%) 患者主要因 TEAE 停止治療;其中三例(7.9%)是由於 Berzosertib 相關的 TEAE(貧血、血小板減少和疲勞)。四例(10.5%) 患者經歷了導致死亡的 TEAE。四例死亡中的一例(2.6%)與研究治療有關(咯血、低血容量性休克和心臟驟停),該名患者在經歷 3 級下呼吸道感染和呼吸急促(均與治療無關)> 1 個月後死亡。
總的來說未經選擇的NSCLC患者接受Berzosertib聯合吉西他濱治療未顯示出明顯的獲益,未來需探索以基因組特徵(TMB或LOH)選擇受益於聯合治療的患者,此外Berzosertib的毒性有可能與吉西他濱疊加,主要是骨髓抑制,導致較多患者終止用藥,要注意安全性。