驅動基因的發現和靶向藥物的研發,使得非小細胞肺癌(NSCLC)這一肺癌亞型,由組織學分型進入更為精準的分子分型,真正開啟了非小細胞肺癌個體化診治時代的大門。針對表皮生長因子受體(EGFR)的小分子酪氨酸激酶抑制劑(TKI),目前已有三代藥物進入臨床,為存在EGFR這一驅動基因突變的非小細胞肺癌患者帶來了諸多治療選擇。
奧希替尼(Osimertinib)是第三代EGFR-TKI,現已獲批用於:
- 一線治療存在EGFR敏感突變的晚期非小細胞肺癌;
- 經前代EGFR-TKI治療後存在T790M耐藥突變的晚期非小細胞肺癌的後續治療;
- 存在EGFR敏感突變的非小細胞肺癌患者根治術後的輔助治療
藥物的這些適應症,離不開優秀的大型臨床試驗資料。然而,臨床試驗是群體性研究,在臨床實際應用中,個體更值得關注。近期,一項病例報道顯示:奧希替尼使晚期非小細胞肺癌骨轉移患者病灶達到完全病理緩解。
病例故事
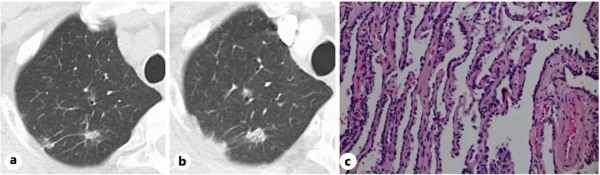
A先生70歲時,每年的常規體檢發現右肺下葉的一個病灶在逐步增大(圖1a),到醫院就診。醫生仔細觀察了病灶形態,感覺惡性可能性大,建議A先生在完善全身檢查排除轉移後,做手術切除病灶。
全身檢查沒有發現其他部位有可疑病灶,病變屬於很早期。因此,A先生接受了胸腔鏡下右下肺切除+淋巴結清掃術,手術很順利。病理醫生對手術切除標本進行塗片染色,確診A先生為肺腺癌(圖1b),進一步的基因檢測,提示A先生的腫瘤存在EGFR 21號外顯子L858R這一驅動基因突變。術後兩個月,A先生開始口服藥輔助化療,以便更好地清除體內潛在的“微轉移”。
術後隨訪是每一位腫瘤患者的必修課。術後6個月時,一次胸部CT複查偶然發現A先生右側第8肋骨存在一塊明顯的溶骨性病灶,進一步的PET-CT顯示,此處最大標準吸收值高達5.4(圖2a),提示骨轉移病灶可能大。A先生病情復發了。
醫生與A先生做了充分的溝通,考慮到A先生存在EGFR 21L858R突變,且病情進展快,醫生建議他直接服用第三代EGFR-TKI,即奧希替尼。A先生同意了這一治療策略,馬上開始服藥(80mg每日)。
之後A先生進入了服藥後隨訪階段。奧希替尼治療1個半月後,A先生的癌胚抗原(CEA)水平相比治療前有明顯下降,治療6個月後,CEA水平已在正常範圍內。奧希替尼治療1年時,CT顯示肋骨病灶發生了大面積鈣化,提示腫瘤活性大大下降(圖2b)。
考慮A先生治療後疾病穩定,且隨訪其他部位沒有發生遠處轉移,醫生決定為A先生再次行手術治療,將病變的肋骨和肺部非浸潤性的病灶一併切除。對切除的病灶進行常規的病理檢查,醫生髮現A先生骨病灶上竟然沒有了存活的腫瘤細胞(圖2c、d),達到了病理學完全緩解(pCR);影像學上原有的病變(圖3a、b)被確證為非浸潤性腺癌(圖3c)。8天后,A先生出院了,沒有再接受包括奧希替尼治療在內的全身治療。
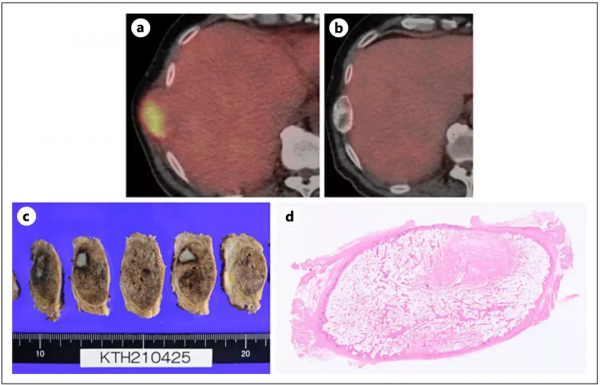
圖2. 肋骨轉移的影像學(a、b)、手術樣本(c)及病理染色(d)
小結與啟示
本例手術復發後,透過奧希替尼治療,骨轉移病灶內腫瘤活性明顯下降。在此基礎上,進行骨寡轉移灶的手術切除,達到了病理完全緩解,再一次印證了奧希替尼的效果。
靶向治療後進行手術的情況在臨床上相對是很少見的,而且影像學對骨轉移病灶活性的評估也不是絕對的。這一例中,考慮肋骨病灶是寡轉移灶,醫生為其進行了手術,術後病理恰巧為完全緩解狀態。後續A先生要求不進行包括奧希替尼在內的全身治療,至於“無病生存期(DFS)”時間多久,需要進一步隨訪來看。如果無病生存期達到預期,那麼治療可以說是成功的。
靶向治療和免疫治療,為非小細胞肺癌個體化診療帶來了諸多的治療手段。但臨床情況複雜多變,具體到個例,臨床醫生還需為患者提供更加精準化的診斷和治療選擇。相信分子分型時代的最佳化策略,定會使患者會活得更久,活得更好。
參考文獻:Hiroshi Shintani, et al. Bone Metastasis of Non-Small-Cell Lung Cancer Showing Pathological Complete Response to Osimertinib Monotherapy. Case Rep Oncol 2021;14:1876-1881.