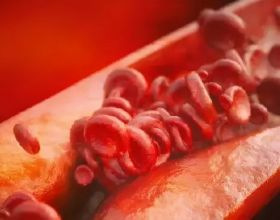
一年前,美國俄勒岡州的昆茲曼一家遇到了些意外——13歲的馬修·昆茲曼(Matthew Kunzman)突然咳嗽不已,並伴有高燒。在疫情期間,任何類似新冠的症狀都會引起人的高度警覺,而醫生的診斷結果喜憂參半:好訊息是馬修沒有得新冠,壞訊息是馬修的症狀可能源自心臟。
▲馬修·昆茲曼是受益於這項技術12名患者之一(圖片來源:參考資料[2];Courtesy of Jenny Kunzman)
當地的醫生告訴馬修的父母,他的身上有心肌炎的徵兆。這是一種心臟出現的炎症,使這個重要器官難以維持正常功能,無法把足夠的血液送至全身。後續的檢測結果證實了這一猜測:馬修的心臟功能正在衰竭,這超出了當地診所的治療能力。醫生們推薦馬修立刻前往斯坦福醫院就診,那裡可能保住馬修的一條命。
馬修短暫躲過了死神的這次突然襲擊。幾個小時後,他的父親帶他飛到了斯坦福就診。第二天,他的情況就迅速惡化。當他母親次日抵達時,他已經用上了生命支援系統。如果再晚上幾天,後果可能不堪設想。
尤安·阿什利(Euan Ashley)是斯坦福大學醫學院的一名教授,也是一名遺傳學和生物醫學資料方面的專家。聽說馬修的病例後,他的心裡萌生出了不同的看法——總體而言,馬修是一名非常健康的年輕人。突發心衰,主要可能有兩個原因:其一就是俄勒岡醫生的診斷,即由於病毒或者其它身體不適誘發的心肌炎;其二則是遺傳學上的原因,某個基因突變帶來的影響,在日積月累之下,終於壓垮了馬修的心臟。
▲本研究的負責人尤安·阿什利教授(斯坦福醫學院)
這兩個原因各有各的可能,卻有著完全不同的治療方案——心肌炎往往是可逆的。透過治療,心臟功能可以恢復正常水平。但基因突變帶來的心臟病則不然。如果病因真的是基因缺陷,唯一的治療方案就是心臟移植。
阿什利教授課題組的約翰·戈爾津斯基(John Gorzynski)博士聯絡了馬修的父母,介紹了他們實驗室正在進行的一項基因組快速測序的研究,並徵求許可,將馬修納入到這項研究中。對於這個請求,馬修的父母當即同意下來。他們迫不及待地想知道,馬修究竟是得了什麼病。
徵得同意後,研究人員們抽取了幾毫升馬修的血液,送去做快速的基因組測序。幾小時後,測序結果返回,顯示馬修的基因組裡確實有著導致疾病的基因突變。獲取這一資訊後,醫生們立即將馬修放到了心臟移植的等待列表上。過了三週,他等來了一顆全新的心臟。一年後的今天,馬修的母親說他依然活得很健康。
喜悅之餘,他們可能沒有想到馬修參與的是一項具有里程碑意義的研究。替馬修做出關鍵診斷的技術,僅在短短數小時內就完成了全基因組的測序。“通常來說,如果能在幾周時間裡完成對患者基因組的測序,並返回結果,大部分醫生就會說很迅速了。” 阿什利教授說道。
圖片來源:123RF
在世紀之交,當人類首次完成基因組草圖的繪製時,或許少有人能預料到在短短二十多年後,基因組測序竟能成為診斷個體疾病的工具——當時,為了完成基因組草圖,多個國家的科學家們耗時十餘年,耗費了近30億美元的資金。放在任何一個個體身上,這都是難以想象的天文數字。
而如今,隨著分子生物學技術的發展,基因組測序技術的門檻不斷下降。數年前,商業化的個體基因組測序便已成為了可能。幾千美元,幾周時間,一份屬於自己的生命藍圖就將測序完成。在有經驗的醫生眼中,這份藍圖裡還蘊藏著遺傳疾病的蛛絲馬跡,也有著通往治療疾病方向的指示牌。
▲人類基因組的測序成本在過去二十年迅速下降(圖片來源:Wetterstrand KA. DNA Sequencing Costs: Data from the NHGRI Genome Sequencing Program (GSP) Available at: www.genome.gov/sequencingcostsdata. Accessed 01/13/2021.)
但正如阿什利教授所言,現有的基因組測序技術和世紀之交相比已經變迅速了不少,但對於馬修這樣的危重症患者,還是太慢了。傳統的幾周測序時間,普通健康人還等得起,馬修等不起。為了對類似馬修的患者做出及時診斷,研究人員們還需要開發出更為快速的測序技術。快速測序意味著更快的診斷,更快的治療,也意味著患者可能會在重症病房待上更短的時間,或是更快康復。更關鍵的是,這種速度上的提升,還不能犧牲準確度。
為了滿足這一需求,研究人員們想到了“奈米孔”技術。這是一種已經在基因測序中得到廣泛應用的技術,它的原理也很容易理解——當長鏈DNA分子透過奈米尺寸的空隙時,會隨著鹼基的不同,產生相應的電流變化。而透過儀器識別這種電流變化,就可以反推出相應的鹼基,從而還原DNA的序列。
阿什利教授聯絡了牛津奈米孔技術公司,並使用了該公司開發的PromethION 48測序系統。這套系統裡一共有48個測序流動池(flow cell),每一個流動池都能單獨完成基因組測序的工作。而為了節省時間,研究人員們決定讓48個流動池同時工作,極大加快速度。
▲奈米孔技術對DNA測序的示意圖(圖片來源:DataBase Center for Life Science (DBCLS), CC BY 4.0 <https://creativecommons.org/licenses/by/4.0>, via Wikimedia Commons)
並行的測序固然提高了速度,卻也產生了海量資料,超過了實驗室的分析能力。為此,研究團隊進一步將資料傳到雲端,擴大計算能力。同時,團隊也開發了一些演算法,在掃描測序獲得的遺傳資訊的同時,尋找可能導致遺傳疾病的突變。最後,科學家們還會拿尋找到的基因變異去和公開發表的論文進行比對,進行確認。
在2020年12月到2021年5月間,研究人員們在兩家位於斯坦福的醫院招募了12名患者,使用上述的技術進行了快速的基因組測序,用於輔助診斷。昨日,科學家們在《新英格蘭醫學雜誌》上介紹了他們的階段性工作成果。根據介紹,從收集患者血樣到獲得初步診斷結果,最短的時間僅為7小時18分鐘。
速度當然是這項工作非常引人注目的一點。根據斯坦福醫學院的新聞稿,在一個病例中,如果去除診斷環節,僅統計基因組的測序部分,那麼耗時僅需5小時2分鐘,這也創下了吉尼斯世界紀錄。
但速度絕非本研究的唯一亮點。事實上,奈米孔技術的一大特徵就是對長序列的測序。傳統的基因組測序方法會先將基因組打碎成小的片段進行測序,然後再以標準的人類基因組作為參照,將測序結果重新拼成一個基因組。但這樣的方法有時會錯過一些基因組片段,或是遺漏一些遺傳變異。長序列測序則能對長達幾萬個鹼基的DNA片段進行測序,提供更多的細節。
《新英格蘭醫學雜誌》的文章中提到,超過一半的測序片段超過25 kb。總體來看,每一個基因組能產生173到236 Gb的資料,序列比對一致性(alignment identity)達到94%,常染色體的覆蓋率達到46到64x。
▲本研究的示意圖(圖片來源:參考資料[1])
“透過長序列測序,更容易在大片段的基因組上找到突變,” 阿什利教授評論說,“如果不使用一些長序列測序的手段,幾乎不可能發現其中的一些變異。”
該技術還能回答透過傳統診斷技術難以回答的醫學問題。研究團隊介紹了另外一個案例——一名3個月大的嬰兒出現病因不明的癲癇,於是醫院雙管齊下,一方面使用標準的臨床基因診斷,另一方面則使用這種新型的全基因組快速測序技術。僅過了8個多小時,後者就給出了答案——這名患兒的CSNK2B基因出現了突變,它已知與神經發育疾病有關,會導致早發的癲癇。相反,標準的臨床基因診斷中則不含有CSNK2B這一項檢測內容,因此檢測返回的資訊對患者的幫助有限。
這一研究成果得到了不少醫生和科學家的關注。斯坦福的醫生們對能在幾小時內完成遺傳診斷的前景感到非常興奮,知名科學家Eric Topol教授也在其社交媒體上表示“未來已來”。
圖片來源:Eric Topol教授社交媒體截圖
當然,這一工作目前只是得到了小規模的運用,在成本和準確度上相信還有不少可以最佳化的空間。但這一先驅性的嘗試已向我們證明,基因組的快速測序有望成為診斷的重要一環,為懷疑患有罕見遺傳疾病的患者家庭及時帶來重要的診斷資訊。快速、準確、個體化……或許,這就是未來醫療診斷的模樣。
參考資料:
[1] John E. Gorzynski et al., (2022), Ultrarapid Nanopore Genome Sequencing in a Critical Care Setting, NEJM, DOI: 10.1056/NEJMc2112090
[2] Fastest DNA sequencing technique helps undiagnosed patients find answers in mere hours, Retrieved January 13, 2022, from https://med.stanford.edu/news/all-news/2022/01/dna-sequencing-technique.html
[3] Scientists describe new approach in NEJM, using Oxford Nanopore DNA sequencing technology to improve prognosis in critically ill patients, in less than 8 hours, Retrieved January 13, 2022, from https://nanoporetech.com/about-us/news/scientists-describe-new-approach-nejm-using-oxford-nanopore-dna-sequencing-technology