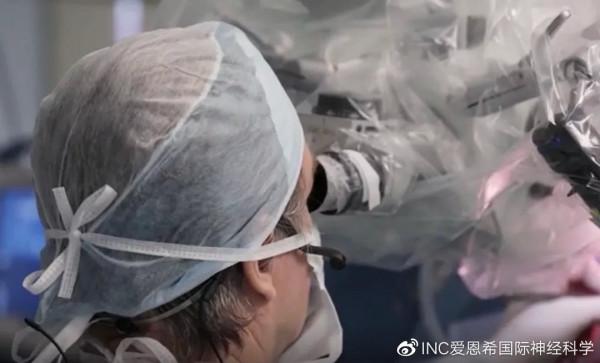
儘管現代顯微神經外科技術近來得到了很大發展,但島葉膠質瘤的治療仍然面對著許多重要問題:
島葉膠質瘤具體都可以怎麼分型?
為什麼島葉膠質瘤手術這麼高風險、容易造成手術併發症?
島葉膠質瘤患者最大切除手術是否能帶來生存益處?
腫瘤在島葉內的位置會影響圍手術期的發病率嗎?
醫生能夠根據病變的解剖位置預測切除範圍和圍手術期發病率嗎?
做手術的患者是否經歷過術後併發症,如生活質量下降、癲癇發作和神經功能障礙等?
INC德國巴特朗菲教授島葉膠質瘤安全全切案例
病史摘要:Z老師,近1年來出現反覆右臂的感覺麻木障礙,有時甚至放射延伸至右半部面部,並出現了語音障礙,單詞識別困難,伴有疲勞和精神不振,嚴重影響了工作。後就診醫院檢查發現島葉佔位,考慮島葉腫瘤引起的反覆癲癇發作。由於該位置緊靠功能區,術後發生癱瘓、認知障礙等風險極大,四處求醫不得,終獲巴特朗菲教授安全全切。
術前術後影像資料:

圖:術前MR顯示島葉佔位,直徑約為4 cm,緊鄰重要腦功能區,包繞左島葉的大部分,並在背側延伸至島葉的後部。術後MR顯示腫瘤全切,無腦出血、水腫等正常腦組織損傷。
術後情況:術後當天即拔除氣管插管,可完全自主呼吸。術後第3天,患者能獨立下床、少量活動,能自行康復鍛鍊,無癲癇發作,無構音障礙,無肢體無力、感覺障礙等,無呼吸抑制等手術相關併發症。術後第14天,出院,神志清楚,語言流利,全身狀態好,無肢體無力、感覺麻木等問題。
島葉膠質瘤手術案例解析
島葉皮層最早由德國神經學家J. C. Reil在1809年命名,是神經膠質瘤的常見好發位置。島葉內膠質瘤由於島葉皮層複雜的形狀和組織、島葉的功能意義以及與大腦內動脈、大腦中動脈和豆狀紋狀體血管的密切關係,干係著人體認知、感覺、精神、運動、語言等關鍵功能,一直以來都是手術治療的難題。考慮到這些重要因素,在當今時代之前,島葉神經膠質瘤被認為過於危險,不適合手術治療,術後併發症率、致殘率往往高得令人無法接受。
然而,在過去的 20 年裡,隨著腫瘤分子層面的深入研究加上對外科手術在新診斷和複發性膠質瘤中的作用的更全面的理解,已經說明了最大腫瘤切除程度 (EOR) 對提高整體和複發率的重要性。因此,神經外科醫生不得不為位於島葉皮質內的低級別和高級別膠質瘤開發治療模式。雖然關於正常島葉的功能仍有許多未知,但我們知道切除該區域的膠質瘤可以以較低的發病率完成。透過仔細的研究,採用解剖解剖、結構和功能成像分析、語言、運動和認知圖譜,以及對患者預後和長期發病率進行細緻的前瞻性和回顧性評估,降低圍手術期發病率的努力得以實現。
在這篇文章中,INC旗下組織世界神經外科顧問團成員、美國神經外科學會主席Mitchel Berger教授等全面回顧已發表的文獻,為島葉內低級別和高級別膠質瘤患者梳理了手術治療的發展史及積極手術的重要意義。
島葉膠質瘤多見於低級別膠質瘤,少數為高級別膠質瘤。Yasargil將島葉病變分為4型:
① 病變完全位於島葉未超過島葉環狀溝的為純島葉腫瘤
② 病變累 及島葉及額葉島蓋(眶額葉後部)的稱為島葉—額蓋病變
③ 病變位於顳底內側面 —島葉的病變稱為顳底內側面—島葉腫瘤
④ 累及島葉、眶額葉回皮質及顳極的稱 為眶額—島葉—顳極腫瘤 。
總結來說,島葉膠質瘤的治療是具有挑戰性的,原因如下:
1. 島葉在外側裂深部,不在大腦表面;
2. 覆蓋島葉的大腦皮質多為重要的功能區;
3. 外側裂區包含重要的引流靜脈。
這些因素都增加島葉膠質瘤的手術難度,然而,島葉膠質瘤的生存期與切除程度密切相關。因此,如何在保證安全的前提下儘可能全切腫瘤,確是重大的難題。
神經解剖學
島葉由額葉、顳葉及頂葉皮質覆蓋(圖1),皮質下有最外囊、屏狀核、豆狀核、外囊及內囊等結構;大量的神經網路連線優勢半球與非優勢半球島葉,表明島葉執行感覺、運動和認知等重要功能。島葉皮質接受頸內動脈和大腦中動脈分支的豐富血供。功能MRI的研究顯示,島葉具有整合感覺輸入纖維的作用,額枕下束與鉤束均穿過島葉的皮質下區。術中語言功能區的腦電描記在優勢半球島葉膠質瘤手術中有重要的指導作用。
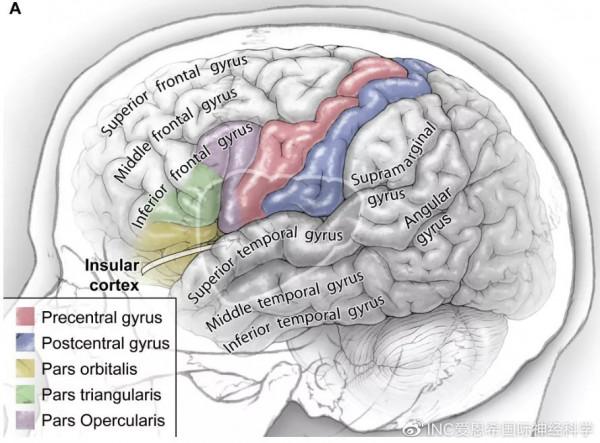
圖1:島葉由額葉、頂葉及顳葉覆蓋。三角區(綠色),島蓋部(紫色),中央前回(紅色)位於島葉前部
島葉呈上寬下窄倒三角形,平均大小5.2cm×2.9cm,表面有呈扇形分佈的溝,上環島溝位於額頂蓋下方,下環島溝位於顳蓋下方,前環島溝位於眶額蓋下方,這三個溝是確定島葉範圍的重要標誌。島前點是前、上環島溝的交叉點,距皮層外側面23~26 mm,上、下溝的交叉點是後島點,距皮層外側面30~36 mm。
前部的島下極和後部的島閾構成島下部;島閾為位於側裂蝶骨部和島蓋部的結合處呈弓形半包圍外側裂,被認為是島葉的門檻,平行於外側嗅紋走形;島下極位於島葉前下緣,其內側緣是前穿質的外側界;島葉與島蓋之間的外側裂底在橫位像上自下向上逐漸增長,在冠狀位像前向後逐漸縮短;島中央溝前後方向2cm範圍內的中央溝可以作為術中確定中央區下部的解剖標誌。
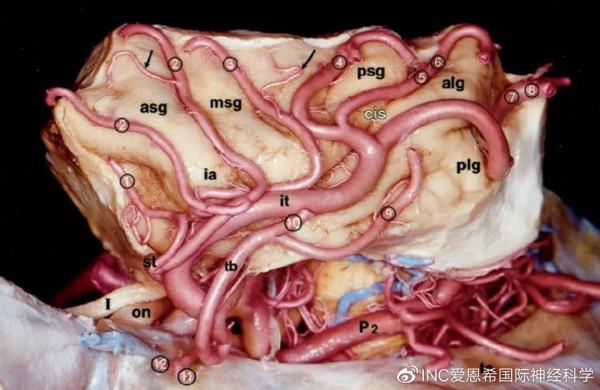
圖2:複雜的島葉血供解剖,島葉主要接受 M2 段的分支血供,若破壞了各分支血供對人體的關鍵功能有致殘影響。
島葉表面行經及供血血管主要是大腦中動脈。大腦中動脈主要分為蝶骨段(M1)、腦島段(M2)、島蓋段(M3)、側裂周圍段(M4)及終末段(M5)。其中M1段發出的豆紋動脈經過前穿質,途經杏仁核的後面,主要供血內囊區域,側面觀豆紋動脈以扇形方式放射狀延伸至幾乎整個內囊。低級別膠質瘤切除常以豆紋動脈扇形面為腫瘤切除的內側介面。島葉皮層具有豐富的血管供應,島葉的靜脈迴流由外側裂的淺表靜脈及大腦中深靜脈引流,但變異較大,各個靜脈引流區域範圍並不恆定。
島葉-複雜的神經網路連線系統
顯性和非顯性腦島內的大規模網路連線表明具有廣泛的功能意義,包括感覺、邊緣和認知等。島葉的很大一部分專門用於接收來自丘腦和皮層傳入的感覺輸入,涉及人的嗅覺、味覺、視覺、聽覺和體感資訊。總之,感覺投射是沿著島葉皮層在投射走形,但因為沒有一種模式是純粹的感覺,島葉皮層最常被認為是一個多模式整合位點。除了感覺輸入外,來自眶額和扣帶回區域的投射還與人的獎勵、驅動力和動機行為有關。與邊緣系統的聯絡,特別是中央杏仁核、背內側丘腦、下丘腦、終紋和海馬旁回,表明島葉在恐懼和焦慮中起作用。
島葉-對人體功能的意義
來自丘腦的綜合感覺傳入神經和來自與情緒處理有關的區域的傳入神經會聚在腦島和皮層下白質中。腦島對人類行為的功能影響幾乎完全基於在對大鼠進行各種任務和藥理學損傷研究期間的功能性 MRI 啟用,這兩者都未能提供將腦島內特定位點與功能和功能聯絡起來的直接因果關係-行為改變。
來自丘腦的傳入神經攜帶來自許多身體感覺的資訊,例如血氧合、頸動脈壓力感受器、血壓、飢餓、疼痛和口渴。因此,相信島葉的功能是整合自主感覺輸入。這包括積極和消極的情緒,如恐懼、焦慮、悲傷、喜悅、憤怒和厭惡。
在健康受試者中,應用巴甫洛夫恐懼條件反射的實驗說明了腦島啟用;然而,目前尚不清楚腦島的作用主要是促進恐懼還是抑制恐懼。鑑於多模式感覺和邊緣傳入,島葉皮層被認為部分負責將情緒相關性分配給感覺刺激。
中風後腦島損傷的病例報告說明了這種解剖學考慮的一個重要但罕見的例子,其中患者味覺和味覺障礙。類似地,中風後疼痛分離也被記錄在案,其中患者認識到疼痛,但對刺激缺乏適當的負面反應。表明島葉皮層有助於處理同理心。傳統上,腦島與語音和語言處理有關。鉤狀束和下額枕葉束 (IFOF) 都延伸穿過島葉皮質下區域(圖 3)。鉤狀束從額下回延伸,在外側裂下方,終止於顳上回,而 IFOF 向後延伸至枕極(圖3)。出於這個原因,在優勢半球島葉膠質瘤手術中,皮層術中語言定位識別的是必不可少的。

圖3:大腦皮質外側面解剖圖。MRI彌散張量成像可顯示腹側和背側語言纖維束。額枕下束和鉤束均穿過島葉的皮質下區。ILF:下縱束;SLF:上縱束。圖自加州大學舊金山分校神經外科。
二、現代以前的島葉膠質瘤手術:切除範圍爭議不斷
過去20年,最大安全範圍下切除島葉膠質瘤的爭議不斷。這些努力始於根據影像檢查,對EOR和殘餘腫瘤體積的粗略估計,將患者分為“次全切除”組和“全切除”組。下一波研究隨後採用了基於病灶最大直徑的腫瘤體積橫斷面測量方法,這種方法可以實現提高採收率的體積測量。目前的研究還權衡了切除範圍對不同分子亞組的影響。島葉膠質瘤的切除範圍一直是一個有爭議的話題,早期儘管有證據支援最大安全切除,但很少嘗試切除島葉膠質瘤,因為醫生認為島葉手術風險太大。即便如此,2000~2009年間,不少研究均證實了島葉膠質瘤手術的可行性,記錄了技術考慮和併發症發生率,並編入島葉膠質瘤手術指南。
Yaşargil等首次提出翼點開顱經側裂入路切除島葉膠質瘤。報告240例以癲癇為最常見症狀的患者,95%術後僅出現輕微的神經功能缺損,生活能力獨立,均迴歸社會。這些結果表明可以考慮採用顯微外科手術治療島葉腫瘤。Ebeling與Kothbauer報道5例優勢半球額葉島蓋和島葉膠質瘤的患者,其中1例優勢半球島葉膠質瘤經側裂入路,在術中額葉島蓋運動區腦電監測下手術,由於術中內囊梗死繼發對側肢體偏癱而終止手術;該研究的術後併發症發生率為20%。基於他們的術後神經病學結果,作者主張僅在大的優勢半球島葉和島葉膠質瘤病例中進行活檢。

顯微外科技術的改進,皮質和皮質下術中語言和運動標測的更廣泛應用,以及更好的神經麻醉,都有助於隨後一系列報告患者結果的改善。Zentner和Vanaclocha分別報道30例和23例島葉膠質瘤的治療體會,手術全切率分別達16%和86%;63%患者術後出現短暫的神經功能缺損,隨訪8.5月時降至10%-22%。神經外科醫生透過細緻的解剖和最大化的結構保護,逐步得出手術經驗,建議擴大切開外側裂;採用術中喚醒麻醉,並記錄皮質和皮質下腦電活動,以分辨皮質運動傳導束與皮質下的內囊;在側裂上輕柔操作,避免大腦中動脈M2段和外側豆紋動脈閉塞。如此操作可使島葉膠質瘤術後3個月時的神經功能缺損下降至8%-10%。
三、現代島葉膠質瘤的外科治療
手術切除範圍與生存率的關係
Simon等人首次報道了WHO Ⅱ-Ⅳ級島葉膠質瘤的大宗病例分析,其中42%的病例切除程度達90%以上,51%病例達70-90%。預後不佳的預測因素包括WHO Ⅳ級、高齡,和術前KPS低分;預後良好的預測因素包括年齡小於40歲、低級別膠質瘤(WHO Ⅰ、Ⅱ、Ⅲ級)、涉及額葉島蓋的Yaşargil 5A/B型腫瘤以及切除程度大於90%。
Sanai等報告104例島葉膠質瘤的病例研究結果,以更好地瞭解切除範圍與生存率、惡性轉化和圍手術期發病率之間的關係。但當時尚無可以指導島葉膠質瘤解剖的臨床實用命名方式。於是,Berger-Sanai提出根據外側裂和室間孔的腫瘤分類方法(圖4)。從矢狀位看,島葉可在水平切面上被外側裂所在平面分開,又可在垂直切面上被沿著室間孔所在平面分開。島葉區域被這2個近似垂直的平面分為4個空間上相鄰的區域,前上、後上、後下、前下的四分之一分割槽分別被定義為I、Ⅱ、Ⅲ、Ⅳ區,腫瘤可累及一個或多個區域內。腫瘤累及範圍大於一個分割槽時,被表示如:I+Ⅳ區。累及所有(4個)區域的島葉腫瘤定義為“巨大型”。Berger-Sanai分型方法穩定可靠,有助於預測島葉膠質瘤的手術切除程度和術後併發症的發生。

圖4:Berger-Sanai根據膠質瘤位於外側裂上下以及室間孔前後分為四區。1區:腫瘤在外側裂上方,室間孔的前方;2區:腫瘤在外側裂上方,室間孔後方;3區:腫瘤在外側裂的下方,室間孔後方;4區:腫瘤在外側裂下方,室間孔前方。圖自舊金山加州大學神經外科。
最近的研究顯示,島葉膠質瘤的中位切除程度為81-86%,切除程度達90%以上的WHO Ⅱ級腫瘤患者5年生存率為100%,切除程度小於90%的患者5年生存率84%。不同切除程度的WHO Ⅲ、Ⅳ級島葉膠質瘤患者5年生存率由91%降至75%。腫瘤切除程度是WHO Ⅱ-Ⅳ級島葉膠質瘤總體生存期與無進展生存期的預測因素;切除程度低的患者容易發生惡變,腫瘤復發時應當及時手術。
手術入路:經外側裂入路為主
在過去的十年裡,島葉膠質瘤的手術方法被重新審視。患者被置於半側位,頭部與地板平行。對於病變位於門羅孔後2區或3區的患者,可將頭部向上旋轉15°,允許切除位於後島葉上方的功能性皮質結構下方的腫瘤(圖5)。然後,根據腫瘤是位於外側裂上方還是下方,將頭頂朝地板傾斜15°,還是朝天花板傾斜15°。追溯到yasargil的早期出版物,最常見的島葉手術入路是經外側裂入路。但87%的病例需要犧牲橫跨過外側裂的優勢引流靜脈。透過島蓋作皮質造瘻後的經皮質入路,也稱為“皮質視窗入路”,可暴露島葉皮質及大腦中動脈M2段的穿支。術者可以在保護橋靜脈的情況下,進行島葉腫瘤切除,尤其適用於涉及4個區的巨大島葉膠質瘤。
在島葉膠質瘤切除術的入路選擇及操作上,相比於傳統島葉腫瘤切除術,經側裂入路的島葉膠質瘤顯微切除術具有更好的臨床效果且更具安全性,其在臨床上的應用也更加廣泛。但島葉膠質瘤的切除手術仍屬於難度較大且具有挑戰性的手術,即便是現在的顯微外科技術也無法保證術後無併發症出現、無復發且效果良好的地步,這就要求我們對手術中各個環節中進一步分析與反思,如何更好的分辨、保護血管神經等精細組織,如何最大限度的發揮手術的效果並保護好正常的腦組織,以及尋找更加安全有效的治療方法等。
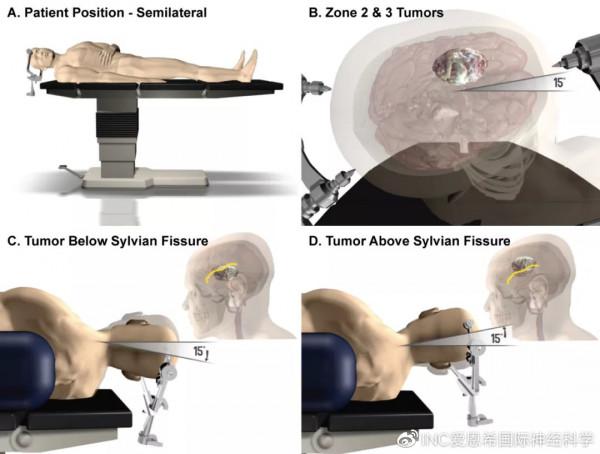
圖5:A:病人處於半側位。B:當接近位於門羅孔後的島葉膠質瘤(2區和3區)時,頭部向上15°,以最大限度地顯示功能皮質區下方。對於位於側裂下方的腫瘤,頭部的頂點向地板傾斜15度(C),而對於位於側裂上方的腫瘤,頭部的頂點向天花板傾斜15°(D)。圖自舊金山加州大學神經外科。
手術輔助技術
在切除島葉膠質瘤手術過程中我們可適當使用輔助技術和技巧,包括喚醒麻醉、神經導航、術中超聲、誘發電位以及皮質電刺激等。
1.功能輔助:在切除優勢半球島葉膠質瘤時可採用喚醒開顱,在術中可評價腦部各功能區;
2.定位輔助:術中腫瘤定位技術已進展到無框架立體定向和術中超聲,但是都不能代替細緻的手術分離技術 。

喚醒手術中,皮質及皮質下腦電圖監測可以顯著降低術後永久性神經功能缺損率(p=0.008)。除此之外,3D超聲導航、高分辨術中磁共振等輔助技術也可以降低術後併發症發生率。WHO Ⅲ-Ⅳ級膠質瘤的長期神經功能缺損發生率高於WHO Ⅱ級膠質瘤;短期神經功能缺損最常發生在1區膠質瘤以及涉及4個區域的巨大島葉膠質瘤。雖然即刻(手術後3天內)的短期併發症發生率為20%–26%,但3個月後,已發表報告的總體併發症發生率為3.2%–9%。7.8%–9%的患者出現新的運動神經功能缺損,3個月內緩解至1.6%。16.3%的患者術後立即出現語言障礙,3個月內緩解至0.8%。
手術效果評估:癲癇控制是不可忽略的重要因素之一
評估腦島膠質瘤患者時,功能結果、發病率和生活質量仍然是重要的考慮因素。島葉皮層接受廣泛的體感、邊緣和認知傳入輸入,然而患者在該區域手術後能夠體驗到高質量的生活和最低的發病率。癲癇控制是生活質量考慮的一個重要因素,特別是考慮到大多數患者都有癲癇發作。除了提供生存益處,最大限度地提高腦島膠質瘤的切除率,改善癲癇發作控制。此外,癲癇發作的復發往往預示著神經膠質瘤的復發和進展。與語言結果相關的生活質量也是一個重要的考慮因素。
儘管鉤束和IFOF延伸穿過島葉,上縱束和弓狀束在上後方向上延伸,術中喚醒皮質語言功能定位允許外科醫生識別該關鍵區域的語言位點(圖2)。腦島膠質瘤切除術中應用的語言任務包括圖片命名、文字閱讀、音節重複、聽覺命名和句法生成。大多數優勢半球低級別島葉膠質瘤患者的基線語言任務表現出色,這表明語言可塑性可能發揮了作用。無論是在出現時還是在切除後,嚴重的情緒、自主神經和個性問題導致的殘疾在腦島膠質瘤患者中很少觀察到。這就提出了這樣一個問題:是否丘腦和邊緣傳入途徑與島葉的功能相關,或者是否中樞神經系統的可塑性和功能重組有助於這些觀察結果。
島葉膠質瘤切除程度越大,控制術後癲癇發作的效果越好,術後癲癇再發作與腫瘤進展相關,再次切除腫瘤能進一步控制癲癇發作。
四、結論
島葉毗鄰重要功能區和血管,安全切除島葉膠質瘤充滿挑戰。在過去20年,透過神經外科醫生、麻醉師、神經科學家和解剖學家的共同努力,人們對大腦解剖和功能的理解上升到新的高度;微創外科技術的發展、喚醒麻醉、語言和運動區腦電監測技術應用,為改善患者預後提供可能,使高、低階島葉膠質瘤患者都可以考慮進行最大安全範圍下的切除。
參考資料:
1、Shawn L. Hervey-Jumper MD and Mitchel S. Berger MD. Insular glioma surgery: an evolution of thought and practice.J Neurosurg 130:9–16, 2019
2、馮江,段宇,李鍵,毛仁玲.經側裂入路的島葉膠質瘤顯微切除的療效觀察.神經損傷與功能重建·2020年9月·第15卷·第9期
【來源:中國網醫療頻道】