人都有生老病死,當內臟器官發生壞死或者病變時,往往需要透過移植新的健康器官來延長患者的壽命。其中,心臟移植是治療終末期心臟病的首選方式,能顯著提高患者的生活質量,。
據統計,2021年美國共進行了超過3800例心臟移植手術,數量上創下了歷史新高。國際心肺移植協會(ISHLT)的資料顯示,移植1年後,患者的平均存活率約為83%,5年後為72%,10年後則為55%,生活質量均明顯提升。
全球首例豬心臟在美移植成功
2022年1月7日,國際心肺移植領域又發生了一件大事:美國馬里蘭大學醫學院成功進行了一例豬心臟的移植手術,在全球尚屬首例。這臺手術長達7個小時,57歲的David Bennett成為了世界上第一個擁有豬心臟的病危患者。
據外媒報道,在手術進行3天后,病人的身體狀態表現良好。而在手術前,Bennett的身體狀況非常糟糕,心臟嚴重衰竭,心律失常,已經無法再進行人類的心臟移植,這次冒險移植豬心臟其實也是“破釜沉舟”之舉。
那麼,豬心臟真的能用來拯救心臟病患者嗎?現在下定論還為時尚早,在接下來的幾周將是關鍵期,醫生將對David Bennett的心肺功能進行密切監測。只有當病情穩定之後,豬心移植才算是真正看到了曙光。
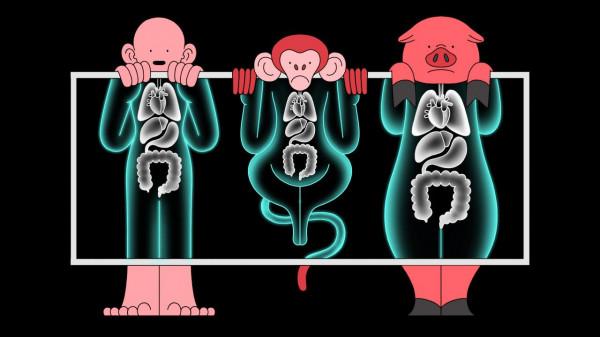
在歷史上,跨物種的心臟移植有不少案例,但最後都以失敗告終。上世紀60年代,醫學家曾嘗試把黑猩猩的腎臟轉移到人類患者體內,接受者起初表現正常,但最終因免疫排斥只活了9個月時間。
在1983年,一隻狒狒的心臟被移植到了一名病危的嬰兒體內,後來這名嬰兒僅存活了21天,原因同樣是免疫排斥。
被“修飾”的豬心:10處關鍵基因被修改
這例豬心臟移植與過去的跨物種移植有所不同,供體動物不再是靈長類,移植的這顆心臟還是基因編輯的產物,有10處關鍵基因被修改,其中就有包括與免疫識別相關的糖蛋白基因。
在2021年9月,紐約的研究人員就已經將轉基因的豬腎移植到了一名死者的體內,結果並未發現排異現象。這項實驗似乎讓人們看到了異體器官移植的新希望——當然,在此之前免不了要從個別案例的嘗試開始,以此不斷完善基因編輯和器官移植的水平。
說到這裡想必大家都已經明白,這顆轉基因的豬心做到了“對症下藥”,也就是從基因層面入手進行人為干預,減輕或者消除受體的免疫排斥。
我們知道,人體的免疫系統具有識別“自我”與“非我”的能力,外來的器官、病毒會被識別為抗原並引發免疫應答,這就是免疫排斥。如今,研究人員對豬的基因進行編輯,有4個關鍵基因被敲除或者滅活,關鍵的免疫識別資訊就會丟失;另外6個基因則插入了人類的基因,目的是增強豬的免疫器官對人體的耐受性。
如果這種方式被證明是可行的,那麼豬將成為最佳的外源心臟提供者,一是數量多,尺寸大小合適,二是成本低,培育週期短。再借助基因編輯這項強有力的工具以及免疫抑制藥物,豬心臟移植的可行性將大大提高,為未來大規模的醫學應用奠定了重要基礎。
心臟移植術後的風險有多大?
在手術完成後,患者有可能會出現感染症狀,這也是臨床上最常見的併發症。據統計,手術後一年內,由感染引發的病死率將近20%,是心臟移植患者最主要的致死因素。
- 手術後第1個月,大部分感染都是和手術相關的細菌性感染,比如導管手術、機械通氣相關的感染;
- 手術後第2個月,患者容易發生機會性感染,如弓形蟲病、查加斯病、麴黴病、CMV感染等;
- 手術後6個月開始,免疫抑制劑的劑量逐漸減少,這一時期的獲得性感染相對常見。
另外很多醫學中心經研究發現,心臟移植後感染的部位主要在肺部,這是因為應用免疫抑制劑後,患者自身的免疫力會變低,抵抗力下降,容易發生原蟲、細菌、真菌等感染,其中病死率最高的是真菌感染。
除了感染,患者的排斥反應也是一個難題,而且持續時間更長。基因編輯的豬心臟是否有潛在排斥風險,目前還不好確定,如果後期出現了排斥反應,後果也可能很嚴重。
以急性細胞性排斥反應為例,最早可出現在手術後一週內,最晚可在幾年後才出現,潛伏時間不確定。在發生免疫反應期間,患者可能沒有明顯症狀,需要在術後1年內定期進行心肌活檢。
根據國際心肺移植協會修訂的標準,心肌活檢的評分分為四個不同的等級,分別是:
- 0級:沒有免疫排斥反應。
- 1R級:有間質性或血管周浸潤,存在1處心肌細胞的損害。
- 2R級:中度排斥反應,存在2處以上的心肌細胞損害。
- 3R級:重度排斥反應,存在多處心肌細胞損害,並呈瀰漫性浸潤;可能伴有水腫、出血、血管炎等症狀。
總之,移植手術後的風險不容低估,持續觀察是降低風險的最好措施。經過術後恢復,患者的健康狀況比手術之前可大大改善,甚至有半數以上的群體可重返工作單位。相信隨著移植技術的成熟,越來越多的心臟病患者有望享受到現代醫學的福利。