*僅供醫學專業人士閱讀參考
迄今為止,免疫檢查點抑制劑(ICI)已經顯著改善了晚期肺鱗狀細胞癌(LUSC)的治療療效。多項研究表明,免疫檢查點抑制劑聯合化療可顯著延長晚期肺鱗癌患者的無進展生存期(PFS)和總生存期(OS)。然而這種聯合治療方案的預測性生物標誌物在很大程度上仍是未知的。腫瘤突變負荷(Tumor mutation burden, TMB)是ICI單藥治療各種實體腫瘤療效的候選生物標誌物,但相當大比例的患者無法提供足夠的組織用於下一代測序(NGS)計算TMB。由於利用外周血迴圈腫瘤DNA (ctDNA)計算的血液腫瘤突變負荷 (Blood tumor mutation burden, bTMB),具有簡便性、無創性,並且能矯正腫瘤異質性或低腫瘤佔比帶來的抽樣偏差,以及實現對早期治療進行動態監測的優勢,從而成為一種更有潛力的方法。
近日,恆瑞醫藥聯合上海市肺科醫院周彩存教授團隊牽頭合作的全國多中心研究成果發表於“Molecular Cancer”(IF:27.401)。文章題為“On-treatment blood TMB as predictors for camrelizumab plus chemotherapy in advanced lung squamous cell carcinoma: biomarker analysis of a phase III trial”。作為唯一參與該研究的腫瘤精準診斷企業,臻和科技承擔了該研究的基因測序與相關分析等工作。
主要研究內容
恆瑞醫藥、上海市肺科醫院周彩存教授團隊合作開展的CameL-sq研究(NCT03668496)是一項隨機、雙盲、多中心三期臨床試驗,以評估卡瑞利珠單抗聯合化療在晚期肺鱗癌一線治療中的有效性和安全性。研究表明,相比化療,卡瑞利珠單抗聯合化療作為晚期肺鱗癌患者一線治療的方案,顯著提高了患者的PFS和OS。同時此研究還創新地使用了治療期bTMB及動態bTMB(∆bTMB=治療期bTMB-治療前bTMB)作為檢測指標。研究結果表明,bTMB和∆bTMB均可以有效預測晚期肺鱗癌患者卡瑞利珠單抗聯合化療的療效。
關鍵結論
治療期bTMB及其動態∆bTMB可作為晚期LUSC患者卡瑞利珠單抗(Camrelizumab)聯合化療的預測性生物標誌物。
研究設計
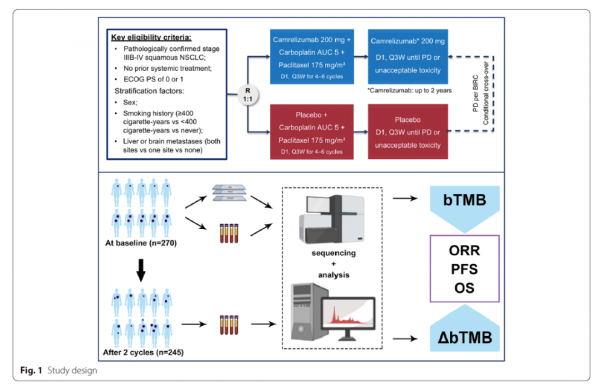
此研究共招募了病理確認為IIIB-IV期,且之前未進行過全身治療,也無EGFR敏感突變或者ALK相關的基因組變異的389名肺鱗癌患者,並隨機分組進行卡瑞利珠單抗聯合化療(n=193)或安慰劑加化療(n=196)的治療。其中共有270名患者收集到基線時的腫瘤組織樣本和基線血(卡瑞利珠單抗聯合化療n=134,化療n=136)樣本以及245例治療期外周血樣本,並納入此生物標誌物研究分析,以探討治療前tTMB、治療前bTMB、治療期bTMB 和動態∆bTMB對晚期肺鱗癌患者卡瑞利珠單抗聯合化療的療效預測價值,研究設計如圖1所示。
研究結果
1.治療期bTMB是預測免疫治療聯合化療療效和預後的有效生物標誌物
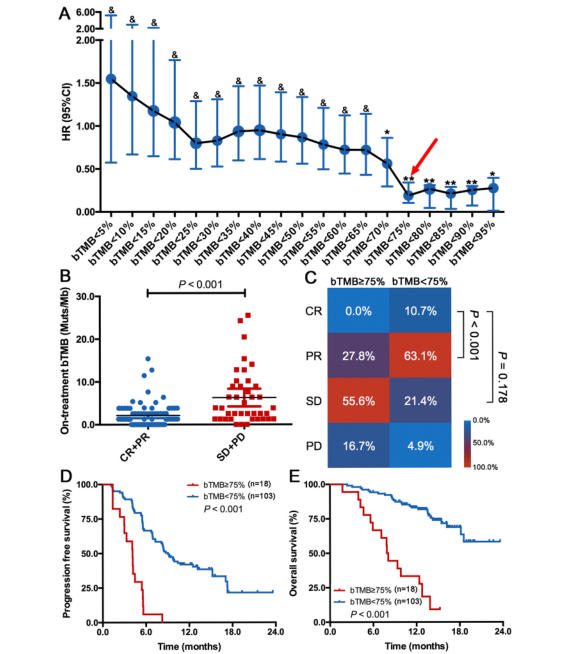
為了更好地體現bTMB預測預後的價值,研究將bTMB值≥75%的組定義為高bTMB組,bTMB值<75%的組定義為低bTMB組(圖2A)。在卡瑞利珠單抗聯合化療組中,完全緩解(CR)+部分緩解(PR)患者的治療期bTMB顯著低於疾病穩定(SD)+疾病進展(PD)患者(P < 0.001,圖2B)。同時,治療期bTMB低的患者,其ORR顯著高於治療期bTMB高的患者(73.8% vs 27.8%,P < 0.001,圖2C),其PFS (中位數 9.1 vs 4.1 月;HR = 0.190,P < 0.001;圖2D)和OS(中位數 未達到 vs 8.0 月;HR = 0.144,P < 0.001;圖2E)也顯著延長。且經過臨床資訊/治療前tTMB和治療前bTMB的多因素矯正後,治療期bTMB仍然與PFS(adjusted HR = 0.189;95%,0.101-0.358;P < 0.001)和OS(adjusted HR = 0.152;95% CI,0.075-0.308;P < 0.001)獨立相關。然而在化療組,治療期bTMB與ORR和PFS均無相關性。以上結果表明治療前tTMB和bTMB不能很好地預測卡瑞利珠單抗聯合化療的療效和預後,而治療期的bTMB則可以很好地預測卡瑞利珠單抗聯合化療的療效和預後。
2.動態bTMB可作為預測免疫治療聯合化療療效和預後的補充生物標誌物
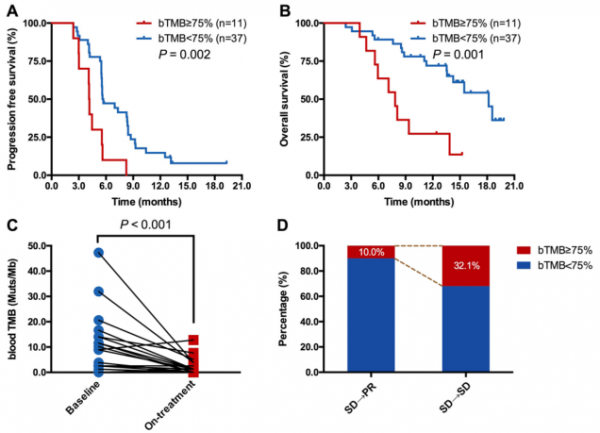
進一步研究表明,動態bTMB(∆bTMB=治療期bTMB-治療前bTMB)也可預測免疫治療聯合化療的療效和預後。bTMB增加或不變的患者(∆bTMB ≥0),其PFS(中位數,4.5個月vs 8.5個月;HR= 2.545,P < 0.001;圖3A)和OS(中位數,9.0個月vs未達到;HR = 4.199,P = 0.201;圖3B)均明顯縮短。儘管∆bTMB與治療期bTMB呈顯著相關性(rSpearman= 0.849,p < 0.001,圖3D),但將∆bTMB與治療期bTMB聯合進行生存分析時發現它們可以互補地,非重複地預測療效。具體為,治療期bTMB低且∆bTMB <0的患者PFS和OS最長,治療期bTMB低且∆bTMB <0或∆bTMB≥0的患者PFS和OS居中,治療期bTMB高且∆bTMB≥0的患者PFS和OS最差(P < 0.001;圖3E、F)。
3.治療期bTMB可從初始放療SD的患者中鑑定出能長期獲益於免疫治療的患者
目前,從初始放療SD患者中區分免疫治療長期獲益的人群仍是一個挑戰。考慮到治療期bTMB和腫瘤負荷之間的相關性,此研究又進一步探索了治療期bTMB能否區分最初放療SD但最終獲益於免疫治療的人群。對卡瑞利珠單抗聯合化療組中48例初始放療SD患者進行分析發現,治療期bTMB高的患者其PFS(中位數,4.1 vs 5.6個月;HR = 2.861,P = 0.002;圖4A)和OS(中位數,7.8 vs 18.2個月;HR = 3.546,P = 0.001;圖4B)均顯著更低。而對於20例初始放療SD,但最佳評效為PR的患者,其治療期bTMB明顯低於其對應的基線bTMB (P < 0.001;圖4 C),治療期bTMB≥75%的比例也低於最佳評效為SD的人群(10.0% vs 32.1%;圖4 D)。
臨床意義
本研究基於bTMB及∆bTMB的分析資料,首次報道了治療期bTMB與卡瑞利珠單抗聯合化療的ORR/PFS/OS的顯著相關性,以及動態∆bTMB對此的補充和非重複性預測效果。此外,治療期bTMB還能從放療SD的患者中,鑑定出可在卡瑞利珠單抗聯合化療治療中長期獲益的人群。綜上所述,對於晚期肺鱗癌患者,治療期bTMB可作為預測免疫治療療效和預後的有效分子標誌物。
研究原標題
On-treatment blood TMB as predictors for camrelizumab plus chemotherapy in advanced lung squamous cell carcinoma:biomarker analysis of a phase III tria .Jiang et al. Molecular Cancer (2022) 21:4;https://doi.org/10.1186/s12943-021-01479-4
*此文僅用於向醫學人士提供科學資訊,不代表本平臺觀點