恆瑞醫藥是一家從事藥品研發、生產還有銷售的製藥企業,是中國知名的抗腫瘤藥、手術麻醉類用藥、特色輸液、造影劑等的主要供應商,多次榮登《全球製藥企業50強》排行榜,同時也連續幾年佔據《中國藥品研發實力排行榜》的榜首位置。2021年卻是恆瑞醫藥跌落神壇的一年,股價一瀉千里,連跌八個月上演“腰斬”慘劇。對於投資恆瑞醫藥的股民朋友來說
們,你是否瞭解恆瑞醫藥的“前世今生”呢?
一、藥中茅臺的崛起之路
恆瑞醫藥創立於1970年,起初只是生產紅藥水、紫藥水以及為大製藥廠做灌裝作業的工廠,這種沒有技術含量的業務競爭激烈,利潤非常低,工廠一直都在勉強支撐著。一直到了1990年,當時32歲的孫飄揚升任廠長,他意識到沒有技術,你的命運就掌握在別人手裡。因此,他一上任後就尋找可以仿製的藥品。這裡需要解釋一下:仿製藥就是模仿專利到期的創新藥而研製的藥品,創新藥就是自家研發擁有20年專利保護期的新藥。
憑著敏銳的市場嗅覺,經過市場調查後,孫飄揚選擇了當時市場銷售量非常高的一種抗癌藥VP16的針劑,把原料製成膠囊銷售,因為服用膠囊比打針方便,所以產品一上市就大賣。1992年他買下了國內研發的一款抗癌新藥的專利權,這個專利權只是製藥工藝,買回來過後還要進行臨床測試、生產和銷售,在當時對這個小小的製藥廠來說是一場生死存亡的豪賭,幸運的是產品一上市就讓藥廠一炮而紅。
接連兩個產品的成功,讓孫飄揚更加確定了藥品研發的道路是正確的。1993年之前,中國並沒有對藥品實行專利保護,所以在研發生產仿製藥的過程中,難免還是會碰到訴訟的問題。恆瑞甚至和一家法國製藥廠打了長達七年的官司,雖然最後官司還是打贏了,但是也讓孫飄揚深刻體會到,擁有屬於自己的智慧財產權的重要性,加上國家政策的鼓勵,恆瑞開始投入大量的資金建設研發中心,招聘大量的科學家,開啟了研發創新藥的道路。而帶領著恆瑞從仿製藥起家,再以創新藥奠定龍頭地位的孫飄揚更被稱為“中國藥神”。
二、由“仿製”轉型為“創新”打造的護城河
成功研發創新藥肯定能賺錢,這是大家都知道的常識,但對很多藥廠來說,問題不是不想研發,而是研發不起。根據一項由英國倫敦經濟學院分析的資料顯示,2009年-2018年期間,將一種新藥推向市場的平均成本為13億美元,腫瘤還有免疫調節藥物的研發成本最高,平均45億美元。
這筆資金包括從實驗室開始研發需要的支出到經過3期臨床實驗的同期研發損失費,所以單單是資金門檻就把大多數的藥企擋在門外了。一個創新藥從研發成功經歷了臨床實驗再到批准上市,至少都需要8到10年的時間,甚至更長的時間,超長的研發週期成為了第二個門檻。研究成功了,根據中國的專利條規,從申請專利保護開始到結束,在20年的時間裡其他企業不能仿製。但是藥品必須申請了專利保護才能夠進行臨床研究,所以專利期不是從上市開始計算,而是研發過程也計算在內。如果研發和臨床實驗用了10年,藥品獨家銷售的時間也只有10年的時間,加上推廣還有行銷時間又用去幾年,真正的黃金銷售期可能也只剩下5-6年的時間。雖然目前中國政府已經透過新的專利法給創新藥專利權最長五年的補償期,但是如果一家藥企想要在短短的專利保護期限內,透過壟斷銷售來收回研發的支出和獲利,其實還是有一定的難度。
那麼,恆瑞是怎麼突破資金高、研發時間長和專利保護期的問題呢?
90年代的中國,是缺醫少藥的年代,這個時期誰能夠快速地開發出滿足市場需求的產品,誰就能夠賺到最多錢,恆瑞就在這個時期透過仿製需求大的產品,迅速累積了豐厚的資本。隨著競爭加劇,重心開始轉移到研發首仿藥。首仿藥就是“首款非專利藥”,藥品監督機構批准的第一個在國內銷售的仿製藥。在美國,經過FDA批准的首仿藥,能夠擁有180天的市場獨佔期,在中國新的鼓勵政策之下,對挑戰專利成功的化學仿製藥品,市場獨佔期是12個月。在這一年內,監管部門不會批准同樣品種仿製藥上市。而透過首仿藥開啟市場的恆瑞,在這個階段又累積了大量的經驗和資金,為創新藥打下非常堅固的基礎。在瞭解一家制藥企業的時候,不能只看現在的收入,必須瞭解公司大賣的產品專利什麼時候到期,更重要的是,你必須知道公司其他研發中的藥品效率還有周期,這是判斷企業未來成長性的重要根據。任何藥品的專利一旦到期,銷售額就會面臨斷崖式的下跌,如果沒有其他專利藥品來接棒,公司的收入就會大大地影響。
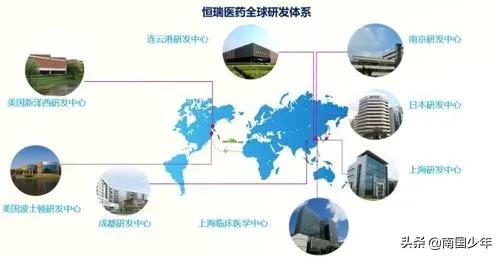
恆瑞經過多年的發展,已經擁有4000多人的研發團隊,在美國、歐洲、日本和中國多個地點都設立了研發中心,還有臨床醫學部,每年投入銷售額至少10%以上的研發資金。2021年恆瑞的研發資金創歷史新高,前三季度共投入了41.42億元,佔總營收的20.5%。公司在創新藥的開發上,已經形成了“上市一批、臨床一批、開發一批”的發展迴圈,而且排期緊密,基本上是每年都有創新藥申請臨床實驗,每1到2年都會有創新藥上市。恆瑞從資金、時間、人才技術,還有政策方面都已經建立了非常強大的護城河。
三、優先審評——甩開對手加速器
2016年2月26日,國家食品藥品監督管理總局落實了優先審評制度,來解決藥品審批積壓的問題,以及鼓勵更多創新藥的研發、具有臨床價值的創新藥、抗腫瘤或者市場短缺的藥品等,這方面的藥品都被納入優先審評範圍的藥品。對於納入優先審批程式的藥品,上市許可申請的審評時限由標準時限200個工作日縮短到130個工作日。如果已經在國外上市了,國內上市的審批期限最快可以縮短到70個工作日。至今,恆瑞透過這條高速公路上市的創新藥品就有10種,這還不包括其他仿製藥的申請。
根據國家藥品監督管理局藥品審評中心(CDE)公開的資訊顯示,2021年恆瑞醫藥受理的藥品審評就高達171款,2022年目前有2款藥品審評受理。截止2021年恆瑞醫藥獲得CDE臨床試驗默示許可就高達343項,其中就有26款是海內外都還未上市的新藥。
恆瑞醫藥研發藥品的數量還有速度,加上優先審評的政策,會大大降低時間成本,加速公司藥品上市和獲利的步伐。
四、高價藥“以量換價”進醫保
一款藥好不好賣,藥效很重要,但是能賣多少數量,除了藥效以外,在不在醫保的藥品目錄內也非常重要。中國的醫保基金是醫藥市場最大的支付主體,進入醫保目錄的藥品,代表醫院的用藥意願加大,理論上會帶動藥品的銷售量增加。因為在現行的醫療體制下,中國公立醫院佔據了全國藥品市場七成的份額,雖然進入醫保目錄醫院不一定就會下單大量購買,但是如果不在醫保目錄,想要把藥品賣給醫院就更加難。因此,國內外的藥企打破頭都想要進入醫保目錄。
就以PD-1來說,這是透過調節人體自身的免疫細胞來治療腫瘤的抑制劑,同一款PD-1產品,可以用來治療十多種癌症,因此被稱為治療腫瘤的神藥。在中國,恆瑞醫藥、百濟神州、信達生物、君實生物是最先成功研發PD-1的4家公司。你可能會覺得,既然這是腫瘤神藥就不用擔心沒有人要,但是在面對強烈的競爭之下,能夠賣多少更為重要。恆瑞就曾經表示,因為PD-1卡瑞利珠單抗錯過了2019年的醫保目錄,進醫院的工作非常困難,在國內500家醫院中的滲透率只有8.8%,只能在醫院外銷售,而信達生物在2019年的醫保談判中,主動降價64%,成功進入醫保目錄,銷售業績顯示2020年全年PD-1的銷售額超過22億元,2019年同期只有10億元,翻了不止一倍。這也是為什麼恆瑞在2020年醫保談判的時候,寧願降價85%也要進入醫保目錄。
談到藥效,一款PD-1產品獲批的適應症越多,表示市場越大,數量也會越來越多,代表在醫院的滲透率就更高。
適應症就是藥物適合使用的病症範圍,比如說治療某種癌症,四款PD-1產品都可以用,如果其中一款的適應症比較多,臨床使用的機率就會高一點。恆瑞成功進入醫保的PD-1產品是國產PD-1產品中適應症最多的,截止2021年12月,恆瑞PD-1獲批的適應症達到了8項,覆蓋四種癌症,用於晚期肺癌、肝癌、食管癌和霍奇金淋巴瘤的治療。2020年,即使在疫情的影響之下,國產PD-1的銷售額合計也超過了90億元。根據弗羅斯特沙利文預計,2025年中國PD-1市場規模將達到917億元,未來幾年會迎來10倍的增長空間。
因此,我們也相信,恆瑞即使面臨仿製藥集採業績快速下滑的壓力,未來在創新藥的領域收入將會快速增長,成為公司新的利潤增長點。
五、龐大銷售團隊和創新走向海外
醫保目錄是進入醫院的入門票,能不能夠獲得爆發性的銷售額,考驗的還是各家的銷售能力。雖然孫飄揚重掌恆瑞以來,對公司團隊進行了大刀闊斧的改革,銷售團隊從最高峰的14600多人一路大幅裁員,但多年來恆瑞強大的銷售網路已經滲透到各大城市的醫院,也覆蓋了鄉鎮,即便恆瑞超高的銷售費用一直被投資者詬病,但龐大的銷售團隊和密集的銷售網是提高銷售能力的一個關鍵。
除了國內的市場,恆瑞現在也加大國際化佈局的腳步,加入到國際競爭的行列中。目前恆瑞的策略就是“引進來,走出去”,引進國外先進創新藥品還有技術的同時,把自己的科研成果推出海外賺外國人的錢。目前恆瑞在美國、歐洲、日本都設立了海外研究中心,負責追蹤最新技術、引進海外專案、以及向相關部門申報批文等工作。2011年至今,恆瑞已有多款仿製藥產品在海外上市,而目前恆瑞正加大在海外建立臨床中心,把國內研發的產品送到國外做臨床實驗,提高藥品在海外上市的成功率。英國醫院資訊IDERA Pharma公司釋出了2020年醫院創新指數還有醫藥發明指數的排行榜,恆瑞醫藥是唯一上榜的中國製藥企業,全球排名第13位和第15位。IDERA Pharma是一家協助藥企將產品從開發階段推入市場的諮詢公司,這兩份指數評估的是藥企在研發管線的廣度還有創新性,考量的是如果把同一份早期臨床階段的資料給兩家公司,誰更能夠成功地創造出具有影響力的新藥。恆瑞能上榜,更進一步地證實了公司的實力還有成長的潛能。
六、近乎完美的財務表現
恆瑞無論是從盈利、財務狀況、資產、股息或者增長五個維度來看,都是一家近乎完美的公司。公司的毛利率多年來都在80%以上,營收方面的五年複合年均增長率有25.6%,淨利潤有28.8%,多年來都是0商譽,短期還有長期貸款也是0,流動比率6.52倍,現金比率4倍,公司的自由現金流年年增加。我們是從以往的資料來分析,雖然2021年恆瑞出現了“滑鐵盧”,但這是公司處於轉型的一個階段,不妨礙我們判斷它以往以來取得的成績。這裡只想提一點:剛才提到的四家PD-1創新藥的企業,目前除了恆瑞以外,其他三家都還沒有盈利,其他的就請小夥伴們自己去思考了!
七、風險與利益共擔
即使恆瑞醫藥擁有雄厚的營收能力,必然也需要承擔一定的風險,沒有一家企業是零風險的,那麼恆瑞會面臨哪些風險呢?
創新藥品從研發到上市需要平均至少10年以上的時間,資金高、時間長、還不擔保會成功,出了實驗室,還有可能在臨床研究上宣告失敗,資金還有時間上的損失就不小了,藥品終於上市了,也有可能面臨銷售額比預期來得更低,或者因為其他市場的因素導致降價幅度超過預期的情況。
在仿製藥方面競爭對手之間比的是市場資訊的蒐集能力,還有研發的實力和速度,誰能夠提前做好佈局還有規劃率先研發成功,誰就能夠佔領首發的優勢,另外,研製仿製藥也是挑戰專利的一種行為,所以隨時可能收到來自專利廠商的訴訟,訴訟費用高、時間長,搞不好還高過研發成本或者利潤,所以這是仿製藥需要考量的風險。
一款創新藥上市後,還需要一段時間的推廣,讓更多醫生了解和接受,才會進入銷售的黃金期。恆瑞的好幾款創新藥都是過去幾年上市的,目前已經慢慢進入創新藥的收穫期了,雖然目前是恆瑞醫藥最艱難的時刻,“山重水複疑無路,柳暗花明又一村。” 恆瑞醫藥未來依然可期!