近日,山東大學齊魯醫院急診科陳玉國教授和徐峰教授團隊在JCI Insight雜誌(JCR 1區,IF=8.315)上發表題為“Aldehyde dehydrogenase 2 protects against acute kidney injury by regulating autophagy via Beclin-1 pathway”的研究論文,闡明瞭乙醛脫氫酶2(ALDH2)改善造影劑和缺血再灌注誘發急性腎損傷的機制,併為急性腎損傷的治療提供了新的理論依據和分子靶點。山東大學齊魯醫院為文章第一作者和通訊作者單位,陳玉國和徐峰為共同通訊作者,急診科徐同輝、王甲莉,碩士研究生郭家麟、魏茂增為共同第一作者。
急性腎損傷(AKI)是影響全球數百萬患者的重要疾病,常發生於腎臟缺血、心血管疾病、膿毒症、重大手術、造影劑暴露以及藥物治療的患者,其中,血管造影劑誘發的急性腎損傷(CI-AKI)在醫院獲得性急性腎損傷病因中位居第三。隨著接受心臟導管手術以及血管增強CT患者的增多,血管造影劑誘發的急性腎損傷對病人健康和公共醫療資源的影響正逐年增加。儘管指南已提出相關預防措施,但在最近的數項大規模隨機對照試驗中並未觀察到明顯益處。因此,探究血管造影劑誘發的急性腎損傷的發病機制並尋找新的治療靶點具有重要意義。
乙醛脫氫酶2是一種位於線粒體基質中的變構四聚酶,在多臟器中均有表達,主要參與催化毒性醛類等的代謝。大約40%的東亞人群(佔全球8%的人口)攜帶ALDH2 E504K突變,導致毒性醛代謝異常,增加冠心病、消化系統癌症和阿爾茨海默病等疾病的風險,而增強乙醛脫氫酶2活性可在心、肺等臟器損傷中發揮保護作用。乙醛脫氫酶2在急性腎損傷中有沒有作用、起到什麼作用及其機制是什麼,目前尚不明確。
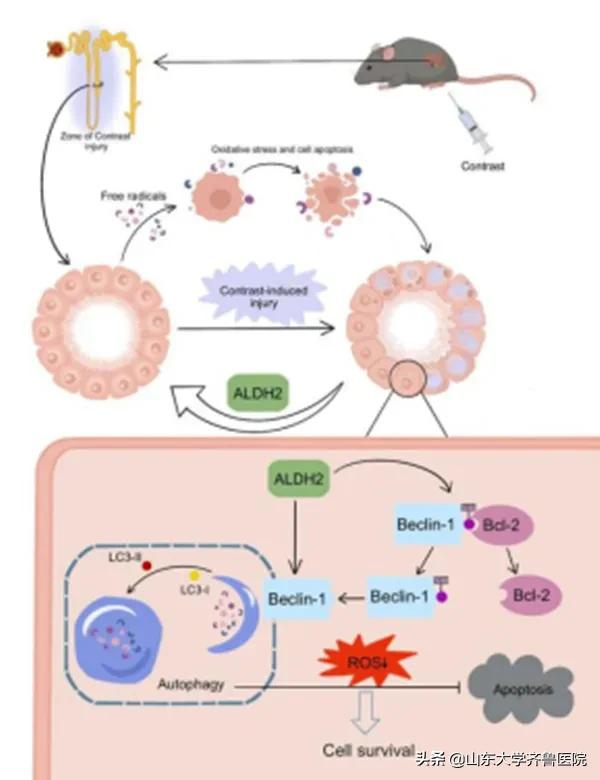
該課題透過體內體外實驗,明確了乙醛脫氫酶2缺乏可增加活性氧(ROS)的產生並誘導氧化損傷,從而導致腎小管上皮細胞(RTECs)凋亡數量增加和管狀結構損傷加重,加劇造影劑誘導的腎損傷;而啟用乙醛脫氫酶2能顯著改善造影劑腎損傷。血管造影劑誘發的急性腎損傷模型小鼠的腎臟皮質轉錄組測序結果,揭示了乙醛脫氫酶2調控Beclin-1訊號通路啟用自噬改善血管造影劑誘發的急性腎損傷的機制。為了驗證這一結論,研究人員運用自噬抑制劑3-甲基腺嘌呤(3-MA),Beclin-1的小干擾和自噬雙色熒光腺病毒等方法,在體內外實驗證實了乙醛脫氫酶2上調腎小管上皮細胞中Beclin-1的表達,減少Beclin-1在BH3結構域與Bcl-2之間的結合,削弱Bcl-2對Beclin-1介導自噬的抑制功能,清除腎小管上皮細胞中累積的活性氧。此外,該團隊在腎臟缺血再灌注損傷(IRI)模型中,再次驗證了乙醛脫氫酶2調控自噬改善急性腎損傷的作用和機制。
在研究中,該團隊發現了乙醛脫氫酶2新的臟器保護作用,證實了乙醛脫氫酶2調控自噬,改善血管造影劑誘發的急性腎損傷和缺血再灌注腎損傷的機制,為急性腎損傷的治療提供了新的理論依據和分子靶點。