*僅供醫學專業人士閱讀參考
精準治療,檢測先行!一文教你讀懂基因檢查報告中的MET 14號外顯子跳躍突變。
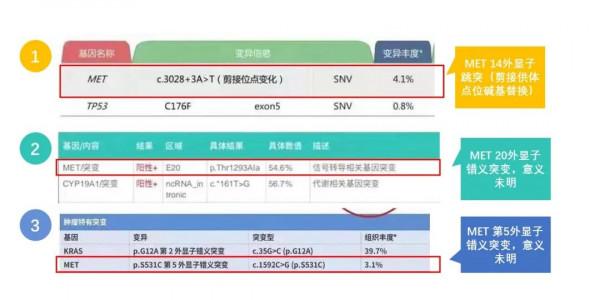
MET TKI在國內外相繼獲批治療MET 14外顯子跳躍突變的晚期NSCLC,MET 14號外顯子跳躍突變進入精準治療時代。但是報告怎麼看,卻讓人很頭大!醫生們臨床上看到的檢測報告可能是這樣的:
到底以上哪個報告是MET 14號外顯子跳躍突變呢?本文教你一文讀懂MET檢測報告!
別急,看檢測報告前,先了解下面資訊做足準備。
報告的突變型怎理解?
開頭提到的MET變異型別,如c. 3028+3 A>T, p.S531C,醫生們經常會有疑問,這些要怎麼理解。其實,上面的這些變異都是根據HGVS(human genome variation society,人類基因組變異協會)標準命名規則表示的。一般包括參考資訊來源[如“c.”代表編碼DNA參考序列,“p.”代表蛋白(氨基酸)參考序列],位置編號(一般根據參考序列資訊,如c. 3028就是編碼序列的第3028個核苷酸)以及具體發生的改變(DNA 層面就是核苷酸的變化,包括>點突變、ins插入、del刪失等;蛋白層面的改變,氨基酸的變化)。
一般DNA變異命名參考都是編碼DNA序列,但是一些變異可會發生在非編碼區,如本文介紹的MET 14號外顯子跳躍突變。對於這些變異位點,沒有對應的位置編號,需要用附近編碼區的位置編號作為定位參考,上游使用“-”,下游使用“+”來進行表示。
現在再看看開始提到的幾個變異型。
c. 3028+3 A>T,在第3028號編碼核苷酸下游第三個非編碼的核苷酸發生了點突變,從A變成T。p.S531C,蛋白第531號氨基酸從S(絲氨酸)變成了C(半胱氨酸)。
注:突變會因生信分析時參考轉錄本不同而比對出不同的結果,會導致位置編號不同。如參考MET基因NM_000245.3轉錄本,突變為c. 3028+3 A>T;但如果參考MET NM_001127500.3轉錄本,同一突變則表示為c. 3082+3 A>T。下列介紹均基於NM_000245.3轉錄本資訊。
什麼是MET 14號外顯子跳躍突變?
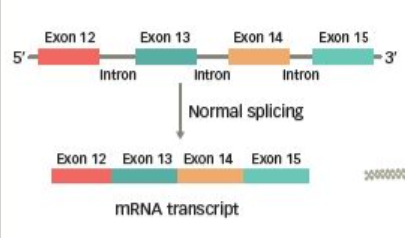
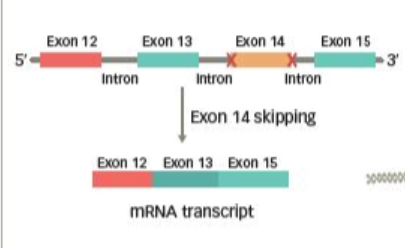
MET 14號外顯子跳躍突變是指MET mRNA中14號外顯子丟失的現象,通常由RNA剪接異常造成。那什麼又是RNA剪接?
DNA是由非編碼的內含子區域和編碼的外顯子區域交錯組成。在由DNA轉錄到mRNA再翻譯為蛋白的過程中,需要將內含子剪下除去,並將外顯子有序連結形成一個連續的RNA(mRNA)分子。這就是RNA剪接過程(如圖)。
RNA剪接過程需要識別內含子上的多個區域。這些區域如果遭受到破壞或受影響,都可能導致RNA剪下異常。MET 14號外顯子周圍內含子的剪下相關區域發生突變時,導致外顯子14被錯誤剪下而丟失,即所謂“MET 14號外顯子跳躍突變”。
MET 14號外顯子跳躍突變會導致其編碼的蛋白近膜結構域(JM)缺失。該結構中的Y1003殘基是E3泛素連線酶CBL的結合位點,CBL結合Y1003殘基將介導MET泛素化,導致MET蛋白降解,是MET蛋白主要的負調控機制。當該區域缺失時,會導致MET受體泛素化降低,MET蛋白降解降低,最終導致下游訊號通路的持續啟用,從而導致腫瘤發生(如圖)。
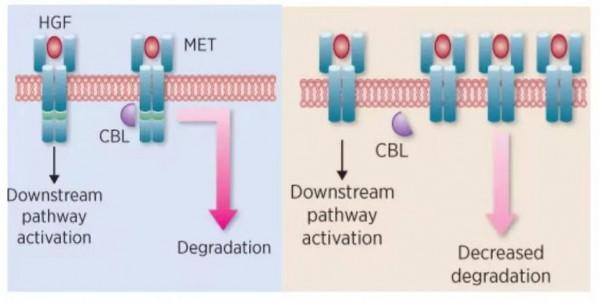
圖4 MET ex14 RNA正常剪接的生物學結果(左)和異常剪下的生物學結果(右)[1]
導致MET 外顯子跳躍的突變區域有哪些?
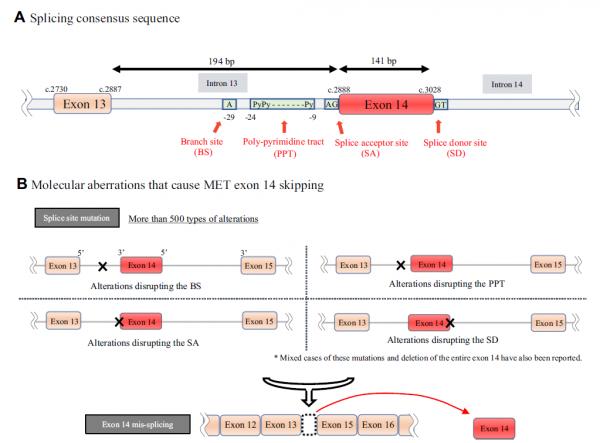
上文提到發生在內含子區域的突變可能會導致外顯子跳躍,那MET 14號外顯子跳躍突變的區域有哪些?下圖詳細介紹了MET 14號外顯子跳躍突變的區域,主要包括14號內含子的5'端剪接供體位點(splice donor, SD site)和13號內含子3'剪接受體位點(splice acceptor, SA site)、分支位點(Branch site, BS)和多嘧啶位點(Poly-pyrimidine tract,PPT)等。
據累及的功能位點的差異可以分為兩大類:
一類是基因變異累及邊緣經典剪接區,即位於內含子邊緣SA和SD區域,如圖5A所示。經典剪接區上發生的點突變或插入缺失(indel)可導致剪下子無法識別剪接受體或供體位點,從而導致MET外顯子14的異常剪下。
SA site
邊緣1-2bp位置發生的點突變有c.2888-1,c.2888-2可直接判定為MET 14號外顯子跳躍突變,例如c.2888-1G>A等。除點突變外,累及該區域的插入/缺失也可導致MET 14號外顯子跳躍突變,例如c.2888-7_c.2920del。發生在該區域的突變型別以插入缺失較為多見。
SD site
邊緣1-2bp位置發生的點突變有c.3028+1,c.3028+2可直接判定為MET 14號外顯子跳躍突變,例如c.3028+1G>A,c.3028+1G>T,c.3028+2T>A等。除經典剪接序列外,供體位點c.3028的鹼基替換(例如:c.3028G>A,對應氨基酸改變為p.D1010N;c.3028G>C對應氨基酸改變為p.D1010H等),c.3028+3的鹼基替換也曾被報道為MET 14號外顯子跳躍突變[2][3]。同樣累及該區域的插入/缺失也可導致MET 14號外顯子跳躍突變,例如c.3018_ c.3028+8del。發生在該區域的突變型別以點突變較為多見。
另一類是基因變異累及內含子上的BS和PPT區域,多為發生在緊鄰剪接受體位點上游約25bp的內含子非編碼區的鹼基替換和插入缺失突變,如上圖5A所示。此類變異可能會導致RNA無法完成正常的剪接過程,故而通常會被認可導致MET 14號外顯子跳躍突變。這類MET 14號外顯子跳躍突變的判定主要來自文獻報道[4]。
BS位點
上的A鹼基與RNA剪接過程中的親核攻擊有關,其核苷酸位置在如圖5A所示的c.2888-29(即內含子-29位點)。若缺失的部分包含該區域,則可能導致MET 14號外顯子跳躍突變。
PPT位點
是RNA剪接過程中剪接因子相關蛋白與分支位點結合蛋白(SF1)相互作用的區域。其核苷酸位置在如圖5A所示的c.2888-24_2888-9(即內含子-24_-9區域)。若缺失的部分涉及該區域,也可能導致MET 14號外顯子跳躍突變。
此外,外顯子14上發生的Y1003突變和部分缺失突變,不會干擾正常的剪接機制,即不會導致外顯子14的錯誤剪下,但因為最終也可以導致MET降解減少、下游訊號的持續啟用,此時也會被報告為MET 14號外顯子跳躍突變。
NGS測序過程中實際檢出的變異往往會跨越多個區域影響RNA剪接,如c.2888-35_2888-17del,這個變異導致內含子-35_-17的區域發生了缺失,影響了BS以及部分PPT區域。c.2888-35_2888del這個變異不僅影響了BS位點、PPT區,還影響了剪接受體位點。這些突變都可能導致MET 14號外顯子跳躍突變。
圖注:研究者在1141例肺癌患者中確定了28名非鱗狀NSCLC患者發生了MET突變。根據以上對於變異型別的分類,可將患者的MET突變分為圖中顯示的4類,其中有些患者的變異涉及多個區域。
不同型別的MET 14號外顯子跳躍突變的發生率如何?
2020年ASCO口頭彙報的一項針對MET 14號外顯子跳躍突變肺癌患者的研究中,作者透過對60495名非小細胞肺癌患者的樣本進行NGS雜交捕獲測序,在1387個樣本中檢測出MET 14號外顯子跳躍突變,包括>500種變異形式,這些突變根據累及的功能位點可分為:剪接供體位點(42%)、剪接受體位點(4.7%)、多嘧啶位點(15%)、剪接受體和多嘧啶位點(13%)、D1010(23%)、Y1003(2.1%)和全外顯子缺失(0.3%)。

圖7 非小細胞肺癌樣本中的MET 14號外顯子跳躍突變事件分佈[5]
怎麼針對報告進行MET 14號外顯子跳躍突變的報告解讀?
第一步:看數字。突變是否發生在外顯子14邊緣,即c.2888,-1/-2和c.3028,+1/+2/+3附近。如果看到c.2942和c. 3082也別先否定,確認轉錄本資訊, 若為NM_001127500.3,也為外顯子14前後。
第二步:看變異。剪接位點邊緣的點突變或缺失是否影響剪下(主要看c.)。
第三步:看範圍。若變異中不包括2888/3028等數字,需判斷髮生變異區域是否包含SA、SD、BS、PPT等功能區域。如BS,c. 2888-29, PPT c. 2888-24_c. 2888-9,以及SA、SD區域。
比如,c.2888-35_2888-17del這個變異, 影響了BS區域(c.2888-29)以及部分的PPT區域(c.2888-24_c.2888-17),推測為MET 14號外顯子跳躍突變。
再比如,c.3020-c.3038+24del, 缺失範圍包括了SD區域,c.3028以及c.3028+1_c.3028+3,也推測為MET 14號外顯子跳躍突變。
第四步:如果是外顯子14上的點突變或缺失,不能輕易下結論。
注:可導致MET 14號外顯子跳躍突變的突變位置多樣化且變異型別多樣化,目前已報道超過500種變異可導致MET 14號外顯子跳躍突變,並且仍有新的位點被報道。如檢測到的突變未查詢到相關文獻報道,或未累及上述經典區域,判斷是否發生MET 14號外顯子跳躍突變,最終需要透過其他檢測方法來驗證,通常認為RNA水平的檢測是比較好的驗證方法,例如RNA NGS和實時聚合酶鏈反應(qRT-PCR)等。
回到一開始的檢測報告,現在你能知道哪個才是MET 14號外顯子跳躍突變了嗎?
國家癌症中心/中國醫學科學院腫瘤醫院病理科主任,主任醫師,教授,博士生導師
中國抗癌協會腫瘤病理專業委員會候任主任委員
中國抗癌協會腫瘤病理專業委員會分子協作組組長
中華醫學會病理學分會分子病理學組副組長
中國醫師協會病理醫師分會分子病理委員會副主任委員
中國研究型醫院學會超微及分子病理專委會副主任委員
中國研究型醫院學會病理學專委會副主任委員
國家腫瘤質控中心單病種質控專家委員會委員
國家抗腫瘤藥物臨床應用監測專家委員會委員
國家藥品監督管理局醫療器械技術評審專家諮詢委員會委員
中國合格評定國家認可委員會CNAS認可評審專家、評定專家
點選下方空白處可以檢視答案
▼
正確答案:
1、ABCD
2、A
參考文獻:
[1] [PMID: 27009743] Drilon, Alexander. “MET Exon 14 Alterations in Lung Cancer: Exon Skipping Extends Half-Life.” Clinical cancer research : an official journal of the American Association for Cancer Research vol. 22,12 (2016): 2832-4. doi:10.1158/1078-0432.CCR-16-0229.
[2] [PMID: 34295201] Fujino, Toshio et al. “Lung Cancer with MET exon 14 Skipping Mutation: Genetic Feature, Current Treatments, and Future Challenges.” Lung Cancer (Auckland, N.Z.) vol. 12 35-50. 20 May. 2021, doi:10.2147/LCTT.S269307.
[3] [ PMID: 25971938] Frampton, Garrett M et al. “Activation of MET via diverse exon 14 splicing alterations occurs in multiple tumor types and confers clinical sensitivity to MET inhibitors.” Cancer discovery vol. 5,8 (2015): 850-9. doi:10.1158/2159-8290.CD-15-0285.
[4] [PMID: 26729443] Awad, Mark M et al. “MET Exon 14 Mutations in Non-Small-Cell Lung Cancer Are Associated With Advanced Age and Stage-Dependent MET Genomic Amplification and c-Met Overexpression.” Journal of clinical oncology : official journal of the American Society of Clinical Oncology vol. 34,7 (2016): 721-30. doi:10.1200/JCO.2015.63.4600.
[5] Awad, M. et al. “Characterization of 1,387 NSCLCs with MET exon 14 (METex14) skipping alterations (SA) and potential acquired resistance (AR) mechanisms.” Journal of Clinical Oncology 38 (2020): 9511-9511.
*此文僅用於向醫學人士提供科學資訊,不代表本平臺觀點
*醫學界力求其發表內容在稽核透過時的準確可靠,但並不對已發表內容的適時性,以及所引用資料(如有)的準確性和完整性等作出任何承諾和保證,亦不承擔因該些內容已過時、所引用資料可能的不準確或不完整等情況引起的任何責任。請相關各方在採用或者以此作為決策依據時另行核查。