歡迎關注凱萊英藥聞
民以食為天,正常的飲食是保證身體健康的基礎。受到一些特定疾病的影響,部分人群需要調整飲食結構以避免病情持續發展。然而,食物甚至食物中的特定物質成為疾病的誘因時,患者只能被迫無奈“顛覆式“地改變飲食結構,對其正常生活造成極大的負面影響。本期新藥巡禮將重點介紹因麩質攝入而引起的疾病--乳糜瀉,和有望成為該病首個治療藥物的奈米微球創新療法TAK-101。
No.1 乳糜瀉
乳糜瀉(celiac disease,CD)是一種遺傳易感人群攝入麥膠蛋白後不耐受引起的自身免疫性疾病。而麥膠蛋白廣泛存在於小麥類食物中,患者在進食麵包、饅頭、麵筋等食物後就會出現的長期慢性腹瀉、便秘、腹痛、腹脹等消化道症狀。如果是幼兒或青少年患者,還有可能出現貧血、體重減輕、生長髮育遲緩、骨密度降低等症狀。
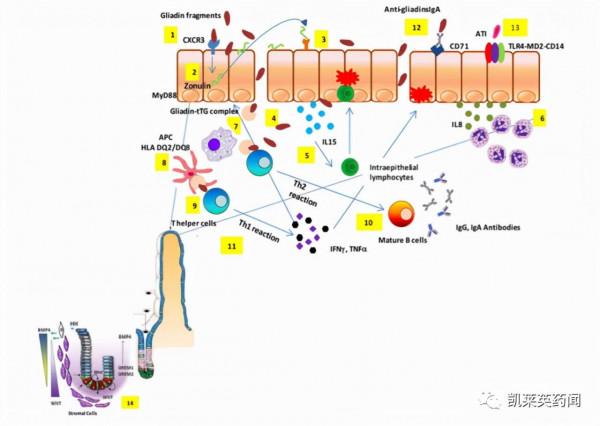
自1888年,英國醫生Samuel Gee首次將乳糜瀉的發病與麥類食品相關聯後,經過進一百年的發展,學界才正式明確小麥類食物中的麥膠蛋白(Gliadin)為乳糜瀉的致病抗原。當麩質不耐受患者攝入麥類食物後,其中的麥膠蛋白無法被完全分解為氨基酸,而是以較大的肽段形式進入小腸黏膜。Caio等人的研究顯示,麥膠蛋白肽段透過與小腸上皮頂端的趨化因子受體3(CXR3)相互作用,引起腸通透性增加和IL-8、IL-15等炎症因子的分泌,進而導致小腸黏膜萎縮、隱窩增生、炎細胞浸潤等症狀的發生。
乳糜瀉患病率較高,根據Prashant Singh等人的流行病學統計分析顯示,全球經小腸活檢診斷為乳糜瀉的患病率約為0.7%,其中南美洲0.4%,非洲和北美洲0.5%,亞洲0.6%,歐洲和大洋洲為0.8%。
全球分國家乳糜瀉患病率情況
(按患病率百分位標註)
由於我國現階段對乳糜瀉的疾病認知尚不充分且缺少大規模流行病學調查資料,部分乳糜瀉患者難以得到有效的診斷和治療。近年來,針對國內成人及兒童慢性腹瀉患者的血清檢驗發現,乳糜瀉特徵血清抗體的陽性率高達1.77%-12%。已被發現的乳糜瀉患者可能只是“冰山一角“。
No.2 奈米顆粒與免疫調節
奈米顆粒(nanoparticles)是指尺寸在1到1500 nm之間的顆粒。它們幾乎可以由任何化合物製成,包括多聚氨基酸、多糖和聚(α-羥基酸)以及金、銀、碳、鐵和二氧化矽等不可降解化合物。根據奈米顆粒的尺寸大小不同,其在體內有不同的生理分佈模式。透過靜脈注射的奈米顆粒大多被脾臟和肝臟中的單核細胞和吞噬細胞所吞噬,可以促進免疫耐受的調節。
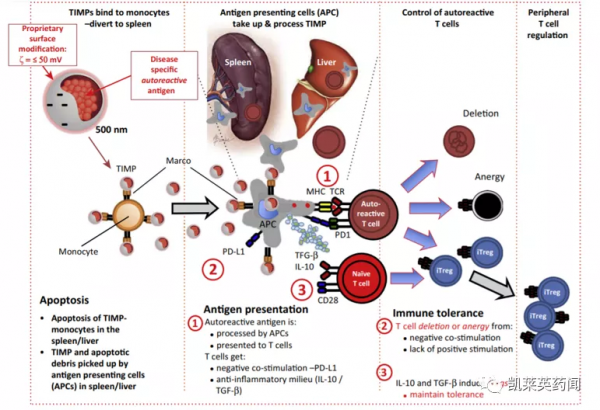
以聚乳酸-羥基乙酸共聚物(PLGA)為代表的生物相容性聚合物在免疫調節中有著巨大的前景。研究發現,攜帶有抗原物質的耐受性免疫修飾奈米顆粒(TIMPs)經靜脈遞送後,在吞噬細胞表面的清道夫受體(scavenger receptor)的介導下被巨噬細胞所吞噬,這一過程中巨噬細胞分泌IL-10和TGF-β並調節抗原呈遞細胞(APC)上PD-L1的表達水平。而後透過誘導初始T細胞(naïve T cell)失能並轉化為調節性T細胞(Treg),從而維持免疫耐受(即對該抗原不引起免疫反應)。
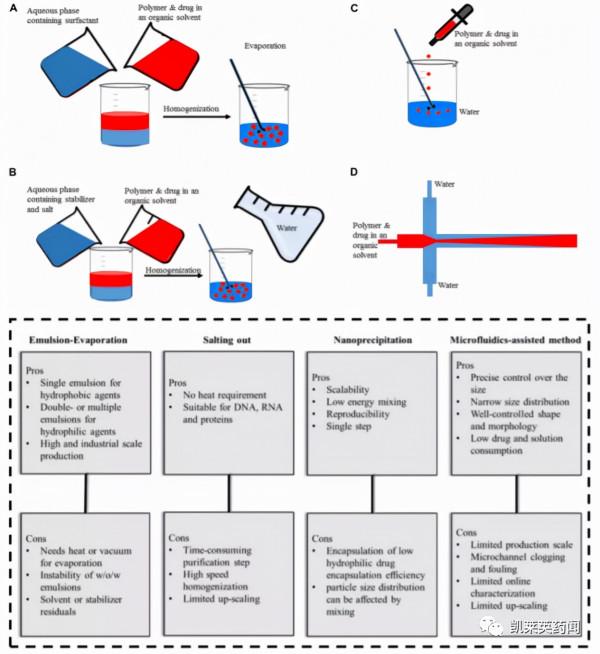
本文重點介紹的TAK-101就是一種PLGA奈米顆粒製劑。目前,PLGA奈米顆粒的製造主要有乳化-溶劑揮發法(emulsification-evaporation,下圖A)、鹽析法(salting-out,下圖B)、奈米沉澱法(nanoprecipitation,下圖C)、微流控輔助法(microfluidic-assisted,下圖D)等,各種製造方法各有優缺點。
No.3 TAK-101
TAK-101是武田製藥從Cour Pharmaceutical引入的一款PLGA奈米顆粒治療藥物,是一種直徑約為500nm,表面帶有負電荷,內部包裹有抗原物質的創新奈米微球。該藥透過CourPharmaceutical獨有的COUR 奈米顆粒平臺(CNP)完成對麥膠蛋白(Gliadin)的包裹。該平臺有效優化了奈米顆粒的粒徑和表面電荷,以實現藥物在肝臟和脾臟中靶向分佈,保證了藥物被靶器官中APC的靶向攝取和免疫調節,避免了抗原在靜脈給藥後引起免疫啟用。
與前期對PLGA相關研究類似,TAK-101被肝臟和脾臟邊緣區表達MACO清道夫受體的耐受性APC吸收,並誘導PD-L1的上調以及TGF-β和IL-10的釋放。而後透過T細胞失能, FOXP3陽性Tregs(iT regs)誘導和Tr1細胞啟用等三種通路實現免疫耐受,避免因麥膠蛋白特異性IFN-γ導致的效應T細胞的啟用和向小腸部位的轉運。
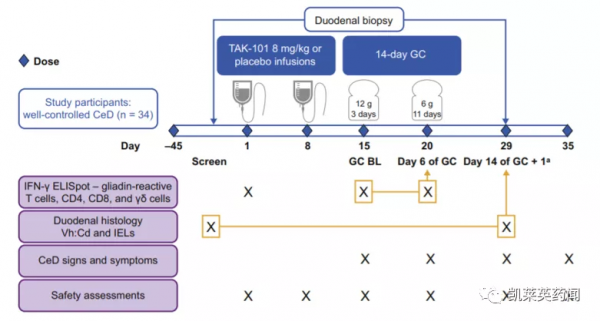
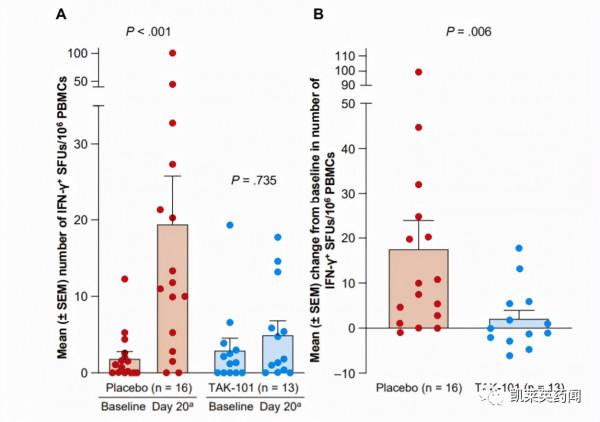
目前,TAK-101已完成了I期和IIa期臨床研究。其中,IIa期臨床(NCT03738475)是一項隨機、雙盲、安慰劑對照、平行分配的臨床研究,於2019年1月啟動,以評估TAK-101對口服麩質後的乳糜瀉患者的安全性、藥效學、療效和藥代動力學。試驗主要終點為與安慰劑相比,麩質刺激(GC)6天后,使用TAK-101治療的患者外周血單核細胞(PBMC)中IFN-γ產生量與基線相比發生的變化。次要終點共有三個:(1)小腸粘膜損傷的減少,透過十二指腸活檢定量組織學評估,絨毛高度與隱窩深度比(Vh:Cd)的變化;(2)上皮內淋巴細胞(IEL)密度變化;(3)血液中活化的CD4+、CD8+和γδ+效應記憶T細胞百分比的變化。
試驗結果顯示,與基線檢查時相比,麩質刺激(GC)6天后,安慰劑組的IFN-γ平均變化為17.58 SFU,TAK101組為2.01 SFU(p=0.006),達到試驗主要終點。
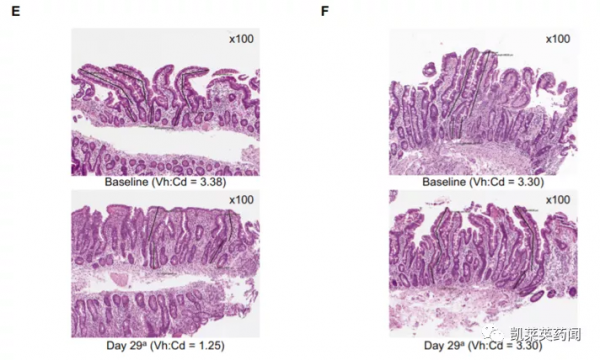
在試驗次要終點方面,安慰劑組和TAK-101治療組在Vh:Cd變化(p=0.080)和IEL密度(p=0.289)兩項指標上無統計學差異。
但組織病理切片結果顯示,與TAK-101治療組(下圖右)的患者相比,安慰劑治療組的患者(下圖左)在14天口服麩質刺激後出現絨毛變平和隱窩深度減少的症狀。
而對於另一次要終點指標,與安慰劑組相比,服用TAK-101的患者CD4+CD38+α4β7+、CD8+CD38+αEβ7+、γδ+CD38+αEβ7+T細胞減少(P=0.013、P=0.004和P=0.010)。
目前,奈米微球在mRNA疫苗以及寡核苷酸藥物遞送系統方面有著廣泛的應用,直接推動了相關藥物的成功開發。隨著TAK-101等管線的持續研發及PLGA等奈米微球技術的不斷進步,免疫治療領域有望迎來一個全新的治療視窗。
參考資料
1. vitapharmed.ch
2. 乳糜瀉研究進展 世界最新醫學資訊文摘,2021
3. 乳糜瀉診斷技術進展. 協和醫學雜誌,2020
4. Celiac disease: a comprehensive current review. BMC Med. 2019 Jul
5. Global Prevalence of Celiac Disease: Systematic Review and Meta-analysis. Clin Gastroenterol Hepatol. 2018 Jun
6. TAK-101 Nanoparticles Induce Gluten-Specific Tolerance in Celiac Disease: A Randomized, Double-Blind, Placebo-Controlled Study. Gastroenterology. 2021 Jul
7. Harnessing nanoparticles for immune modulation. Trends Immunol. 2015 Jul
8. PLGA-Based Nanoparticles in Cancer Treatment. Front Pharmacol. 2018 Nov
9. 公司官網